3.1) Codeine: acțiune centrală antitusivă; alcaloid de fenantren. Un agonist al receptorilor de opiacee care reduce excitabilitatea centrului tusei. Efectul antitusiv central este asociat cu suprimarea centrului tusei. Activitatea analgezică se datorează excitării receptorilor de opiacee din diferite părți ale sistemului nervos central și a țesuturilor periferice, ceea ce duce la stimularea sistemului antinociceptiv și la o modificare a percepției emoționale a durerii. Într-o măsură mai mică decât morfina, deprimă respirația, provoacă mai rar mihoză, greață, vărsături și constipație (activarea receptorilor opioizi din intestin determină relaxarea mușchilor netezi, scăderea peristaltismului și spasmul tuturor sfincterelor). Efectul analgezic se dezvoltă după 10-45 minute după administrarea i / m și s / c și la 30-60 minute după administrarea orală. Efectul maxim este obținut după 30-60 minute după administrarea i / m și 1-2 ore după administrarea orală. Durata analgeziei este de 4 ore, blocajul reflexului de tuse este de 4-6 ore.
3.2) Bromhexina: medicament mucolitic (secretolitic), are un efect antitusiv expectorant și slab. Reduce vâscozitatea sputei (depolimerizează fibrele mucoproteinei și mucopolizaharidelor, crește componenta seroasă a secreției bronșice); activează epiteliul ciliat, crește volumul și îmbunătățește descărcarea de spută. Stimulează producerea de agent activ de suprafață endogen, care asigură stabilitatea celulelor alveolare în timpul respirației. Efectul se manifestă după 2-5 zile de la începerea tratamentului.
3.3) Salbutamol: bronhodilatatorul, în doze terapeutice, are un efect stimulant pronunțat asupra beta2-AR a bronhiilor, vaselor de sânge și a miometrului. Practic nu are efect asupra beta1-AR a inimii. Inhibă eliberarea de mastocite de histamină, leucotriene, PGD2 și alte substanțe biologice active pentru o lungă perioadă de timp. Suprimă reactivitatea bronșică precoce și târzie. Are un efect bronhodilatator pronunțat, împiedică sau oprește bronhospasmul, reduce rezistența în căile respiratorii, crește VC. Crește clearance-ul mucociliar (în bronșită cronică până la 36%), stimulează secreția de mucus, activează funcțiile epiteliului ciliat. Inhibă eliberarea de mediatori inflamatori din mastocite și bazofile, în special eliberarea de histamină indusă de anti-IgE, elimină suprimarea transportului mucociliar dependent de antigen și eliberarea factorului chimiotaxiei neutrofilelor. Previne dezvoltarea bronhospasmului indus de alergeni. Poate duce la scăderea numărului de receptori beta-adrenergici, inclusiv pe limfocite. Are o serie de efecte metabolice: reduce concentrația de K + în plasmă, afectează glicogenoliza și excreția, are hiperglicemie (în special la pacienții cu astm bronșic) și efect lipolitic, crește riscul de acidoză. În dozele terapeutice recomandate, nu afectează în mod negativ CCC, nu provoacă o creștere a tensiunii arteriale. Într-o măsură mai mică, în comparație cu medicamentele din acest grup, are un efect crono- și inotrop pozitiv. Provoacă expansiunea arterelor coronare. După utilizarea formelor de inhalare, acțiunea se dezvoltă rapid, debutul efectului după 5 minute, maximul după 30-90 minute (75% din efectul maxim, obținut în 5 minute), durata este de 3-6 ore.
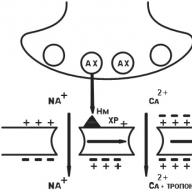
3.4) Atrovent: agentul bronhodilatant, blochează M-XP de mușchii netezi ai arborelui traheobronchial (în principal la nivelul bronhiilor mari și medii) și inhibă bronhoconstricția reflexă, reduce secreția glandelor mucoasei cavității nazale și a glandelor bronșice. Având asemănări structurale cu molecula AX, este un antagonist competitiv. Împiedică eficient îngustarea bronhiilor rezultate din inhalarea fumului de țigară, a aerului rece, a efectelor diverselor bronhospasm și, de asemenea, elimină bronhospasmul asociat cu influența n.vagus. Atunci când este inhalat, practic nu are un efect resorptiv - pentru dezvoltarea tahicardiei este necesară inhalarea a aproximativ 500 de doze, în timp ce doar 10% ajunge la bronhiile și alveolele mici, iar restul se instalează în gât sau în cavitatea bucală și este înghițit. Efectul bronhodilatant se dezvoltă după 5-15 minute, atinge maxim după 1-2 ore și durează până la 6 ore (uneori până la 8 ore).
3.5) Eufilin: un bronhodilatator derivat din purină; inhibă PDE, crește acumularea de cAMP în țesuturi, blochează receptorii de adenozină (purină); reduce aportul de Ca2 + prin canalele membranelor celulare, reduce activitatea contractilă a mușchilor netezi. Relaxează mușchii bronhiilor, crește clearance-ul mucociliar, stimulează reducerea diafragmei, îmbunătățește funcția mușchilor respiratorii și intercostali, stimulează centrul respirator, își mărește sensibilitatea la dioxidul de carbon și îmbunătățește ventilația alveolară, ceea ce duce la o scădere a gravității și frecvenței episoadelor de apnee. Normalizarea funcției respiratorii, ajută la saturarea sângelui cu oxigen și la reducerea concentrației de dioxid de carbon. Îmbunătățește ventilația în hipokalemie. Are un efect stimulant asupra activității inimii, crește forța și ritmul cardiac, crește fluxul sanguin coronarian și cererea miocardică de oxigen. Reduce tonul vaselor de sânge (în principal vasele creierului, pielii și rinichilor). Are un efect venodilator periferic, reduce rezistența vasculară pulmonară, scade presiunea în cercul „mic” al circulației sângelui. Crește fluxul sanguin renal, are un efect diuretic moderat. Extinde tractul biliar extrahepatic. Stabilizează membranele mastocitelor, inhibă eliberarea mediatorilor reacțiilor alergice. Inhibă agregarea plachetară (suprimă factorul de activare a trombocitelor și PgE2 alfa), crește rezistența globulelor roșii la deformare (îmbunătățește proprietățile reologice ale sângelui), reduce tromboza și normalizează microcirculația. Are efect tocolitic, crește aciditatea sucului gastric. Când este utilizat în doze mari, are efect epileptogen.
3.6) Zafirlukast: blocant al receptorului de leucotriene peptidic competitiv, extrem de selectiv (LTC4, LTD4, LTE4), acționează ca un medicament antiinflamator care reduce efectul mediatorilor inflamatori. Nu afectează receptorii pentru Pg, tromboxanii, precum și receptorii colinergici și histaminici. Împiedică reducerea mușchiului neted al bronhiilor (cauzate de toate leucotrienele peptidice), previne o creștere a permeabilității vasculare, umflarea mucoasei și influxul de eozinofile la plămâni; reduce creșterea conținutului de bazofile, limfocite și histamină, reduce producția stimulată de superoxizi prin macrofage alveolare; reduce componentele celulare și non-celulare ale inflamației în căile respiratorii cauzate de provocarea antigenică. Slăbește hiperreactivitatea bronșică și bronhospasm după provocarea de alergeni prin inhalare; cu utilizare prelungită reduce sensibilitatea la metacolină, îmbunătățește funcția pulmonară: reduce obstrucția; previne bronhospasmul cauzat de leucotriena D4 inhalată, dioxid de sulf, exerciții fizice, aer rece. Atenuează fazele precoce și târzii ale reacțiilor inflamatorii cauzate de diverși antigeni: plante, eroare: sursă de referință nu au fost găsite animale, ambrozie și antigene mixte. Acesta reduce numărul de atacuri de zi și de noapte ale astmului bronșic, îmbunătățește funcția pulmonară, reduce nevoia de beta2-adrenostimulante și reduce frecvența exacerbărilor. Debutul acțiunii este în primele zile și săptămâni de admitere.
3.7) Intal: agent antialergic, are un efect de stabilizare a membranei, previne dezreglarea celulelor mastice și eliberarea de histamină, leucotriene (inclusiv bradicinina), Pg și alte substanțe biologice active din acestea, împiedică dezvoltarea bronhospasmului. În plămâni, inhibarea răspunsului mediatorului împiedică dezvoltarea atât a etapelor precoce, cât și a celor târzii ale unei reacții astmatice (ca răspuns la imunități și la alți stimuli). Medicamentul este cel mai eficient pentru prevenirea reacțiilor alergice imediate la pacienții cu o vârstă relativ mică, care încă nu au dezvoltat modificări cronice ireversibile la plămâni. Nu elimină bronhospasmul dezvoltat. Utilizarea pe termen lung reduce frecvența atacurilor de astm bronșic x facilitează cursul acestora, reduce nevoia de bronhodilatatoare și corticosteroizi. Se obține un efect stabil după 2-4 săptămâni. O singură doză durează până la 5 ore.
3.8) Ranitidina: blocant H2-R II generație. Mecanismul de acțiune este asociat cu blocarea membranelor H2-R ale celulelor parietale ale mucoasei gastrice. Suprimă secreția de HCl de zi și de noapte, precum și bazală și stimulată, reduce volumul de suc gastric cauzat de întinderea stomacului prin încărcarea alimentară, acțiunea hormonilor și stimulenților biogeni (gastrina, histamina, acetilcolina, pentagastrina, cofeina). Reduce cantitatea de HCl din sucul gastric, practic fără a suprima enzimele „hepatice” asociate cu citocromul P450, nu afectează concentrația de gastrină în plasmă, producția de mucus. Reduce activitatea. Nu afectează concentrația serică de Ca2 +. După administrarea orală în doze terapeutice, aceasta nu afectează concentrația de prolactină (poate exista o ușoară creștere a concentrației de prolactină în serul din sânge după administrarea iv de ranitidină la o doză de 100 mg sau mai mult). Nu afectează secreția de hormoni hipofizari: gonadotropină, TSH și STH. Nu afectează concentrația de cortizol, aldosteron, androgeni sau estrogeni, motilitatea spermei, numărul și compoziția spermatozoizilor și, de asemenea, nu are efecte antiandrogenice. Poate atenua eliberarea vasopresinei. Îmbunătățește mecanismele de protecție ale mucoasei gastrice și promovează vindecarea daunelor sale asociate cu expunerea la HCl (inclusiv încetarea sângerării gastrointestinale și cicatrizarea ulcerelor de stres) prin creșterea formării mucusului gastric, a glicoproteinelor sale și stimularea secreției de bicarbonat de mucoasa gastrică. sinteza endogenă de Pg în ea și rata de regenerare. La o doză de 150 mg, inhibă secreția de suc gastric timp de 8-12 ore.Inhibă enzimele microsomale (mai slabe decât cimetidina).
3.9) Pirenzepina: blocant M1-XP. Nu penetrează BBB și nu afectează sistemul nervos central; efectul cronotrop nu este foarte pronunțat. În doze terapeutice, nu afectează semnificativ motilitatea tractului gastro-intestinal, vezicii biliare. Inhibă secreția de suc gastric, reduce secreția de gastrină, reduce producția de HCl și pepsină. După stimularea cu histamina blochează secreția de HCl cu 25%; după mâncare - cu 53%; după administrarea insulinei - cu 58%. La 1 oră după masă, pirenzepina reduce HCl cu 48% și cu 30% în 2 ore.Secreția de pepsină stimulată de insulină este redusă cu 49%, histamina cu 34%, gastrina cu 24%. Inhibă eliberarea bicarbonatului din epiteliu în cavitatea stomacului la pacienții cu leziuni erozive ale antrumului și îmbunătățește protecția mucoasei gastrice; crește fluxul de sânge în stratul submucos al stomacului și intestinelor, îmbunătățește microcircularea.
3.10) Omeprazol: inhibitor al pompei de protoni, reduce producția de acid - inhibă activitatea H + / K + -ATPase în celulele parietale ale stomacului și blochează astfel stadiul final al secreției de HCl. Medicamentul este un promedicament și este activat în mediul acid al tubulelor secretoare ale celulelor parietale. Reduce secreția bazală și stimulată, indiferent de natura stimulului. Efectul antisecretor după administrarea a 20 mg are loc în prima oră, maxim - după 2 ore. Inhibarea a 50% din secreția maximă durează 24 de ore. O singură doză pe zi asigură o inhibare rapidă și eficientă a secreției gastrice de zi și de noapte, atingând maximul după 4 zile de tratament și dispărând până la sfârșitul 3-4 zile de la sfârșitul dozei. La pacienții cu ulcer duodenal, administrarea de 20 mg de omeprazol menține un pH intragastric de 3 timp de 17 ore.
3.11) Bicarbonat de sodiu: antiacid. Când este administrat, acesta interacționează cu HCl de suc gastric, neutralizându-l. Crește excreția de Na + și Cl-, diureză osmotică; mutarea reacției mucusului bronșic pe partea alcalină, crește secreția bronșică, reduce vâscozitatea sputei și îmbunătățește expectorația acesteia. Elimină durerea în ulcerul peptic și 12 ulcer duodenal. Efectul antiacid este rapid, dar pe termen scurt, rezultat din reacția de neutralizare a CO2, irită receptorii mucoasei gastrice, îmbunătățește excreția de gastrină cu activarea secundară a secreției și poate provoca senzații neplăcute în stomac (datorită întinderii) și burping. Absorbit, duce la dezvoltarea alcalozei. Alcalizarea urinei previne precipitația acidului uric în tractul urinar. Ameliorează simptomele bolii de mișcare și a bolilor aeriene.
3.12) Dicitrat de tripotassiu al bismutului: agent anti-ulcer cu activitate bactericidă împotriva Helicobacter pylori, are de asemenea efecte antiinflamatorii și astringente. La pH 4 și mai mic (suc gastric), oxiclorură de bismut insolubil și precipitat citrat, compușii chelați se formează cu un substrat proteic (acoperire protectoare insolubilă la locul ulcerului). Creșterea sintezei de PgE, care crește formarea de mucus și secreția de bicarbonat, stimulează activitatea mecanismelor citoprotectoare. Conduce la acumularea factorului de creștere epidermică în zona defectului. Reduce activitatea și pepsinogenul. Îmbunătățește proprietățile protectoare ale mucoasei gastro-intestinale. Crește producția de mucus, rezistența mucoaselor la pepsină, HCl și enzime.
3.13) Metoclopramida: un antiemetic este un blocant specific al receptorilor dopaminei (D2) și serotoninei. Are efect antiemetic, elimină greața și sughițul. Reduce activitatea motorie a esofagului, crește tonul sfincterului esofagian inferior, accelerează golirea stomacului și accelerează, de asemenea, mișcarea alimentelor prin intestinul subțire, fără a provoca diaree. Stimulează secreția de prolactină.
3.14) Oxafenamida: agent coleretic. Are efect coleretic și colekinetic. Îmbunătățește formarea și secreția bilei, ameliorează spasmul mușchilor netezi ai tractului biliar și sfincterului canalului biliar comun, reduce concentrația de colesterol și bilirubină în sânge.
3.15) Zenofalk: sistemul de acid biliar al reglării ficat-intestinale; Are un efect coleretic care scade lipidele, coleretic. Reduce sinteza și absorbția, dizolvă calculii biliari ai colesterolului. Acidul Chenodeoxicolic - acidul biliar primar, reprezintă 20-30% din totalul de acizi biliari. Inhibă sinteza enzimatică a colesterolului în ficat, reducând activitatea HMG-CoA, ceea ce duce la o scădere a concentrației de colesterol în bilă. Modifică raportul dintre acizii biliari și colesterol și predominanța acidului chenodeoxicolic în grupul total de acizi biliari. Modifică cantitativ și calitativ biliara: volumul de bilă secretată crește cu o creștere a concentrației de acizi biliari conjugate, raportul dintre acizii biliari trioxicolici și dioxocholici scade, concentrația acidului glicocolic crește în comparație cu acidul taurocholic și crește concentrația fosfolipidelor.
3.16) Ulei de ricin:laxativ din plante. Atunci când este luat pe cale orală, este hidrolizat de lipază în intestinul subțire cu formarea acidului ricinoleic, care provoacă iritarea receptorilor intestinali (pe întreaga lungime) și îmbunătățirea reflexă a peristaltismului. Efectul laxativ apare după 5-6 ore. De asemenea, provoacă miometru reflex.
3.17) Oxitocină: agent hormonal, analog polipeptidic al hormonului glandei pituitare posterioare. Are acțiune uterotonizantă, stimulând forța de muncă și acțiunea lactotropă. Are un efect stimulant asupra miometrului (în special la sfârșitul sarcinii, în timpul travaliului și direct în timpul nașterii). Sub influența oxitocinei, permeabilitatea membranelor celulare pentru Ca2 + crește, potențialul de repaus scade și cresc (o scădere a potențialului membranei duce la creșterea frecvenței, intensității și duratei contracțiilor). Stimulează secreția de lapte matern, sporind producția de prolactină de către glanda pituitară anterioară. Reduce celulele mioepiteliale din jurul alveolelor glandei mamare, stimulează fluxul de lapte în canalele mari sau sinusuri, contribuind la creșterea separării laptelui. Aproape lipsit de efecte vasoconstrictoare și antidiuretice (numai în doze mari), nu provoacă contracția mușchilor vezicii urinare și intestinelor. Efectul apare în 1-2 minute cu introducerea s / c și / m, durează 20-30 minute; cu iv - în 0,5-1 minute, intranazal - timp de câteva minute.
3.18) Fenoterol: stimulator selectiv al receptorilor beta2-adrenergici, activează adenilat ciclaza, urmat de o creștere a formării de cAMP, care stimulează pompa Ca2 +, care redistribuie ionii de Ca2 + în miocite, rezultând o scădere a concentrației acestora din urmă în miofibrilele. Extinde bronhiile, vasele de sânge, reduce contractilitatea și tonul miometrului, contribuind astfel la îmbunătățirea fluxului sanguin uteroplacental.
3.19) Epoitina alfa: un agent care stimulează eritropoieza, activează mitoza, stimulează formarea globulelor roșii din celulele progenitoare ale eritrocitelor. Glicoproteina purificată este sintetizată în celulele de mamifer în care este inserată o genă care codifică eritropoietina umană. Proprietăți biologice și imunologice identice cu eritropoietina umană, excretate din urină. Aceasta duce la o creștere a hematocritului și a Hb, îmbunătățirea aportului de sânge la țesuturi și funcția inimii. Cel mai pronunțat efect în anemie cauzat de boli renale cronice. O creștere a hematocritului se manifestă la 4 săptămâni după începerea tratamentului.
3.20) Pentoxil: agent imunostimulator, îmbunătățește sinteza acizilor nucleici, stimulează leucopoieza.
3.21) Acid acetilsalicilic: AINS; Are efecte antiinflamatorii, analgezice și antipiretice asociate cu inhibarea nediscriminată a activității COX1 și COX2, care reglează sinteza Pg. Ca urmare, Pg nu este format, asigurând formarea de edem și hiperalgezie. Scăderea conținutului de Pg (în principal E1) în centrul de termoreglare duce la o scădere a temperaturii corpului datorită extinderii vaselor de sânge ale pielii și a transpirației crescute. Efectul analgezic se datorează acțiunii centrale și periferice. Reduce agregarea, aderența trombocitelor și tromboza prin inhibarea sintezei tromboxanului A2 în trombocite. Efectul antiplachetar persistă timp de 7 zile după o singură doză (mai accentuat la bărbați decât la femei). Reduce mortalitatea și riscul de a dezvolta infarct miocardic cu angină pectorală instabilă. Este eficient în prevenirea primară a bolilor de BCV, în special a infarctului de miocard la bărbații mai mari de 40 de ani și în prevenirea secundară a infarctului de miocard. În doză zilnică de 6 g sau mai mult, inhibă sinteza protrombinei în ficat și crește timpul de protrombină. Crește activitatea fibrinolitică plasmatică și reduce concentrația factorilor de coagulare dependenți de vitamina K (II, VII, IX, X). Crește complicațiile hemoragice în timpul intervențiilor chirurgicale, crește riscul de sângerare în timpul terapiei cu anticoagulante. Stimulează excreția acidului uric (perturbă reabsorbția acestuia în tubii renali), dar în doze mari. Blocarea COX1 în mucoasa gastrică duce la inhibarea Pg gastroprotectoare, ceea ce poate duce la ulcerarea membranei mucoase și la sângerare ulterioară. Efectul mai puțin iritant asupra mucoasei tractului gastro-intestinal sunt formele de dozare care conțin substanțe tampon, stratul enteric, precum și forme speciale „efervescente” de comprimate.
3.22) Heparină: anticoagulant acțiune directă, aparține grupului de heparine moleculare medii, încetinește formarea fibrinei. Efectul anticoagulant se găsește in vitro și in vivo, apare imediat după administrarea iv. Mecanismul de acțiune al heparinei se bazează în principal pe legarea sa la antitrombină III, un inhibitor al factorilor de coagulare a sângelui activat: trombină, IXa, Xa, XIa, XIIa (capacitatea de a inhiba trombina și factorul X activ este deosebit de importantă). Crește fluxul sanguin renal; crește rezistența vaselor cerebrale, reduce activitatea hialuronidazei cerebrale, activează lipoproteina lipază și are un efect de scădere a lipidelor. Reduce activitatea agentului tensioactiv în plămâni, suprimă sinteza excesivă de aldosteron în cortexul suprarenal, leagă adrenalina, modulează răspunsul ovarelor la stimuli hormonali și îmbunătățește activitatea hormonului paratiroidian. Ca urmare a interacțiunii cu enzimele, aceasta poate crește activitatea tirozinei hidroxilazei creierului, pepsinogenului, ADN-polimerazei și poate reduce activitatea ATPazei miozinei, piruvat kinazei, ARN polimerazei. La pacienții cu boli coronariene (în asociere cu ASA), acestea reduc riscul de a dezvolta tromboză acută coronariană, infarct miocardic și moarte subită. Reduce frecvența atacurilor de cord și a mortalității recurente la pacienții după infarct miocardic. Este eficient în doze mari pentru embolie pulmonară și tromboză venoasă, în doze mici pentru prevenirea tromboembolismului venos, inclusiv după operație. Odată cu administrarea intravenoasă, coagularea sângelui încetinește aproape imediat, cu injecție intramusculară - după 15-30 minute, cu administrare subcutanată - după 20-60 minute, după inhalare, efectul maxim este într-o zi; durata efectului anticoagulant, respectiv - 4-5, 6, 8 ore și 1-2 săptămâni, efectul terapeutic - prevenirea trombozei - durează mult mai mult. Deficitul de antitrombină III în plasmă sau la locul trombozei poate reduce efectul antitrombotic al heparinei.
3.23) Trombină: agent hemostatic. Trombina - o componentă naturală a sistemului de coagulare a sângelui, este formată în organism din protrombină cu tromboplastina enzimatică din urmă. Primite din plasma donatorilor. Activitatea medicamentului este exprimată în unități de activitate (EA).
3.24) Fibrinogen: agent hemostatic. Componenta naturală a sângelui. Tranziția fibrinogenului la fibrină, care are loc sub influența trombinei, asigură etapa finală a procesului de coagulare a sângelui - formarea unui cheag de sânge. Primite din plasma donatorilor.
Profesorul EpanchintsevaTI
Anii recenți sunt caracterizați de
apariția de noi boli: SIDA,tulburări ale gripei porcine și gripei
boala metabolica
„Civilizație” etc.
Pentru tratamentul bolilor utilizate
medicamente.
Farmacologie (din greacă farmacie - medicament, otravă; predare logos)
este o știință despre interacțiunea substanțelor chimicecompuși cu organismele vii.
Farmacologia studiază în principal
medicamente utilizate
pentru tratamentul și prevenirea diverselor
boli și patologice
state.
Principalele obiective ale farmacologiei:
găsirea și crearea de noi eficiente șimedicamente sigure;
dezvoltarea celor mai eficiente metode
și utilizarea sigură a medicamentelor
medicamente (LP);
cercetare clinică și reevaluare
medicamente vechi;
asistență informațională și
sfaturi medicale
angajaților.
Studii de farmacologie:
efectul substanțelor asupra biologiculuisisteme de complexitate diferită - de la
întreg organism pentru a se separa
celule;
schimbări în funcționare
sistem biologic cauzat de
chimicale -
acțiune biologică (activitate).
Importanța farmacologiei.
Studiul mecanismelor de acțiune a medicamentelorajută la extinderea prezentării:
despre natura chimică a proceselor din
celule vii;
mecanisme de funcționare a tuturor
sistemele corpului uman.
Surse de primire a medicamentului.
Compuși minerali (magneziu)sulfat, sulfat de sodiu);
Țesuturi și organe animale (insulină,
preparate hormonale etc.);
Plante (glicozide cardiace etc.);
Microorganisme (antibiotice etc.);
Sinteza chimică.
Eforturile oamenilor de știință moderni
care vizează reducerea frecvențeiluând medicamente
menținerea eficacității sale;
în timp ce preferința este astfel de
metodele de administrare a medicamentelor
medicamente care nu rănesc
pacientul.
Istoria farmacologiei.
Timp de milenii, căutarea,fabricarea și utilizarea medicamentelor
preparatele au fost efectuate empiric.
În secolul IX arabii au încercat
sistematizare și standardizare
medicamente.
În acest scop, special
cărți de tip
farmacopeea modernă.
Principalele etape ale dezvoltării farmacologiei.
Prima mențiune a medicamentelorplante găsite în egiptean
papirus secolul XVI î.Hr.
Înainte de începutul secolului al XIX-lea, baza studierii și
dezvoltarea de droguri
experiența empirică este expusă fără
profund teoretic științific
anchete.
Farmacologie internă.
În Rusia antică, principalulconsilierii să folosească
medicamente erau
rătăcitori, vindecători, magicieni. Sunt
a avut date aleatorii și ale lor
recomandările nu au fost suficiente
justificate.
Cunoașterea acumulată treptat despre
medicamente.
Primele lucrări scrise de mână (ierboristi).
„Compendiul lui Svyatoslav” (1073),Herbalist cunoscut sub numele de
„Un vânt favorabil” (1534).
Istoric farmacologie internă.
În 1581 primul a fost deschis la Moscovao farmacie.
La începutul secolului XVII. la Moscova a fost aprobat
Comanda farmaceutică care a fost responsabilă
afaceri medicale ale țării.
O importanță deosebită au fost reformele lui Petru I.
Deci, un decret special la Moscova a fost
S-au deschis 8 farmacii, s-au înființat farmacii
grădini de legume, în locul comenzii farmaceutice a fost
Cancelaria de farmacie organizată
(Colegiul medical). Pentru unificarea producției și
calitatea medicamentului în
1778 primul stat
Farmacopeea în latină și 1866. - mai departe
Limba rusă.
Primul ghid intern
Studiul medicinii a fost publicat în 1783.
Se numea „Medical
substanță sau descriere
plante vindecătoare în medicină
folosit ... "de prof. univ. NM
Maksimovic-Ambodik. La sfârșitul secolului al XVIII-lea - începutul secolului al XIX-lea. a devenit
farmacologie științifică să se dezvolte.
Cel mai mare centru de cercetare medicală
în Rusia a avut loc o intervenție medicală și chirurgicală
Academiei (transformată în 1881 în Academia Medicală Militară) din Sankt Petersburg.
AP Nelyubin (1785-1858) este cunoscut pentru
explorarea apelor minerale caucaziene
și Farmacografie sau
prescripții chimice
gătit și mâncat cel mai recent
medicamente ”(1827). OV Zabelin (1834-1875) organizat la
Academia de Farmacologie Specială
laboratorul
Un rol major în dezvoltarea farmacologiei
jucat experimental și clinic
activitatea marii fiziologi și clinicieni.
Deci, N.I. Pirogov și fiziologul A.M.
Filomafitsky a efectuat cercetări
înseamnă pentru anestezie.
În domeniul farmacologiei neurotrope
fonduri deținute de fondator
fiziologie I.M.Sechenov.
I. P. Pavlov
Impact semnificativ asupra dezvoltăriifarmacologie internă a avut
I. P. Pavlov.
În laboratorul experimental,
condus de el, a studiat inima
glicozide, medicamente antipiretice, un număr
ioni.
Pentru prima dată în istoria științei I.P. Pavlov și ai săi
angajații au studiat efectele bromurilor,
cofeina cu activitate nervoasa mai mare in
animale sănătoase și când sunt experimentale
cauzată de nevroză. Laudă înaltă
inițiații merită munca sa
cercetarea digestiei.
Nikolai Pavlovici Kravkov (1865-1924).
Fondatorulanestezie domestică.
El a fost cel care a dovedit
principial
oportunitate și
oportunitate
aplicații
anestezie non-prin inhalare
gedonalom.
Detine o idee
anestezie combinată
(hedonal cu cloroform). N. P. Kravkov a acordat multă atenție
probleme de farmacologie generală:
în funcție de clarificare
efectul biologic al dozei și
concentrația substanțelor
acțiune combinată
agenți farmacologici
relația dintre structură
compuși și fiziologic al acestora
activitate. Stiloul său este conducerea
„Bazele farmacologiei”.
Activitatea științifică a lui N. Kravkov
a fost foarte lăudat de guvern.
În 1926 a fost premiat (postum)
Premiul lui V.I. Lenin.
S. V. Anichkov (1892-1981)
-Lucrările sunt dedicate:
farmacologie
mediator
resurse;
neuroendocrinologie
și,
farmacologie
trofice
procese
toxicologie a BOV.
V.V.Zakusov (1903-1986)
Lucrări principalesunt dedicate
studiu de impact
farmacologic
fonduri pentru
sinaptică
transmiterea excitației în
CNS.
Propunere nouă
medicamente
psihotropă,
anestezice,
relaxante musculare
antianginal etc. A creat Institutul de Farmacologie al Academiei de Științe Medicale
URSS numit după el.
El a fost președintele All-Union
Societatea farmacologilor și
Uniunea Internațională a Farmacologilor.
Mulți ani a fost V.V.Zakusov
Reprezentant al URSS în comisia din
Medicamentele ONU, expert OMS,
membru al Comitetului Executiv al Internaționalului
Uniunea Farmacologilor.
M. D. Mashkovsky (1908-2002)
De 66 de ania lucrat în All-Union
himikofarmatsevticheskom
Institutul.
Autor excelent
carte de referință
„Medicament
inseamna "
rezistența 16
publicații. Regizat și direct
multe originale
preparate:
analgezic opioid - promedol;
α-blocant - tropafen;
bronhodilatator - troventol;
antihistaminice - fencarol și
bukarfen;
antidepresive - azafen, pirazidol:
psihostimulante - Sydnocarb și Sydnofen și
etc.
Z.V. Ermolaeva (1898-1974)
În timpul mareluipatriotic
am luat un război
penicilina.
Foarte cunoscut pentru ea
lucrați mai departe
interferon,
ekmolinu,
antibiotice.
Principalele secțiuni de farmacologie.
Farmacologia este împărțită în general șiconfidențialitate.
Farmacologie generală studierea generalului
modele de interacțiune
medicamente cu vii
organisme.
În farmacologie privată sunt luate în considerare
grupuri farmacologice specifice și
medicamente individuale.
Principiile clasificării medicamentelor.
Clasificarea ar trebui să reflectemulte aspecte:
Structura chimică;
Mecanismul și domeniul de aplicare;
Patologie în care sunt utilizate medicamente
etc.
În prezent, în farmacia internă se folosesc:
ATX - clasificare;Clasificare alfabetică;
Clasificarea chimică;
Clasificarea farmacologică;
farmacoterapie
clasificare;
Clasificare mixtă.
Clasificare ATX.
(Anatomică și terapeutice-chimice).Recomandat de OMS în 1981 și în 1996
Clasificarea ATX a devenit
standard internațional.
Drogurile sunt împărțite în 5 niveluri.
Clasificare ATX.
Conform acestei clasificări a medicamentelorcoduri de șapte cifre alocate
cinci niveluri de sistem: anatomice
zona terapeutică
grup, subgrup farmacologic,
Droguri, subgrupa chimică, număr,
atribuit acestui medicament.
Clasificare alfabetică.
Principiul plasăriinume de medicamente în alfabet
comandă.
Folosit în ediție
cărți de referință enciclopedice.
Clasificarea chimică.
Baza este structura chimicăMedicamente (glicozide, alcaloizi, esteri
simplu și complex, aciclic
conexiuni etc.)
Acest principiu este utilizat în
organice și farmaceutice
chimie.
Clasificarea farmacologică
Este o combinație.Drogurile sunt împărțite în categorii - mari
blocuri corespunzătoare sistemului
organismul asupra căruia acționează drogurile.
Clasificare mixtă.
Include farmacoterapeuticefarmacologice și chimice
clasificare în același timp.
Biletul 4. Întrebarea 4.
Farmacologie – aceasta este o știință care studiază interacțiunea medicamentelor cu organismele vii. Farmacologia, tradusă din greacă, este știința medicinei, farmacologiei (farmacie - medicament sau otravă, logos - predare).
Principalele obiective ale farmacologiei sunt:
1) reglarea medicamentelor a funcțiilor afectate ale unui organism viu;
2) căutarea de noi medicamente eficiente și sigure și introducerea lor în medicina practică.
Farmacologie în sistemul disciplinelor biomedicale și clinice
Farmacologia, fiind o știință biomedicală, este strâns legată de diverse ramuri ale medicinei. În studiul farmacologiei, cunoașterea biochimiei și fiziologiei este în special necesară, deoarece medicamentele, care afectează anumite procese biochimice, provoacă modificări în organele și sistemele corespunzătoare. Cunoașterea fiziologiei patologice este, de asemenea, extrem de importantă, deoarece medicamentele sunt de obicei folosite pentru corectarea funcțiilor modificate patologic. Fără dezvoltarea cu succes a acestor discipline, este foarte dificil să navighezi corect procesele care au loc în organismele vii și, dacă este necesar, să le corectezi.
Pe de altă parte, farmacologia contribuie la dezvoltarea în continuare a biochimiei, fiziologiei, fiziopatologiei și a altor discipline teoretice. Deci, multe substanțe farmacologice care controlează anumite procese biochimice și fiziologice într-un organism viu, contribuie la dezvăluirea și analiza mecanismelor care le stau la baza.
Farmacologia și farmacia, componentele farmacologiei moderne, se îmbogățesc și se îmbunătățesc reciproc. Farmacia, care s-a remarcat într-o direcție separată datorită dezvoltării rapide a științei medicamentelor, include în prezent următoarele discipline:
1) chimie farmaceutică;
2) farmacognozie;
3) tehnologie farmaceutică;
4) managementul și economia farmaciei.
Progresul farmacologiei contribuie la dezvoltarea disciplinelor clinice. Astfel, descoperirea medicamentelor psihotrope eficiente a contribuit la dezvoltarea rapidă a psihiatriei, la apariția medicamentelor pentru anestezie, anestezice locale și relaxante musculare au permis chirurgiei să se ridice la un nivel cu totul nou. Tratarea cu succes a bolilor infecțioase a devenit posibilă numai după descoperirea agenților antibacterieni eficienți. Există multe alte exemple de astfel de îmbunătățiri în diferite domenii ale medicinei practice, care se bazează pe succesul farmacologiei. Importanța farmacologiei pentru clinică nu poate fi supraestimată. Acest lucru este confirmat de faptul că în ultimii ani, farmacologia clinică a devenit o disciplină independentă.
Astfel, farmacologia, ca disciplină independentă, este legătura dintre cunoștințele teoretice și medicina practică. IP Pavlov a scris: „Pe un teritoriu vast de cunoștințe medicale, farmacologia pare a fi o industrie de graniță, unde există un schimb deosebit de viu de servicii între baza natural-științifică a medicinei - fiziologia și cunoștințele medicale în special - terapia și unde, prin urmare, marea utilitate reciprocă a unei cunoștințe este resimțită mai ales alta ".
Cunoașterea farmacologiei este necesară pentru un medic de orice specialitate. Un vechi doctor indian din Sushrut a scris: „Trăim într-o lume a drogurilor. În mâinile ignoranților, medicamentul este otravă și, în efectul său, poate fi comparat cu focul, în mâinile oamenilor cunoscuți este asemănat cu o „băutură a nemuririi”. În prezent, de asemenea, „prevederea că substanța medicamentoasă și otrava sunt unul și același lucru este una dintre principalele contradicții în farmacologie. Prin natura sa, ea continuă să rămână ambiguă, deoarece toate obiectele și fenomenele sunt caracterizate de contradicții interne, deoarece au laturile lor negative și pozitive ”(PV Sergeev). Astfel, medicamentele pot vindeca boli și pot duce la pierderea sănătății și, uneori, la moarte și numai în mâinile unui medic competent medicamentul va beneficia pacientul.
Principalele etape ale dezvoltării farmacologiei
Farmacologia este la fel de veche ca omenirea însăși. Chiar și oamenii antici au observat cum diverse substanțe de origine vegetală, minerală și animală acționează asupra organismului animalelor și oamenilor. Experiența și observațiile personale au constituit baza cunoștințelor despre acțiune terapeutică diverse substanțecare apoi a început să fie folosit ca medicament. Surse care au ajuns la noi indică faptul că cu câteva mii de ani înaintea erei noastre, diferite popoare aveau deja o idee despre natura efectului asupra oamenilor a numeroase medicamente, inclusiv unele utilizate în prezent
(de exemplu, ulei de ricin etc.). Informațiile despre plantele medicinale au fost transmise oral din generație în generație și, după apariția scrisului, au început să fie menționate pe tablete de lut, papirus etc. Deci, primele surse scrise (4000 î.Hr.) - comprimate de lut din Assyria - conțin o descriere a unui număr mare de plante medicinale. De-a lungul timpului, cunoștințele dobândite în medicină și în special în farmacologie.
Prima încercare de sistematizare a informațiilor despre acțiune substanțe medicinale a fost întreprins de un medic de excepție grecia antica Hipocrate (460-377 î.Hr.), descriind aproximativ 230 de plante medicinale. Hipocrat a legat dezvoltarea bolii cu un dezechilibru de patru lichide: sânge, mucus, bilă neagră și galbenă, așa că a folosit pe scară largă diuretice, laxative, medicamente diaforice și îngrijirea sângelui pentru a trata bolile. Hipocrate credea în acțiunea drogurilor, dar el credea că „ceea ce medicamentele nu vindecă, vindecă fierul; ceea ce fierul nu vindecă, vindecă focul; de ce focul nu se vindecă, atunci ar trebui să fie considerat incurabil ". Hipocrate a formulat cele mai importante principii care stau la baza medicamentului: „Primum non nocere” (în primul rând, nu face rău) și „Natura sanat, medicus curat morbus” (Natura vindecă, medicul tratează bolile).
În Roma antică, învățătura sa a fost dezvoltată de Galen (131-20 î.Hr.). Galen a asociat boala cu colmatarea sângelui, astfel că metodele sale de tratament au avut ca scop purificarea sângelui. Galenul, la fel ca Hipocrat, medicamente utilizate pe scară largă care „curăță sângele” și curgerea sângelui. Galen a propus să pregătească perfuzii și extracte din plante medicinale pentru a evidenția principiul de vindecare al medicamentelor. acestea forme de dozare sunt încă utilizate în practica medicală și sunt numite galenice.
Reprezentantul proeminent al medicinei arabe, Abu Ali al-Hussein Ibn Sina (Avicenna (980-1037)), în lucrarea sa „Canon of Medicine”, a descris aproximativ 700 de plante medicinale și metode pentru prepararea medicamentelor din ele. Medicii arabi au introdus o mulțime de medicamente noi în medicină (în primul rând compuși metalici, medicamente), au căutat „elixirul tinereții veșnice”, au fondat primele farmacii (765), au creat farmacopeea și averea farmaciștilor. Datorită acestui fapt, separarea finală a farmaciei de medicament a avut loc.
Unul dintre oamenii de știință de seamă ai Renașterii a fost profesorul de la Universitatea din Basel, Philippe-Aureol-Teofrast-Bombast von Hohenheim (Paracelsus (1493-1541)), fondatorul direcției chimico-vitaliste în medicină („tatăl iatrochimiei”, din cuvântul grecesc уatros - doctor). A introdus în terapie metalele necunoscute anterior și sărurile lor. Paracelsus credea că, în natură, există un medicament pentru fiecare boală, iar sarcina medicului este să o găsească.
Un reprezentant proeminent al vremii respective a fost Hahnemann (1755-1843), fondatorul homeopatiei (de la boala homoios - similară și patosă). Principalele dispoziții ale învățăturii sale sunt următoarele:
1) legea asemănării ar trebui să fie tratată astfel, adică boala poate fi vindecată de un medicament care, în cantități mari, provoacă un boala de droguri»;
2) medicamentele trebuie testate pe persoane sănătoase și nu pe bolnavi și pentru a stabili toate fenomenele care apar după administrare;
3) deoarece, pe măsură ce doza scade, rezistența medicamentului crește, medicamentul trebuie utilizat în doze mici.
Farmacologia ca știință independentă s-a format în secolul al XIX-lea (de pe vremea când știința studierii funcțiilor organismului animal a început pe calea unui „experiment exact” pe animale). Primii experimentatori au fost Francois Magandy și Claude Bernard. Francois Magandie (1783-1855) a început pentru a monitoriza efectele medicamentelor (metale și alcaloizi (stricnina etc.)) în timpul intervențiilor chirurgicale. Studentul său, renumitul fiziolog Claude Bernard (1813-1878), a pus bazele farmacologiei experimentale moderne și ale toxicologiei datorită numeroaselor sale experimente privind studiul mecanismelor de acțiune ale medicamentelor și otrăvurilor (publicat pentru prima dată în 1857 la Paris).
În Rusia antică, informațiile cu privire la efectul substanțelor medicinale au fost împrăștiate și scoase din natura înconjurătoare, în principal din plante. Apariția mănăstirilor a contribuit la concentrarea informațiilor despre efectul medicamentelor în rândul călugărilor, care la acea vreme erau cei mai educați. Informațiile au fost transmise în „ierbaliști” scrise de mână (de exemplu, cunoscutul „Blagodladnoy vertograd”, 1534), „cărți medicale”.
Chiar și în secolul al XVII-lea, rușii au fost reticenți să se angajeze în medicină, care a fost considerată apoi aproape de „cunoașterea demonică”. Numai Petru I (1672-
1725) a ordonat să învețe „tinerilor ruși limba latină, arta desenului, anatomia, chirurgia, cunoștințele de consum medical” (adică medicamente).
Odată cu deschiderea Universității din Moscova (1755), a Academiei Medicale și Chirurgicale din Sankt Petersburg (în 1799), a Universităților Kazan și Harkov (1804), farmacologia a devenit obiectul predării. Apoi apar primele orientări ruse cu privire la farmacologie, de exemplu, profesorul obstetrician-ginecolog Kazan N. M. Ambodik (1744-1812) - „Substituția medicală sau descrierea plantelor de vindecare”, profesorul farmacolog din Moscova A. A. Nevsky (1796-1844) - „ Schița farmacologiei generale ”(1835), profesor de farmacie și farmacologie al Academiei de Chirurgie Medicală și Chirurgicală din St. Petersburg A. P. Nelyubin (1785-1858), trei volume„ Farmacografie sau prezentare chimico-farmaceutică și farmacodinamică a preparatului și utilizării ultimele medicamente„(1852) și alții.
Studiile din această perioadă nu sunt numeroase, dar unele dintre ele merită atenție în prezent. De exemplu, primul studiu științific asupra proprietăților și utilizărilor apelor minerale caucaziene, realizat de profesorul A.P. Nelyubin (1823).
În Rusia, o metodă experimentală pentru studierea efectelor medicamentelor a fost aplicată pentru prima dată de un profesor de la Universitatea din Moscova A.A. Sokolovsky (1822-1891), care a studiat efectele diferitelor medicamente asupra sistemului nervos, a prezentat noi principii pentru farmacoterapia bolilor sistemului nervos și a emis o serie de orientări. Profesorul V. I. Dybkovsky (1830-1870) este autorul unor lucrări experimentale excelente asupra influenței otrăvurilor asupra corpului uman, precum și a manualului „Lectures on Pharmacology” (1871). Profesorul O.V. Zabelin (1834-1875) a organizat un laborator de farmacologie la Academia Medicală și Chirurgicală din Sankt Petersburg și a efectuat o serie de lucrări experimentale (cu privire la acțiunile sărurilor de arsen, citrat de cafeină, zahăr din lapte etc.).
NI Pirogov (1810 - 1881) a efectuat lucrări experimentale asupra efectului narcotic al eterului și a sugerat utilizarea anesteziei eterice.
În 1860, I.M. Sechenov (1829 - 1905) a efectuat cercetări cu privire la efectul diverselor substanțe asupra sistemului neuromuscular.
Din 1890 până în 1895, Departamentul de Farmacologie al Academiei Medicale Militare a fost condus de marele om de știință rus I.P. Pavlov (1849 - 1936). În timp ce era încă șeful laboratorului, el a investigat efectul asupra inimii unui număr de glicozide cardiace. În laboratoarele fiziologice ale I.P. Pavlov, metoda reflexelor condiționate a fost prima care a dat o justificare experimentală a efectului bromurilor, a numeroase substanțe narcotice și stimulante asupra cortexului cerebral (1910-1936).
De remarcat este activitatea Academicianului N.P., extrem de valoroasă pentru farmacologia rusă. Kravkova (1865-1924) - fondatorul școlii naționale de farmacologi. Timp de un sfert de secol, a direcționat multe dintre lucrările laboratorului său (peste 120) și a realizat personal aproximativ 50 de lucrări științifice dedicate studierii mecanismului de acțiune a medicamentelor, a scris un manual, Fundamentals of Pharmacology, reimprimat de 14 ori. N. P. Kravkov a pus bazele dezvoltării farmacologiei patologice (a studiat efectul medicamentelor în condiții patologice experimentale). Un interes considerabil sunt lucrările sale privind toxicologia, farmacologia sistemului cardiovascular, glandele endocrine și metabolismul. El a studiat mai întâi efectul medicamentelor asupra organelor izolate, a creat un medicament pentru anestezia intravenoasă și a sugerat utilizarea anesteziei combinate.
Crearea Institutului de Medicină Experimentală All-Union, UIEM, VIEV și apoi Academia de Științe Medicale a URSS au oferit condiții favorabile dezvoltării gândirii teoretice farmacologice. Din 1938, a început să fie publicată o revistă specială, Farmacologie și Toxicologie și au fost create mai multe manuale noi.
Marele Război Patriotic din 1941-1945 a făcut solicitări mari farmacologilor și toxicologilor în căutarea și studiul aprofundat și testarea de noi medicamente pentru tratarea rănilor și a condițiilor de șoc, prevenirea și tratarea infecțiilor în masă, stimularea sistemului nervos central, etc. O atenție deosebită a fost acordată chimioterapiei sintetice pentru infecții bacteriene etc.) și antibiotice. În acest moment, Z.V. Ermolieva (1898-1974) a primit penicilină.
Acum farmacologii se confruntă cu sarcinile dificile de a găsi noi medicamente sigure pentru tratamentul bolilor tumorale, boli ale sistemului cardiovascular, boli virale, etc. În paralel cu acestea, sunt studiate medicamente deja cunoscute, noi posibilități de utilizare a acestora, precum și metode de corectare sunt dezvoltate. efecte secundarecauzate de ei.
Mijloace care afectează apetitul și procesele de digestie.eu. Mijloace care afectează pofta de mâncare
1. Mijloace care cresc pofta de mâncare
1.1. Mijloace de acțiune reflexă -
amărăciune (tinctura de pelin)
1.2. Tipul central de acțiune este
cyproheptadine (peritol).
1.3 Mijloace care stimulează procesele metabolice
Insulina, steroizi anabolici (retabolil).
2. Anorexice
2.1 Mijloace care afectează catecolaminergice
sistem (stimularea sistemului nervos central)
2.2 Analogi și derivați ai fenaminei -
fepranon, desopimon.
2.3 Derivați ai izoindolului - mazindolului.
2.4 Mijloace care afectează serotonergicele
Sistemul (depresiv sistemul nervos central) - fenfluramina.
II. Mijloace pentru reducerea secreției stomacului
Creșterea funcției secretorii a glandelor
stomac (pentagastrină, histamină, histaglobulină,
tabel. „Limontar”, cărbune min de apă etc.).
Terapie de înlocuire
(suc gastric, pepsină, pepsidil,
acid clorhidric, acidin-pepsină, abomin).
Tinctură de pelin, pepsină, acid clorhidric, orlistat, sibutramină.
pepsină este una dintre principalele enzime proteolitice ale tractului digestiv. Este produs în celulele mucoasei gastrice într-o formă inactivă - sub formă de pezinogen pro-enzimatic, care se transformă în enzima activă pepsină în conținutul gastric.
Pepsin hidrolizează legăturile peptidice și descompune aproape toate proteinele naturale; joacă un rol important în procesele de digestie. În scopuri medicale ca medicament primi pepsină din mucoasa stomacului porcului.
Este produs într-un amestec cu zahăr pudră.
O pulbere albă sau ușor gălbuie, cu un gust dulce, cu un miros slab deosebit. Solubil în apă și 20% alcool.
De obicei utilizat în combinație cu acid clorhidric diluat (vezi) pentru afecțiuni digestive: achile, hipoacide, gastrită anacidă, dispepsie etc.
GRAS WESTERN AMESTRE.
FOARTE DE RĂZBOI DE POVEST (Herba Artemisiae absinthii).
Folia Artemisae absinthii).
Se recoltează și se usucă iarba (la începutul înfloririi) și se lasă (înainte de înflorire sau la începutul înfloririi) unei plante erbacee perenne de pelin în creștere sălbatică (Arthemisia absinthium L.), fam. asteri (Asteraseae).
Conține glicozide: absintină și anabsintină, uleiuri esențiale, vitamina C, taninuri și alte substanțe.
Aplicat sub formă de tinctură, infuzie, ceai, extrage ca amărăciune pentru a stimula apetitul și pentru a spori activitatea organelor digestive. Face parte din ceaiul delicios și tinctura amară.
Extract de pelin gros (Extactum Absinthii spissum). Extras din iarba de pelin. O masă densă de culoare maro închis cu un miros aromat de pelin, un gust amar; formează o soluție tulbure cu apă
Tinctura de pelin (Tinctura Absinthii). Tinctură (1: 5) pe 70% alcool. Un lichid limpede de culoare brun-brun, cu un miros caracteristic și un gust foarte amar.
Omeprazol -derivat al benzimidazolului substituit. Reduce aciditatea sucului gastric. Medicament antiulcer care inhibă funcția pompei de protoni a celulelor parietale ale stomacului. La pH neutru este ineficient. În mediul acid al tubulelor celulelor parietale, se transformă într-un metabolit activ sulfenamidă, care inhibă ireversibil membrana H, K - ATPază. Astfel, este un prodrug. Inhibă eficient secreția bazală și de altă natură a acidului clorhidric. Reduce volumul total al secreției gastrice și inhibă eliberarea de pepsinogen. Are activitate gastroprotectoare. Castle nu schimbă producția factorului intern. Absorbit rapid. Alocați cu un ulcer de 12 intestine, stomac, ulcer peptic esofagită peptică, cu sindromul Zollinger-Ellison. Bine tolerat, rapid biotransformat. Durerea de cap, diareea, greața etc. sunt posibile. De obicei apare hipergastrinemie compensatorie.
pirenzepina- blochează receptorii m1-colinergici. Este un compus triciclic derivat din benzodiazepină. Nu trece bariera sânge-creier. Blochează receptorii m1-colinergici ai celulelor enterochromaffinului și ganglionilor parasimpatici ai stomacului. Inhibă secreția bazală și a acidului clorhidric și pepsinogenului cauzate de iritanții specifici. De asemenea cauzele antiacide- Pentru a reduce aciditatea excesivă a sucului gastric. Sunt baze care reacționează cu acidul clorhidric și îl neutralizează. Bicarbonatul de sodiu este un remediu cu acțiune rapidă. Acesta provoacă formarea de dioxid de carbon în stomac. Aceasta duce la o distensie a stomacului și poate fi cauza separării secundare a acidului clorhidric. Acționează o perioadă scurtă de timp, este solubil în apă, se absoarbe ușor și poate fi cauza alcalozei sistemice. Almagell- utilizat pentru ulcerul peptic al stomacului și 12 intestine, gastrită hiperacidă și alte procese inflamatorii ale tractului gastrointestinal. Conține un gel de hidroxid de aluminiu, hidroxid de magneziu și sorbitol D. Precipitatul de carbonat de calciu formează dioxid de carbon. Acționează repede. Nu provoacă acțiune sistemică. În doze mari, hipercalcemie și alcaloză sistemică. Uneori constipație.