薬力学
薬力学は、身体に対する薬物の作用の特徴を研究する一般的な薬理学のセクションです。 すなわち、薬力学の研究:
薬物の作用機序;
最終的な薬理効果;
薬物の作用のさまざまな条件への依存;
反復投与に対する薬物の効果;
薬物の複合作用;
薬物の不適合性;
副作用 薬用物質.
薬物の作用メカニズムは、物質が薬理効果を引き起こす方法です。 薬物の作用の主なメカニズムは次のとおりです。
物理的。
直接的な化学的相互作用のメカニズム。
膜(物理化学)。
酵素(生化学)。
受容体。
直接的な化学的相互作用。 これは、薬物の作用のかなりまれなメカニズムであり、その本質は、薬物が体内の分子またはイオンと直接相互作用することです。 そのような作用機序は、例えば解毒剤のグループに属するユニチオール薬によって所有されている。 重金属の塩を含むチオール毒による中毒の場合、ユニチオールはそれらと直接化学反応を起こし、尿中に排泄される非毒性複合体の形成をもたらします。 したがって、制酸薬も作用し、塩酸との直接的な化学的相互作用を起こし、胃液の酸性度を低下させます。
膜 (物理化学) メカニズム。 これは、膜貫通電位を決定するイオン電流(Na +、K +、Cl-など)に対する薬物の効果に関連しています。 このメカニズムによると、麻酔薬、抗不整脈薬、局所麻酔薬など。
酵素的 (生化学) メカニズム。 このメカニズムは、いくつかの薬物が酵素に対して活性化または阻害効果を発揮する能力によって決定されます。 そのような作用機序を備えた薬物の兵器庫は非常に広い。 たとえば、抗コリンエステラーゼ薬、モノアミンオキシダーゼ阻害剤、プロトンポンプブロッカーなど。
受容体メカニズム。 人体には、受容体と相互作用し、身体のさまざまな器官または組織の機能を変化させる、非常に特異的な生物学的に活性な物質(メディエーター)があります。
受容体は、特定の化合物に対して選択的な感度を持つ高分子構造です。 薬物と受容体の相互作用により、生化学的および生理学的変化が発生し、何らかの臨床効果が伴います。
受容体を活性化し、生物学的効果を引き起こすメディエーターと薬物は呼ばれます アゴニスト。 受容体に結合するが、それらの活性化および生物学的効果を引き起こさず、アゴニストの効果を低減または排除する医薬品 拮抗薬。 また割り当てる 拮抗薬 -同じ受容体のサブタイプに対して異なる働きをする物質:一部の受容体サブタイプを刺激し、他のサブタイプをブロックします。 たとえば、麻薬性鎮痛薬ナルブフィンは、オピオイドカッパ受容体を刺激し(したがって、痛みの感受性を低下させます)、オピオイドmu受容体をブロックします(したがって、薬物依存の観点からは危険性が低くなります)。
物質が受容体に結合する能力は、「親和性」という用語で呼ばれます。 同じ受容体に関連して、異なる物質の親和性は異なる場合があります。
次のタイプの受容体が区別されます。
細胞膜受容体:
チャネル型:N型コリン作動性受容体、筋肉型Hコリン作動性受容体、GABA受容体;
gタンパク質受容体:αおよびβアドレナリン受容体、M 3コリノ受容体。
統合型受容体:受容体なし。
サイトゾル。
ミトコンドリア。
核
チャネル型受容体
N n 神経型コリン作動性受容体 (CNS、自律神経節、副鼻腔ゾーン、クロム親和性副腎組織)。 アセチルコリン(AX)とH nコリン作動性受容体の結合後、Na +チャネルが開き、Naが細胞に突入し、正電荷を帯びます。 シナプス後膜は脱分極しています。 ニューロンの膜に沿って移動する活動電位があり、電気的に依存するNa +チャネルを開きます。 神経節後神経線維に神経インパルスが発生します(図6)。
図 6. N n-コリン作動性受容体
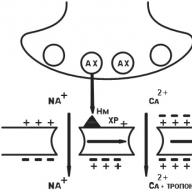
N m 筋肉型コリン作動性受容体 (骨格筋細胞膜)。 初期プロセスは似ていますが、電気的に依存するCa ++チャネルが開きます。 Ca ++イオンが筋線維に入り、Ca ++が筋小胞体から放出されます。 Ca ++のレベルが上昇し、筋肉の収縮を誘発します(図7)。

図 7. N m-コリン作動性受容体
GABA受容体。 これらは、γ-アミノ酪酸(GABA)の受容体です。 GABAはGABA受容体と相互作用し、その構造には塩化物チャネルがあります。 受容体刺激の結果として、チャネルが開き、塩素イオン(Cl-)が自由に細胞に入ります。 細胞内の塩素イオン濃度の増加は、膜の過分極とニューロンの活動の減少につながります。 そのような細胞を励起することはより困難です(図8)。
 図 8. GABA受容体:
図 8. GABA受容体:
GABA-R-GABA受容体、BD-R-ベンゾジアゼピン受容体、BR-バルビツール酸受容体
に関連する受容体 G たんぱく質
Gタンパク質、すなわちGTP結合(グアノシン三リン酸結合)タンパク質は、細胞膜に局在しており、α、β、γサブユニットから構成されています。 それら(Gタンパク質)は、特定のエフェクター(インスタントメッセンジャー、二次中間体)の活性を調節します。 これらのメッセンジャーはエンズマ(アデニル酸シクラーゼ、ホスホリパーゼ)である可能性があります。 カリウム、カルシウム、ナトリウムのチャネル; いくつかの輸送タンパク質。 各細胞は多くのGタンパク質を持つことができ、それぞれが細胞の機能を変えながら、さまざまなメッセンジャーの活動を調節します。
M 3 コリン受容体 (平滑筋膜(MMC)および外分泌腺細胞)。 アセチルコリンは、Gタンパク質に結合したM 3 -XRを刺激します。 ホスホリパーゼ-C(FLS)が活性化され、PIDP(ホスファチジルイノシトール二リン酸)のITP(イノシトール三リン酸)およびDAG(ジアシルグリセロール)への切断を触媒します。 MMCの細胞質に入るITFは、CavesからCa ++を放出します .

図 9. M 3-コリン作動性受容体
Ca ++はカルモジュリンに結合し、ミオシンキナーゼ(MK)を活性化し、ミオシン軽鎖のリン酸化を触媒し、細胞収縮を引き起こします(図9)同様に、分泌腺のシナプスでインパルスが伝達されます。
ノルエピネフリンは刺激する α 1 アドレナリン受容体次の一連のイベントを開始することにより:
ノルエピネフリン(HA)→α1アドレナリン受容体→G sタンパク質のαサブユニットの活性化→PLLの活性化→FIDF切断→ITF濃度の増加→細胞内のCa 2+濃度の増加→Ca 2+がカルモジュリンに結合→ミオシンキナーゼが活性化→軽鎖がリン酸化→軽鎖 ミオシン→ミオシンはアクチンと相互作用します→MMCの減少が発生します(図10)。

図 10.α1-アドレナリン受容体
1 受容体(図11)。 ノルエピネフリン→1 -APを活性化→Gタンパク質のαサブユニットの活性化→ACの活性化→ATPからのcAMPの形成の増加→心筋細胞のcAMP濃度の増加→プロテインキナーゼの活性化→カルシウムチャネルタンパク質のリン酸化→チャネルを介したCa 2+流入の増加とCa濃度の増加 細胞内の2+→心臓の収縮力の増加。

図 11。 receptor 1受容体
2 受容体(図12)。 ON→2 -AR→Gタンパク質のαサブユニットの活性化→ACの活性化→cAMP形成の増加→プロテインキナーゼの刺激→ミオシンキナーゼのリン酸化を触媒するキナーゼは切断されますが、後者の活性は失われます→ミオシンリン酸化は発生しません→HMCの緩和
神経終末からのHAの放出の調節は、α2 -APシナプス前膜の興奮時に神経伝達物質自体によって行われます。 HAの放出は減少します。

図 12。 receptor 2受容体
統合型受容体
これらは、膜を貫通するタンパク質である受容体です。 この場合、タンパク質の外側の部分が受容体の役割を果たし、内側の部分が触媒の役割を果たします(図13)。

図 13。 統合型受容体
サイトゾル受容体
生理学的条件下では、そのような受容体はステロイドホルモン(性ホルモン、糖質コルチコイド)を結合する働きをします。 これらの物質は細胞に入り、そこで細胞質受容体に結合します。 この複合体は核を貫通し、そこでゲノムの働きを変えます。 その結果、細胞内のタンパク質合成が変化します(図14)。

図 14。 サイトゾル受容体
ミトコンドリア受容体
ミトコンドリアには、天然ホルモンT 3の類似体である塩酸トリヨードサイロニンなど、薬用物質と相互作用する受容体もあります。 この相互作用の結果、ATP合成が増加します。
核内受容体
T 3は核を貫通し、このタイプの受容体と相互作用します。 その結果、ゲノムの働きが変わり、新しいタンパク質が合成されます。
最終的な薬理効果(Vershininによる)
薬物が豊富にあるにもかかわらず、体内で薬物によって引き起こされる変化は同じタイプのものです(図15)。 臓器に対する任意の薬物の効果は、5つの主要な薬理効果(N.V. Vershininによる)に減らすことができます:
なだめる -臓器機能の正常化(鎮静剤の使用)。
抑圧 -体の機能の標準以下に低下する(麻酔薬の使用)。
麻痺 -臓器機能の低下の停止(麻薬性鎮痛薬の過剰摂取の場合の呼吸抑制)。
調子を整える -機能の正常化への強化(β1アドレナリン模倣薬の使用)。
興奮 -標準を超えて臓器の機能を高める(中毒の場合の利尿薬の使用、去expect薬)。

図 15.最終的な薬理効果
薬物の作用の種類
主なものは二次的です。
リバーシブル、リバーシブル。
まれに、治療目標に必要なもの 不可逆 機能から構造をオフにします。 これは、たとえば、DNAヘリックス細胞(「架橋」)または細菌酵素の要素と強い(共有)結合を形成できるほとんどの抗菌性抗腫瘍剤に適用され、その結果、細胞は再生能力を失います。
直接、間接(間接)。
間接的なアクションの特殊なケースは 反射 アクション。 たとえば、皮膚の感覚神経の端の刺激の結果としての血管拡張および栄養組織の改善。
選択的、非選択的。
ローカル、吸収性。
吸収性 (全身)作用は、薬物が血液に吸収された後に発生します。 薬の大部分はこの効果があります。
薬物動態に影響を与える要因
と薬力学
I.外部要因
環境:
季節(テトラサイクリンを服用した後の夏には、日焼けが起こる可能性があります(薬物は紫外線に対する皮膚の感受性を高めます));
周囲温度(暑い気候では、中枢神経系を抑制する薬のより強い効果が現れます);
o 2の分圧(エピネフリン(アドレナリン)頻脈により引き起こされる)は、O 2の高い分圧でよりよく許容されます。
薬物の特性:
溶解度(可溶性Ba 2 CO 3は毒性であり、不溶性Ba 2 SO 4は毒性ではありません);
ラジカル(モルヒネ分子の窒素原子のCH 3-基の-CH 2 -CH \u003d CH 2-基(ナロキソン)による置換は、物質中のモルヒネに拮抗する特性の出現をもたらす);
異性(プロプラノロールの回転異性体(アナプリリン)は右旋性より40〜60倍強力です)。
極性(極性分子は通常、脂質膜への溶解性が低いため、吸収が不十分で、細胞膜への浸透が不十分です)。
体内の薬物の摂取:
II。 内因子
生物オブジェクト:
種の特徴(ウサギはヒトの致死量のアトロピンに容易に耐えられる);
民族的特徴(モンゴロイド人種では、アルコール脱水素酵素欠乏症がより一般的であり、その結果、エタノールに対する感受性はヨーロッパ人よりも高い)。
年齢(新生児および幼児では、肝臓が薬物を代謝する能力が低く、腎臓が完全に機能せず、体内の水分量が成人よりも高くなります。高齢者では、薬物の代謝が低下し、年齢とともに腎機能が低下します);
性別(男性の多くの薬物の除去は、男性の性ホルモンが肝臓の酵素を活性化すると考えられているため、女性よりも速くなります);
遺伝子型(欠陥のある(不活性な)偽コリンエステラーゼ、筋弛緩薬スキサメトニウム(ジチリン)の投与後の呼吸停止は、ほとんどの患者のように2〜3分持続しませんが、スキサメトニウムの破壊率の急激な低下(偶発同期性)のため2〜3時間以上持続します );
表現型(肥満の人では、親油性薬物(フェノバルビタールなど)は、薄いものよりも大幅に累積されます)。
身体の生理学:
栄養(食物は薬物の薬物動態に重大な影響を与える可能性があり、ほとんどの場合、薬物の吸収を遅くし、減少させます);
妊娠(胎盤関門を通過する多くの薬物が胎児の発達に影響を与える可能性があります);
授乳(母親と子供が使用する抗生物質は牛乳を受け取ります。これにより、例えば、彼は腸内細菌症になります);
ストレス(興奮した人は刺激効果のある物質に最も敏感です);
概日リズム(尿中のpHが低下する夜間、腎臓によりスルホンアミドがよりゆっくりと排泄される)。
病的状態:
疾患(肝臓の肝硬変患者では、バルビツール酸塩やクロルプロマジンなどの薬物が異常に長い効果を引き起こす可能性があります);
アルコール依存症(エチルアルコールは、中枢神経系の抗不安薬、抗けいれん薬、抗うつ薬に対する効果を高めます);
喫煙(喫煙者の体内での多くの薬物の生体内変化はより速くなります(女性の喫煙者における併用経口避妊薬の有効性の低下))。
用量は、体内に導入された薬物の量であり、 薬理効果.
通常、用量は、質量、体積(グラム、ミリリットル)の単位で表されます。 作用単位(ED)では、断続的な活動を伴う生物学的起源の特定の薬物(ホルモン、抗生物質、ヘパリンなど)が投与されます。
用量分類
管理時まで:
一回限り;
日当;
もちろん。
行動の力によって:
医学的または治療的(最小、中、高);
毒性(最小、中、致死)。
飽和用量とは、組織内で必要な濃度の薬物を作成できる用量です(例えば、強心配糖体の治療)。
維持量-除去中の薬物の損失を補うために、薬物の血漿および組織濃度を維持できる用量(たとえば、デジタル化)。
ショック用量は、特定の内因性基質との競合に必要な薬物の最適濃度を作成できる用量です(例えば、合成段階で葉酸分子の構造内の場所でパラアミノ安息香酸(PABA)との競合に必要なスルファニルアミドのショック用量)。 、薬物は中程度の治療用量で処方され、ほとんどの患者では毒性効果なしに最適な治療効果が得られます。 通常、このような用量は最大治療量の1/2または1/3です。
最小治療と最小毒性の間の用量範囲は呼ばれます 治療効果の幅(SHTD) . 治療作用の幅が広ければ広いほど、薬物はより安全になります(図16)。
SHTD

図 16.治療行動の幅
1-最小治療用量、2-平均治療用量、
3-最大治療用量、4-最小毒性用量
治療指数 (TI)は、次の式によって決定される、平均用量に対する毒性用量の比率です。
tD 50は、患者の50%で中毒を引き起こす用量です。
ED 50-平均治療用量、つまり患者の50%で治療効果を引き起こす用量。
TIが多ければ多いほど、薬はより安全になります。 薬が安全であるためには、そのTIは3以上でなければなりません。
小児および高齢者では、薬物の投与量には独自の特性があり、これはこれらのグループの生理学的な違いに関連しています。
子供の体の特徴:
肝臓の代謝機能の障害(したがって、薬物はより毒性が高い);
皮膚および粘膜は豊富に血管新生しています(したがって、薬物は成人よりもよく吸収されます)。
BBBはより透過性が高くなります(これにより、脳内の薬物濃度が比較的高くなります)
組織の水分含有量が高い;
脂肪組織が少ない
程度は低いですが、薬物は血漿タンパク質に結合します(遊離(活性)画分が増加するため、これは毒性反応を引き起こす可能性があります)。
腎臓の排泄機能が低下します(これにより薬物の作用が長くなります)。
小児および成人における薬物の薬力学と薬物動態に十分な有意差があることを考慮すると、小児の薬物の用量を計算する場合、年齢に比例した成人の用量の単純な用量比例的減少は受け入れられません。 予測不能な結果につながる可能性があります。
小児の線量は、体重1キログラム、生涯、体表面積あたりで計算されます。 例:
子供の投与量\u003d成人の投与量×子供の体重/ 70 kg
老人の生理的特徴:
萎縮およびジストロフィーの変化の結果としての肝臓での薬物の代謝の違反;
体内の水分含量が低く、脂肪組織の含量が高い;
血漿タンパク質の減少(これにより、薬物の遊離部分が増加します);
腎排泄機能の進行性の低下;
中枢神経系と心血管系は、薬物の作用により敏感です。
薬物の副作用(望ましくない)
望ましくない効果とは、病気を治療、診断、または予防するために使用されたときに発生する、体に有害な薬物に対する反応を意味します。 副作用は、臨床診療で薬物を使用した場合の1〜30%で発生します。 薬物があり、その使用は非常に頻繁に望ましくない反応を引き起こします。 これらには、抗生物質、糖質コルチコイド、非ステロイド系抗炎症薬、抗てんかん薬、抗腫瘍薬などの薬が含まれます。 薬物の望ましくない効果は、いくつかのグループに分類できます。
血中の薬物の治療濃度に関連する望ましくない効果:
アレルギー反応;
擬似アレルギー反応;
遺伝的に決定された反応(特異性);
精神的および身体的依存の症候群。
擬似アレルギー反応 (アナフィラキシー様)は、IgE合成なしで、マスト細胞に対する薬物の直接的な効果によって特徴付けられます。 とは異なり アレルギー反応、それらは用量依存的です。 原則として、患者には負担のかかるアレルギー歴はありません。 偽アレルギー反応は、アンピシリン、ヨウ素を含む放射線不透過性物質、局所麻酔薬などによって引き起こされる可能性があります。
特異性 -薬物に対する遺伝的に決定された不耐性。 遺伝的反応は予測できません。 それらは、酵素系の遺伝的欠陥または遺伝性代謝疾患に関連しています。
たとえば、偽コリンエステラーゼ欠乏症には、ジチリンの破壊の抑制が伴います(これにより、筋弛緩が長期化する)。 グルコース-6-リン酸デヒドロゲナーゼの欠乏は、多くの還元酵素(グルタチオンレダクターゼなど)の活性の低下を伴います。 酸化剤(スルホンアミド、ニトロフラン、抗マラリア薬-キニーネ、チンカミン、プリマキンなど)の体内への侵入は、赤血球の溶血の形成とメトヘモグロビンの形成につながります。 筋小胞体の遺伝性異常は、主に麻酔の実践で使用されるハロタン、バルビツール酸および他の薬物が使用される場合、アクトミオシンおよび一般的な酸塩基状態へのカルシウム固定の障害を伴う。 悪性高熱が発生し、患者の死亡につながる可能性があります。
精神的および身体的依存 (中毒)。 薬物は、アヘンやそのアルカロイド(モルヒネ、コデイン、ヘロイン)、プロメドール、コカイン、アンフェタミン、エタノール、いくつかのバルビツール酸塩などの薬物によって引き起こされます。
陶酔感は、コントロールされていない薬物の使用または開発の根本原因です 精神的中毒。 陶酔感は、不快な感情、恐怖感、不安の消失または鈍さによって特徴付けられます。 再び幸福感を経験したいという願望は、精神的依存の原因です。
身体中毒 離脱症候群(離脱症候群または剥奪症候群)の出現に関連する:悪寒、高体温、血圧の急激な変動、筋肉および関節痛、嘔吐、不安、敵意、不眠症。 さらに、症状の数と強度は身体的依存の程度に関連しています。
おそらく、身体的依存の発生のメカニズムは、フィードバック原理により麻薬性鎮痛薬が麻薬受容体を活性化し、内因性の麻薬ペプチドの放出を抑制し、徐々にその活性を置き換えるという事実によるものです。 鎮痛剤の廃止の結果として、以前に投与された鎮痛剤と内因性ペプチドの両方の機能不全があります。 キャンセル症候群が発生します。
血中の薬物の毒性濃度に関連する望ましくない効果(主に治療効果の幅が狭い薬物の特徴):
腎毒性(アミノグリコシド);
耳毒性(アミノグリコシドの長期使用は、不可逆的な難聴の発症まで、難聴につながる可能性があります)。
血液毒性(抗生物質レボミセチンは、造血系に抑圧効果があります);
神経毒性(フルオロキノロンロメフロキサシンのグループからの抗菌薬は不眠症、頭痛を引き起こします);
胃毒性(長期使用のサリチル酸塩は消化性潰瘍疾患につながる可能性があります);
肝毒性
心毒性(抗腫瘍抗生物質)。
血中の薬物濃度に依存しない望ましくない効果:
共生;
重複感染;
ビタミン欠乏症;
免疫不全。
重複感染 高度に活性な抗生物質や他の抗菌剤を使用して開発されています。 その発生は、抗生物質がそれらに敏感な微生物叢を抑制し、抗生物質(無病原性または条件付き病原性)に耐性のある微生物叢が集中的に増殖し始め、特定の条件下で新しい病気-重複感染を引き起こす可能性があるという事実によるものです。
薬物の胚および胎児への悪影響
現代の状況に特に関連するのは、人間の胎児に対する治療濃度と毒性濃度の両方の薬物の効果の問題です。 妊娠中の女性に薬を処方する場合、胎盤関門に浸透し、胎児の血中に現れて悪影響を与える可能性があるため、細心の注意が必要です。
そのような影響は次のとおりです。
胚毒性効果。
催奇形性効果。
胎児毒性効果。
催奇形性効果 主に妊娠3週目から10週目までに薬を服用した結果として起こります(私は妊娠期)。 この期間中に、組織および器官形成が発生します。 催奇形性効果は、胎児組織の分化の違反です。そのため、四肢、頭、および内臓の奇形を持つ子供が生まれる可能性があります。 欠陥の特性に応じて、子供は生存できず、出生後すぐに死亡するか、一生無効になっている場合があります。
催奇形性の影響の例としては、サリドマイドの使用による四肢の発育不良(ホコメリア)があります。 妊娠中のアンドロゲンの使用は、女性の胎児の男性化につながります。 テトラサイクリンを大量に使用すると、胎児の骨に薬物が蓄積し、その発達が阻害されます。
胎児毒性効果 -これは、成熟した胎児または既に成熟した胎児の薬物に対する反応の結果であり、生命機能の変化を引き起こす可能性があります。 たとえば、インドメタシンおよび他のいくつかのNSAIDは、動脈管の閉鎖または狭窄を引き起こします。 アミノグリコシド系抗生物質は耳毒性を引き起こします。 抗凝固剤は、新生児の出血を引き起こす可能性があります。 抗甲状腺薬の使用には、甲状腺腫の発生が伴います。 これらの毒性反応は、胎児および新生児の重篤な病理を引き起こし、子供の周産期死亡率を増加させる可能性があります。
薬物の繰り返し導入で発生する現象
臨床状態では、薬物が一度使用されるケースは多くありません。 これはレンダリングで発生します 救急医療。 ほとんどの場合、薬物は再び処方されます。 この場合、以下のタイプの反応が観察されます。
累積 体内の物質の蓄積です( 材料の蓄積)またはその効果( 機能累積) 確率 素材 蓄積が高いほど、体内での薬物の不活性化が遅くなり、組織内の生体基質に強く結合します。 蓄積は、さまざまな合併症や毒性反応の数と重症度が急速に増加するため、常に危険です。 バルビツール酸塩、強心配糖体などは、最も蓄積されやすく、機能的蓄積により、中毒になる治療効果の増加は、薬の物理的蓄積を時間内に追い越します(そうではないかもしれません)。 したがって、アルコール依存症では、中枢神経系の機能の変化が増加すると、せん妄の発症につながる可能性があります。 この場合、物質(エチルアルコール)は急速に酸化され、組織内に残留しません。 その神経向性効果のみが要約されています。
公差 (中毒性)-これは徐々に弱くなる(完全に失われるまで) 治療作用 長期使用の薬物。 耐性にはさまざまな原因があり、通常、この薬理学的グループのすべての代表者と並行して発症します。 次の反応の結果である可能性があります。
受容体の数の増減;
薬物によって引き起こされるシフトを補う恒常性調節メカニズムの機能を強化する(例えば、体液貯留、心拍数の増加、血管緊張を増加させる他のメカニズムの結果としての高血圧患者の血圧低下血管拡張薬の増加);
彼またはミクロソーム酵素の別の化学因子による誘導の結果としての薬物の不活性化を加速した。
同じ薬物の投与量を単純に増やすことによって中毒を克服しようとする試みは効果がなく、薬物療法の合併症の発生を伴う。
タキフィラキシー -数時間または数日以内に嗜癖が急速に発生した場合の迅速な耐性のオプション。 たとえば、エフェドリンに対する耐性は、薬物の2回目の投与ですでに発生しています。
離脱症候群 次の場合に薬物が突然停止すると発生します:
通常の病原性薬物療法の終了後(例えば、IHDの悪化-硝酸塩、β遮断薬);
禁断症状を引き起こす可能性のある薬物の廃止(麻薬性鎮痛薬、精神安定剤、精神刺激薬);
治療の完了時に、体内でアナログが生成される薬物(グルココルチコイド、甲状腺ホルモン); これらの薬物を服用すると、内因性ホルモンの産生を阻害する可能性があり、これには薬物依存が伴います。
跳ね返り症候群 (リコイル現象)-一種の離脱症候群です。 この現象の本質は、規制プロセスまたは別の反応の脱抑制であり、以前は薬物によって抑制されていました。 結果として、治療前のレベルと比較しても、病気の急激な悪化を伴う一種の過補償があります。
予防する最善の方法は、薬物の漸進的中止でもあります。
薬物中毒 (トピック「 副作用 薬用物質」)。
薬物相互作用
複数の同時管理 薬 同時にいくつかの問題があるときに使用されます。 ただし、1つの疾患の治療では、治療効果を高めるため、および(または) 副作用.
たとえば、フェンタニルの鎮痛効果を高めるために、ドロペリドールと併用されます。
ヒドロクロロチアジドによって引き起こされる低カリウム血症を軽減するために、パナンギンが処方されています(アスパラギン酸カリウムが含まれています)。
治療効果を高め、副作用を減らすために、レボドパはカルビドパと併用されます。
病気を治療するために科学的に不当に多くの薬が使用される治療のタイプは、と呼ばれます ポリファーマシー。
ある薬剤が体内に入った場合、約90〜95%の症例でその運命(薬物動態)とその効果(薬力学)について結論付けることができます。 2種類の薬-ケースの50%のみ、および3種類以上の薬が体内に入る場合-最大10%。 これに加えて、薬物の併用による副作用のリスクも増加する必要があります:5薬物まで使用すると5%、20%-最大8薬物、40%-最大15薬物。
薬物の相互作用は望ましくなく、有害な場合があります。 薬物の治療特性の弱体化、副作用または毒性作用の発生の可能性。 そのような場合、彼らは話します 薬物の非互換性.
たとえば、ペニシリンは成長する微生物に対して殺菌効果があり、テトラサイクリンはタンパク質合成を破壊し、細菌の成長を阻害します。 これに関して、テトラサイクリンはペニシリンの効果を弱めます。
薬物相互作用は次のとおりです。
医薬品
薬理学。
たとえば、酸性媒体中ではアミノフィリンの有効成分であるテウフィリン-が沈殿するため、同じ注射器でアミノフィリンの溶液とピポルフェンまたはアスコルビン酸の溶液を組み合わせるのは不可能です。
薬理学 相互作用は次のように分類されます。
薬物動態;
薬力学。
薬物の薬物動態学的相互作用は、さまざまなレベルで発生する可能性があります。
吸引。
胃腸管のpHに対する薬物の影響-制酸薬の使用は胃のpHの上昇につながり、その結果、弱酸性薬物の吸収、したがって、これらの物質の影響が減少します。
胃腸の運動性に対する薬物の効果-M-抗コリン薬と麻薬性鎮痛薬は、胃腸管の運動性を遅くし、粘膜との薬物のより長い接触を引き起こし、刺激を引き起こす可能性があります(たとえば、アスピリンを使用する場合)
配布。
代謝。
排泄。
薬力学的相互作用 -これは、薬物の一方が他方の薬理効果の生成と実行のプロセスを変更するときの薬物の相互作用です。 薬力学的相互作用は2つの方法で発生します。
相乗効果。
拮抗。
要約-2つ以上の薬物の効果を単純に加算すると(たとえば、エタクリル酸とフロセミドの2つの利尿薬を併用すると、利尿効果が合計されます)、このタイプの相互作用は式1 + 1 \u003d 2で表されます;
増強-薬物の組み合わせの薬理効果が、別々に処方された各薬物の薬理効果の数学的な合計よりも大きい相互作用のタイプ(例えば、抗精神病性抗精神病薬では、ドロペリドールはオピオイド鎮痛薬フェンタニルによって引き起こされる鎮痛効果を著しく高めます); このタイプの薬物相互作用は、式1 + 1 \u003d 3で表されます。
拮抗作用 -これは、体内での全体的な薬理効果が個々の薬物の効果の合計よりも小さい場合、同時に使用される薬物の反対の効果です。 次のタイプの拮抗作用があります。
物理的、物質の物理的相互作用に基づいています(たとえば、活性炭は毒素を吸着します)。
薬物の化学的相互作用に基づく化学物質(例えば、酸性度の増加、制酸剤による胃内の塩酸の中和);
競合的拮抗作用は、物質の構造が類似しており、同じ受容体に対して競合する場合に観察されます(たとえば、M-コリン遮断薬アト\u200b\u200bロピンとM-コリン様ピロカルピンがM-コリン作動性受容体への結合を競合します)。
異なる受容体に作用する場合、物質の反対の効果で非競合的な拮抗作用が観察されます。 非競争的拮抗は 機能的物質が同じ器官の異なる受容体に作用するとき(たとえば、アドレナリンの興奮作用や心機能に対するアセチルコリンの抑制作用) 生理的物質が異なる器官の異なる受容体に作用する場合(例えば、アルドステロンは腎臓に作用して血圧を上昇させ、クロニジンは中枢神経系に作用して血圧を低下させます)。
薬理学、そのセクション、タスク、および医学、生物学、専門分野の中での位置。 国内の薬理学の成果。
薬理学 -薬用物質の生物医学および身体への影響; より広い意味では、一般的な生理活性物質の科学と生物系への影響。
セクション:一般および非公開。 一般:1)医薬品の生産の原理、その組成と特性2)代謝-薬物動態と薬力学、3)毒物学、4)薬理遺伝学5)薬理ゲノミクス。
レシピの定義と構造。 処方箋。 処方に関する一般規則。 処方する毒性、麻薬、強力な薬の特徴。
レシピ-これは、投薬形態、用量、使用方法を示す、患者への薬物の放出に関する薬剤師への医師の訴えです。 これは、無料または優先的に薬物を調剤する場合の医学的、法的、金銭的な文書です。 投与量10進法の質量または体積単位で表され、アラビア数字で示されます。 グラム全体の数は、コンマ(1.0)で区切られます。 より一般的に使用されるもの:0.1-1デシグラム。 0.01-1センチグラム; 1.001 1ミリグラム。 薬を構成する滴はローマ数字で示され、その前に書かれています gtts。 したがって、レシピの生物作用単位は500,000単位を示します。 液体物質 レシピでは、ml(0.1 ml)で示されます。 レシピは、署名と個人の印鑑によって認定されています。 処方箋には、患者の年齢、処方日、姓、患者のイニシャルが記載されている必要があります。 医師の姓とイニシャル、薬の支払い順序。 さらに、優先レシピは、スタンプとシールがある特別なフォームに書き込まれます。 別のサンプルの特別な形式では、麻薬物質、睡眠薬、食欲不振誘発薬のリストからの薬も処方されています。 さらに、医師は処方箋を処方し、署名を入れ、個人の印鑑で証明します。 さらに、それは主治医または彼の代理人によって署名され、処方箋には丸印と医療印があります
機関。 同じ処方手順は、蛋白同化ステロイド、フェノバルビタール、シクロドール、塩酸エフェドリン、クロニジンにも定義されています( 目薬、アンプル)、スノレフの軟膏。 他の処方形態では、抗精神病薬、精神安定剤、抗うつ薬、エチルアルコールを含む薬などが処方されます。外来患者には、麻酔、クロロエチル、フェンタニル、ソンブレビン、ケタミンのためにエーテルを処方することは禁じられています。 レシピは言葉で始まります レシピ (Rp。 -短縮形で)、「テイク」を意味し、書き出された名前と量がリストされます
属格の場合の医薬品。 最初にプライマリと呼ばれ、次に補助と呼ばれます。 次に、必要な剤形が示されます。 例えば Misce ut Fiat pulvis(M. f。 プルビス)-「粉を作るために混ぜる。」 ドーズドライトの場合: " ダ・テイルズがヌメロを投与10 "-"は、そのような線量を10 "で発行します。 単語の後のレシピの終わりに シグナ(S)-ロシア語(または各国語)の「指定」は、薬の使用方法を示します。
一般的な薬理学、そのセクション。 例 一般的なメカニズム 薬の効果。 薬と毒の概念。
1)薬物の生産の原理、その組成と特性2)代謝-薬物動態(体内での吸収、分布、生体内変換の原理)および薬力学(身体に対する薬物の効果の原理)3)毒物学、4)薬理遺伝学(医学セクション) 遺伝学と薬理学、への身体の反応の性質を研究 薬 遺伝的要因に応じて)。 5)薬理ゲノミクス(薬物に対する反応における各人の遺伝的変異の影響を研究する医薬品および薬理学の分野)
体内で薬物を使用する場合、後者は特定の受容体、酵素、細胞膜に作用したり、細胞物質と直接相互作用することができます。 特定の受容体に対する効果は、主に高分子構造が特定の化学化合物に対して選択的に敏感であるという事実に基づいています。 化学物質と受容体の相互作用には、身体の生理学的、生化学的変化が伴い、最終的に臨床効果が決まります。 医薬品-臨床試験を受けており、血液、血漿、およびヒトまたは動物の臓器、組織から得られた処方された方法で、国の認可機関による疾患の予防、診断、治療に使用が承認されている薬剤(物質または物質の混合物) 植物、鉱物、合成またはバイオテクノロジーの使用。 したがって、医薬品には、薬理活性を持ち、生産および製造を目的とする植物、動物、または合成起源の物質が含まれます 剤形. 毒 -中毒、中毒、病気、病的状態など、体重に比べて少量でも体の破壊を引き起こす物質。
薬力学
それは、薬物の作用メカニズム、ならびにその生化学的および生理学的効果を研究します。 彼女の仕事には、薬物と標的細胞の間の化学的および物理的相互作用の説明、ならびにその薬理効果の全範囲と重症度が含まれます。 薬力学的パターンの知識により、適切な薬を選択できます。 薬力学的研究は、体内の生化学的および生理学的プロセスの調節についてより深い理解を提供します(Katzung B.G.、1998; Lawrence D.R. et al。、2002)。
ほとんどの薬物の作用は、身体の高分子への結合によって媒介されます。 これらの高分子の機能的状態の変化は、薬理学的効果に変換される一連の生化学的および生理学的反応を引き起こします。 化学物質が相互作用する高分子は、受容体と呼ばれます。 したがって、機能的に活性な高分子は、薬物の受容体として機能します。 この声明からいくつかの重要な結果が得られます。 まず、薬物の助けを借りて、体内の生理学的プロセスの速度を変えることができます。 第二に、薬物は細胞の自然な生理学的機能のみを変化させ、新しい特性を与えません。
受容体
ほとんどの受容体はタンパク質です。 これらは、ホルモン、成長因子、メディエーター、最も重要な代謝および調節反応に関与するタンパク質(ジヒドロ葉酸還元酵素、アセチルコリンエステラーゼ)、輸送タンパク質(Na +、K + -ATPase)、構造タンパク質(チューブリン)の受容体です。 抗腫瘍剤と相互作用する核酸など、異なる化学的性質の細胞成分も受容体として機能します。
内因性調節因子の受容体-ホルモン、メディエーターなどは、薬理学的に重要です。 これらの受容体は多くの薬物の標的として機能し、通常、内因性リガンドに対する受容体の高い特異性により選択的に作用します。 受容体に結合すると、内因性リガンドの生理学的効果を再現する薬は、アガニストまたは刺激薬と呼ばれます。 この効果を引き起こさないが、内因性リガンドの結合を阻害する薬物は、アンタゴニストまたはブロッカーと呼ばれます。 その作用がアゴニストの作用よりも顕著でない物質は、部分アゴニストと呼ばれます。 非活性化コンフォメーションで受容体を安定化する製剤は、逆アゴニストとして分類されます。
構造的および機能的依存
薬物の化学構造は、受容体および内部活性に対する親和性をかなり厳密に決定します。 化学構造のわずかな変化は、薬理学的特性に大きく影響します。
新薬の合成は、主にこれに基づいています。 化学修飾は必ずしもすべての薬理学的特性に等しく影響を与えるわけではないため、薬物の有効性と安全性を改善し、その選択性を高め、薬物動態特性を改善することが可能です。 たとえば、診療所で使用される多くのホルモンおよびメディエーターアンタゴニストは、内因性物質の化学修飾によって合成されます。
薬物適用ポイント
薬物の効果は受容体によって媒介されるため、薬物の適用ポイントはその分布の特徴だけでなく受容体の局在によっても決定され、薬理効果はこれらの受容体の機能的重要性に依存します。 受容体が多くの臓器や組織に共通している薬物の薬理効果は多様です。 これらの受容体が細胞に不可欠な機能を果たす場合、治療目的で薬物を使用することは困難であるだけでなく、安全でもありません。 それにもかかわらず、そのような薬は臨床的に非常に重要です。 そのため、心不全で広く使用されている強心配糖体は、細胞の生命活動が依存する細胞膜を通るイオンの輸送を変化させます。 それらは治療範囲が狭く、非常に有毒です。 別の例は、抗腫瘍薬です。 薬物が相互作用する受容体が数種類の分化細胞にのみ存在する場合、その効果はより選択的です。 これらの薬物は副作用が少ないかもしれませんが、それでも、それらの受容体が重要な機能を果たす場合、これらの薬物は有毒かもしれません。 いくつかの生物学的毒物(ボツリヌス毒素など)も同様に作用します。 さらに、直接的な薬理効果が選択的であっても、その結果はより多様になる可能性があります。
内因性調節因子受容体
受容体という用語は、薬物が結合する細胞の高分子成分を指します。 最も重要な薬物受容体の1つは、内因性の調節因子(ホルモン、成長因子、メディエーター)の受容体として機能する細胞タンパク質です。 内因性リガンドに結合することにより、受容体はそこからのシグナルを標的細胞に伝達します。
受容体から、シグナルは細胞標的(エフェクタータンパク質)に直接到達するか、中間シグナル分子(タンパク質変換体)を介して到達します。 受容体、タンパク質変換体、およびエフェクタータンパク質は、受容体-エフェクターシステムを形成します。 シグナル伝達鎖の最も近いエフェクタータンパク質は、しばしばターミナルエフェクターではなく(細胞機能に直接影響する)、第二のメディエーターの形成、輸送、または不活性化に関与する酵素または輸送タンパク質、つまりイオンまたは小分子です。 次に、2番目のメディエーターはさまざまな細胞内標的に情報を転送し、1つの受容体からのシグナルに対する同時応答を保証します。
受容体、変換タンパク質、およびエフェクタータンパク質は情報を伝達するだけではありません。 また、一方では異なるリガンドからのシグナルを調整し、他方ではこれらすべてのシグナルを細胞内の代謝プロセスと調整します。
触媒として作用する受容体は、生体信号を増強します。 この重要な特性により、それらは医薬品の優れたターゲットとして機能します。 しかし、シグナルアンプは酵素活性を持つ受容体であるだけでなく、すべての既知の受容体です。 実際、単一のリガンド分子がイオンチャネルに共役した受容体に結合すると、多くのイオンが後者を通過します。 同じことがステロイドホルモン受容体にも当てはまります。1つのホルモン分子がmRNAの多くのコピーの転写を引き起こし、それに基づいて多数のタンパク質分子が合成されます。
構造と作用メカニズムに応じて、生物活性物質の受容体はいくつかのクラスに分類されます。 これらのクラスの数は少ないです。
酵素受容体
酵素活性を持つ受容体の最大のグループは、独自のプロテインキナーゼ活性を持つ膜受容体です。 細胞膜の内側にあるさまざまなエフェクタータンパク質をリン酸化します。 その結果、これらのタンパク質の機能または他のタンパク質との相互作用が変化します。
プロテインキナーゼ活性を持つ受容体には別のクラスがあります-これらはプロテインキナーゼと結合した受容体です。 それらは細胞内触媒ドメインを欠いているが、アゴニストと相互作用する場合、膜の内面の細胞内プロテインキナーゼに結合または活性化する。 これらは、神経栄養因子の受容体であり、いくつかのサブユニットからなるTおよびBリンパ球の抗原認識受容体です。 後者は、リン酸ホスホチロシンと相互作用します。 細胞内エフェクタードメインを持たない他の受容体の機能は、いくつかの他のエフェクタータンパク質によって媒介される場合があります。
独自の酵素活性を持つ他の受容体も同様の構造を持っています。 これらには、例えば、独自のホスホチロシンホスファターゼ活性を持つ受容体が含まれます。それらの細胞外ドメインは、アミノ酸配列が接着分子と類似しています。 独自のホスホチロシンホスファターゼ活性を持つ多くの受容体について、内因性リガンドは知られていない。 しかし、異なる種類の細胞で行われた遺伝的および生化学的研究によると、これらの受容体の酵素活性は重要な役割を果たしています。 心房性ナトリウム利尿ホルモン受容体、他のNUP、およびグアニリン受容体の細胞内ドメインは、それ自身のグアニル酸シクラーゼ活性を有し、2番目のメディエーターとして作用するcGMPを合成します。 おそらく、独自の酵素活性を持つ他の受容体があります。
イオンチャネル共役受容体
一部のメディエーターの受容体は、イオンチャネルに直接接続され、リガンドと相互作用して特定のイオンを選択的に細胞膜に通します(化学感受性チャネル、イオンチャネル型受容体チャネル、イオンチャネル型受容体)。
Gタンパク質共役受容体
これは、Gタンパク質(グアニン三リン酸(GTP)のグアニン二リン酸(GDF)の置換を使用するタンパク質)を介してエフェクターと相互作用するかなり大きなクラスの受容体です。 酵素(アデニル酸シクラーゼ、ホスホリパーゼC)およびカリウムおよびカルシウム膜チャネルはエフェクターとして作用し、Gタンパク質に結合した受容体の多数の重要な生理学的役割により優れています。 薬物の私の目標:医師が処方するすべての薬物の約半分(抗生物質を除く)は、これらの受容体に作用します。
細胞はその表面に最大20個の受容体を保持でき、それぞれが1つまたは複数のタイプのGタンパク質と選択的に相互作用します(異なるタイプのαサブユニットが異なります)。 αサブユニットは1つまたは複数のエフェクタータンパク質と相互作用することができ、1つのGタンパク質を使用して異なるリガンドの受容体からのシグナルを調整することができます。 一方、単一の受容体は、細胞内シグナル伝達のいくつかのメカニズムを誘発し、いくつかのタイプのGタンパク質を活性化し、同じαサブユニットを介して異なるエフェクタータンパク質に作用します。 信号の発散と収束のこのような複雑なシステムは、細胞機能の柔軟な調節を提供します(Ross、1992)。
細胞内受容体
ステロイドおよび甲状腺ホルモン、カルシトリオール、レチノイドの受容体は、特定の遺伝子の転写を制御する可溶性の細胞内DNA結合タンパク質です(Mangelsdorf et al。、1994)。 これらの受容体は、リガンド感受性転写調節因子のスーパーファミリーに属します。 転写因子の機能は、リン酸化、細胞タンパク質との相互作用、代謝産物および細胞の他の調節成分によって調節されています。
第二の仲介システム
cAMP:二次中間システムも外部信号の統合に関与しています。 第二のメディエーターよりもはるかに多くの既知の受容体とタンパク質シグナル伝達分子がありますが、後者は細胞シグナル伝達内の多くの経路に関与しています。 最も研究されている第2の中間体には、cAMP、cGMP、Ca 2+、IF 3(イノシトール三リン酸)、DAG(ジアシルグリセロール)、NOが含まれます。 異種化合物のこのグループは常に成長しています。 2番目のメディエーターは、直接相互作用(相互の代謝を変化させる)するか、間接的に(同じ細胞内標的に作用することにより)相互作用します。 第2メディエーターの機能、およびその形成(または放出)の調節、細胞からの切断および排泄は、cAMPの例で便利に考慮されます。 この2番目のメディエーターは、Gタンパク質と結合した多くの受容体の活性化におけるアデニル酸シターゼの影響下で合成されます。 G sタンパク質はアデニル酸シクラーゼを活性化し、G iタンパク質は阻害します。
活性の調節メカニズムが異なる組織特異的なアデニル酸シクロターゼアイソフォームが少なくとも10個あります。
原則として、cAMPは関連するタンパク質の小さなグループであるプロテインキナーゼA(cAMP依存性プロテインキナーゼ)を活性化します。 これらのプロテインキナーゼは、最終的な細胞内標的(酵素、輸送タンパク質)だけでなく、他のプロテインキナーゼおよび他の調節タンパク質もリン酸化します。 後者には、例えば、転写因子が含まれます。 それらは、遺伝子転写のcAMPを介した調節に関与し、シグナルに対する遅延細胞応答を提供します。 プロテインキナーゼの活性化に加えて、cAMPはカチオン膜チャネルに直接作用し、これは特にニューロンの機能において重要な役割を果たします。 したがって、cAMPからのシグナルは、標的細胞に一連の生化学的変化を引き起こします。
カルシウム 別のよく研究された第二のメディエーターは、細胞内Ca 2+です。 Ca 2+イオンは、さまざまな方法で細胞質に入ります:膜チャネルに沿って(Gタンパク質に依存し、電圧依存性、K +またはCa-Ca 2+によって調節)、および小胞体の特定の領域に位置し、作用下で開くチャネルを介して IF 3、および膜脱分極の結果としての骨格筋。 細胞質血漿からのカルシウムの除去は2つの方法で行われます。小胞体に吸収されるか、細胞から排出されます。 Ca 2+は、細胞の代謝に関与する酵素、プロテインキナーゼ、カルシウム結合タンパク質など、cAMPよりもはるかに多くのタンパク質にシグナルを伝達します。 後者は、他の最終および中間エフェクターと相互作用します。
受容体調節
受容体は生理学的および生化学的機能を制御するだけでなく、調節の対象としても機能します。 この調節は、他の分子との共有結合の形成、調節タンパク質との相互作用、および受容体の動きを通じて、高分子の合成および分解のレベルで実行されます。 タンパク質およびエフェクタータンパク質の変換も規制の対象です。 調節シグナルは、(フィードバックメカニズムを介して)受容体自体の刺激によって活性化される細胞内伝達経路から、および(直接または間接的に)他の受容体から来ることができます。
薬物受容体の長期刺激は、通常、それに対する反応の減少につながります-同じ濃度で、薬物はそれほど顕著な効果を引き起こしません。 脱感作、不応性、および嗜癖と呼ばれるこの現象は、臨床診療で重要な役割を果たします。たとえば、AD患者の治療にβ-アドレナリン作動薬を長期間使用すると、これらの薬物に対する反応の重症度が低下します。
相同的脱感作は刺激された受容体にのみ適用され、リガンドに特異的です。 異種脱感作では、受容体が同じ細胞内シグナル伝達経路を介して作用する他のリガンドに対する反応の重症度が低下します。 最初のケースでは、受容体自体への影響(リン酸化、タンパク質分解、合成の減少)によって負のフィードバックが提供され、2番目のケースでは、受容体に加えて、細胞内シグナル伝達に関与する他のタンパク質に影響を与える可能性があります。
反対に、受容体が長時間刺激されないと、アゴニストに対する感受性が高まります(たとえば、β-アドレナリン遮断薬プロプロノロールによる長期治療では、β-アドレナリン作動性受容体に対するβ-アドレナリン受容体の感受性が高まります)。
受容体機能障害による障害
薬物感受性の個人差に加えて、受容体からエフェクターへの細胞内シグナル伝達のメカニズムの特定のコンポーネントの機能不全によって引き起こされる疾患があります。 高度に特殊化された受容体の機能の喪失により、疾患の表現型の発現が制限される場合があります(たとえば、アンドロゲン受容体の遺伝的欠損または構造的欠陥に関連する精巣の女性化)。 細胞シグナル伝達内のより普遍的なメカニズムが侵害されると、例えば、重症筋無力症やインスリン抵抗性糖尿病のいくつかの形態など、N-コリン受容体とインスリン受容体の自己免疫機能不全によってそれぞれ引き起こされる疾患の症状は、より多様です。 多くの受容体からのシグナル伝達に関与するコンポーネントの欠陥は、複数の内分泌障害を引き起こします。 例は、すべての細胞でアデニル酸シクラーゼを活性化するG sタンパク質欠乏のヘテロ接合型です(Spiegel and Weinstein、1995)。 このタンパク質のホモ接合型の欠損は、死に至る可能性があります。
受容体の構造または局在の乱れは、薬物に対する反応の弱化または強化、およびその他の望ましくない効果として現れる可能性があります。
遺伝子受容体をコードする突然変異は、薬物の単回使用に対する反応と長期治療の有効性の両方を変えることができます。 たとえば、気管支の平滑筋の弛緩と気道抵抗の調節に関与するβアドレナリン受容体の欠損は、AD患者の長期治療中のβアドレナリン刺激薬に対するこれらの受容体の感受性の低下を悪化させます。 受容体機能障害の原因となる変異が特定され、対応する遺伝子がクローン化されると、そのような疾患を治療する方法を開発することが可能になります。
受容体分類
伝統的に、薬物受容体は、これらの受容体に作用する選択的アゴニスト(刺激剤)およびアンタゴニスト(遮断剤)の効果と相対活性に基づいて識別および分類されてきました。 たとえば、ムスカリンアルカロイドのコリン作動性受容体と相互作用するときに再現され、アトロピンによってブロックされるアセチルコリンの効果はムスカリン効果と呼ばれ、ニコチンのコリン作動性受容体と相互作用するときに再現される効果はニコチン効果と呼ばれます。 ムスカリンとニコチンの効果を媒介する受容体は、それぞれMおよびNコリン作動性受容体と呼ばれます。 このような分類は通常、薬物の作用メカニズムを反映していませんが、薬物の効果を体系化するのに便利です。 実際、薬物が特定のタイプの受容体を刺激するという主張は、同時にこの薬物とこれらの効果を強化または弱める物質の効果の範囲を決定します。 ただし、このような主張の有効性は、受容体の新しいタイプとサブタイプの識別、薬物の作用の追加メカニズムの発見、または以前は未知の副作用によって変わる可能性があります。
受容体サブタイプ
ますます多様化する高度に選択的な薬物の出現により、以前に知られているタイプの受容体は多くのサブタイプに分類されることが明らかになりました。 分子クローニング法は、新しい受容体サブタイプの研究において重要な助けとなり、組換え受容体の調製により、これらの受容体に選択的に作用する薬物の作成が容易になりました。 受容体の異なるが関連するサブタイプは、(常にではないが)しばしば異なるアゴニストおよびアンタゴニストと相互作用します。 選択的アゴニストまたはアンタゴニストが同定されていない受容体は、通常、単一のサブタイプに属しているのではなく、同じ受容体のアイソフォームに属します別々のサブタイプも細胞内シグナル伝達のメカニズムが異なります。 例えば、M 1およびM 3コリン作動性受容体は、ホスホリパーゼCを活性化するタンパク質G qを介して作用し、間接的に細胞内デポからCa 2+の放出を引き起こし、M 2およびM 4コリン作動性受容体は、タンパク質G iを介してアデニル酸シクラーゼを阻害します。 同時に、受容体のタイプとサブタイプへの分割は、多くの場合、作用メカニズムではなく、ランダムな選択によって決定されるか、確立されたアイデアに基づいています。 したがって、α1-、α2-、およびβ-アドレナリン受容体は、薬物に対する応答および信号伝達が異なります(それぞれタンパク質G i、G q、およびG sを活性化します)が、αおよびβ-アドレナリン受容体は異なるタイプのものですが、 およびα1-およびα2-アドレナリン受容体-同じタイプ内の異なるサブタイプに。 α1-アドレナリン受容体α1A、α1B、およびα1Dのアイソフォームは、その生化学的特性にほとんど違いはありません。 同じことが、β-アドレナリン受容体のイソホルメラーゼのサブタイプ(β1、β2およびβ3)に特徴的です。
受容体サブタイプ間の違いは、細胞内シグナル伝達のメカニズムが異なる受容体サブタイプへの結合により、同じ組織に対して異なる効果を持つ薬物など、高度に選択的な薬物を作成するために使用されます。 さらに、薬物は、サブタイプの受容体を発現する特定の細胞または組織を選択的に標的とすることができます。 (特定の組織または特定の効果に関して)薬物の選択性が高いほど、その利点と望ましくない効果の比率はより有利になります。
分子遺伝学的手法を使用して、受容体の異なるアイソフォームだけでなく、新しい未知の受容体をコードする遺伝子も発見されました。 これらの受容体の多くはすでに1つまたは別の既知のクラスに割り当てられており、その機能は対応するリガンドを使用して研究されています。 ただし、一部の受容体のリガンドはまだ見つかっていません。
異なる遺伝子によってエンコードされた同じ受容体の多くのアイソフォームの発見により(特にアイソフォームが細胞内シグナル伝達のメカニズムに違いがなく、同じ内因性リガンドと相互作用する場合)、異なる細胞での受容体の発現を異なる身体のニーズに応じて独立して調節することができます 年齢期間。
非受容体媒介薬物作用
すべての薬物が高分子構造-受容体を介して作用するわけではありません。 一部の薬物は、通常、または1つまたは別の病的状態で体内に存在する小分子またはイオンと相互作用します。 したがって、制酸剤は胃の中の塩酸を中和します。 メスナ(腎臓によって急速に排泄され、フリーラジカルを中和する薬剤)は、いくつかの抗腫瘍薬の活性代謝物に結合し、尿路からの副作用の重症度を軽減します。 多くの生物学的に不活性な物質(例えば、マンニトール)は、体液の浸透圧を増加させ、したがって細胞外および細胞内液の分布を変えるのに十分な量で導入することができます。 これらの物質の助けを借りて、利尿を増やし、bccを増やし、脳浮腫をなくすことができます。 さらに、それらは下剤として使用されます。
一部の薬物は、細胞の構成要素に統合され、これらの構成要素を構成する物質と構造的に類似しているため、その機能を変化させることができます。 たとえば、プリンとピリミジンの類似体は核酸に挿入され、抗ウイルス剤および抗腫瘍剤として使用されます。
A.P. ヴィクトロフ「臨床薬理学」