21. 抗ヒスタミン剤:分類、作用機序、使用の適応症、禁忌および副作用。
抗ヒスタミン剤 -体内のヒスタミン受容体の競合的遮断を実行し、その効果の阻害につながる薬物のグループ。
2つのグループに分かれています :1)H2-ヒスタミン受容体遮断薬および2)H2-ヒスタミン受容体遮断薬。 H1受容体遮断薬 抗アレルギー作用があります。 これらには、ジフェンヒドラミン、ジプラジン、スープラスチン、タベギル、ジアゾリン、フェンカロールが含まれます。 それらはヒスタミンの競合的拮抗薬であり、その次の影響を排除します:平滑筋けいれん、低血圧、毛細血管透過性の増加、浮腫の発達、充血および皮膚のかゆみ。 胃腺の分泌は影響を受けません。
中枢神経系への影響により、抑うつ効果のある薬(ジフェンヒドラミン、ジプラジン、スープラスチン)と中枢神経系に影響を及ぼさない薬(ジアゾリン)を区別できます。 フェンカロールとタベギルは鎮静効果が弱いです。 ジフェンヒドラミン、複屈折およびスープラスチンは、鎮静効果と催眠効果があります。 それらは「夜間」薬と呼ばれます。 それらはまた、鎮痙作用および遮断作用を有し、ジフェンヒドラミンは神経節遮断作用であるため、血圧を下げることができる。 ジアゾリンは「日中」抗ヒスタミン薬と呼ばれています。
これらの薬 適用する 即時型のアレルギー反応を伴う。 アナフィラキシーショックでは、あまり効果がありません。 中枢神経系を抑制する薬は、不眠症、麻酔の増強、鎮痛薬、局所麻酔薬、妊婦の嘔吐、パーキンソニズム、舞踏病、前庭障害に処方できます。 PE: 口渇、眠気。 鎮静作用のある薬物は、運用業務、輸送業務などに携わる人には推奨されません。
へ ブロッカー H2-ヒスタミン受容体 関係する ラニチジン と シメチジン。 彼らは胃と十二指腸の病気に使用されます。 アレルギー性疾患では効果がありません
薬物, 邪魔 解放する ヒスタミン およびその他のアレルギー因子..これらには、クロモリンナトリウム(内在)、ケトチフェン(ザディット)、およびグルココルチコイド(ヒドロコルチゾン、プレドニゾロン、デキサメタゾンなど)が含まれます。 クロモリンナトリウムとケトチフェンは、マスト細胞膜を安定化させ、カルシウムの流入とマスト細胞の脱顆粒を阻害し、アナフィラキシーの遅効性物質であるヒスタミンとその他の要因の放出を減少させます。 気管支喘息、アレルギー性気管支炎、鼻炎、花粉症などに使用されます。
コルチコステロイドは代謝にさまざまな影響を及ぼします。 脱感作の抗アレルギー効果は、免疫形成の抑制、肥満細胞、好塩基球、好中球の脱顆粒、アナフィラキシー因子の放出の減少に関連しています(講義28を参照)。
アナフィラキシーの重篤な全身症状(特にアナフィラキシーショック、虚脱、喉頭浮腫、重度の気管支痙攣)を排除するために、必要に応じてアドレナリンとユーフィリンが使用されます-ストロファンチン、コルグルコン、ジゴキシン、プレドニゾロン、ヒドロコルチゾン、血漿置換液(ヘモデシス、レオポロムスリンスポロムセリン)。
遅延型アレルギー(自己免疫疾患)の治療には、免疫原性を阻害する薬剤や組織の損傷を軽減する薬剤が用いられます。 最初のグループには、グルココルチコイド、シクロスポリン、細胞増殖抑制剤が含まれます。 免疫抑制剤。 MDグルココルチコイドは、Tリンパ球の増殖の阻害、抗原の「認識」のプロセス、キラーTリンパ球(「キラー」)の毒性の減少、およびマクロファージ遊走の促進に関連しています。 細胞増殖抑制剤(アザチオプリンなど)は、主に免疫応答の増殖期を抑制します。 シクロスポリンは抗生物質です。 MDは、インターロイキンの形成とTリンパ球の増殖の阻害に関連しています。 細胞増殖抑制剤とは異なり、造血への影響はほとんどありませんが、腎毒性と肝毒性があります。 免疫抑制剤は、臓器や組織の移植、および自己免疫疾患(エリテマトーデス、非特異的リウマチ様多発性関節炎など)における組織の不適合性を克服するために使用されます。
組織の損傷を減らす薬に 無菌性アレルギー性炎症の病巣が発生した場合は、ステロイド系(グルココルチコイド)および非ステロイド系抗炎症薬(サリチル酸、オルソフェン、イブプロフェン、ナプロキセン、インドメタシンなど)が含まれます。
抗ヒスタミン剤には3つの世代があります:
1.第1世代の抗ヒスタミン薬 (ジフェンヒドラミン、スプラスチン、タベギル、ジアゾリンなど)が治療に使用されています アレルギー反応 大人と子供:じんま疹、 アトピー性皮膚炎 湿疹、かゆみを伴う皮膚、アレルギー性鼻炎、 アナフィラキシーショック 、クインケ浮腫など。それらはすぐに効果を発揮しますが、すぐに体から排泄されるため、1日3〜4回まで処方されます。
2. 2世代の抗ヒスタミン剤 (エリウス、ジルテック、クラリチン、テルファストなど)神経系を阻害せず、眠気を引き起こしません。 薬物はじんましんの治療に使用され、 アレルギー性鼻炎、皮膚のかゆみ、気管支喘息など。第二世代の抗ヒスタミン剤は、より長い効果を持っているため、1日1〜2回処方されます。
3. 3世代の抗ヒスタミン剤 (テルフェナジン、アステミゾール)は、原則として、アレルギー性疾患の長期治療に使用されます:気管支喘息、アトピー性皮膚炎、通年性アレルギー性鼻炎など。これらの薬物は、最も長期間持続する効果があり、体内で数日間遅延します。
禁忌:
過敏症、閉塞隅角緑内障、前立腺過形成、胃および十二指腸の狭窄性消化性潰瘍、膀胱頸部の狭窄、てんかん。 注意して。 気管支喘息。
副作用:
眠気、口渇、口腔粘膜のしびれ、めまい、振戦、吐き気、頭痛、無力症、精神運動反応の低下率、光線過敏症、調節不全麻痺、運動の協調障害。
ヒスタミンの病態生理学とH 1ヒスタミン受容体
H 1受容体を介したヒスタミンとその効果
ヒトのH 1受容体の刺激は、平滑筋の緊張、血管透過性、かゆみの出現、房室伝導の遅延、頻脈、気道を支配する迷走神経枝の活性化、cGMPのレベルの増加、プロスタグランジンの形成の増加などにつながります。 テーブルの中。 19-1ローカリゼーションを表示 H 1受容体とそれらを介してヒスタミンの効果。
表19-1。ローカリゼーション H 1受容体とそれらを介したヒスタミンの効果
アレルギーの病因におけるヒスタミンの役割
ヒスタミンはアトピー症候群の発症において主導的な役割を果たしています。 IgEを介したアレルギー反応では、大量のヒスタミンがマスト細胞から組織に侵入し、H 1受容体への曝露を通じて次のような影響を引き起こします。
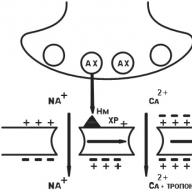
大きな血管、気管支、腸の平滑筋では、H 1受容体の活性化によりGpタンパク質の構造が変化し、次にホスホリパーゼCが活性化され、イノシトール二リン酸からイノシトール三リン酸およびジアシルグリセロールへの加水分解を触媒します。 イノシトール三リン酸の濃度の増加は、EPR(「カルシウム貯蔵所」)のカルシウムチャネルの開放につながり、細胞質へのカルシウムの放出と細胞内のその濃度の増加を引き起こします。 これはミオシン軽鎖のカルシウム/カルモジュリン依存性キナーゼの活性化につながり、したがって平滑筋細胞の減少につながります。 実験では、ヒスタミンは気管の平滑筋の二相性収縮を引き起こします。これは、急速な相収縮とゆっくりとした緊張成分から構成されます。 実験では、これらの平滑筋の収縮の早い段階は細胞内カルシウムに依存し、遅い段階はカルシウム拮抗薬によってブロックされない遅いカルシウムチャネルを介した細胞外カルシウムの流入に依存することが示されました。 H 1受容体を介して作用するヒスタミンは、気管支を含む気道の平滑筋の減少を引き起こします。 上気道では、ヒスタミンH 1受容体が下部よりも多く存在します。これは、ヒスタミンとこれらの受容体との相互作用中の細気管支における気管支痙攣の重症度に重要です。 ヒスタミンは結果として気管支の閉塞を誘発します 直接的な影響 ヒスタミンH 1受容体と反応し、気道の平滑筋に。 さらに、H 1受容体を介して、ヒスタミンは気道内の液体と電解質の分泌を増加させ、粘液産生と気道の浮腫の増加を引き起こします。 気管支喘息の患者は、ヒスタミン誘発試験を実施すると、健康な人よりもヒスタミンに対して100倍敏感です。
小さな血管の内皮(毛細血管後の細静脈)では、ヒスタミンの血管拡張作用は、(アデニル酸シクラーゼ経路を介した、細静脈の平滑筋細胞のH 2受容体を介した)レージン型のアレルギー反応におけるH 1受容体を介して行われます。 H 1受容体の活性化は、(ホスホリパーゼ経路に沿った)カルシウムの細胞内レベルの増加をもたらし、ジアシルグリセロールと一緒に、ホスホリパーゼA 2を活性化して、以下の効果を引き起こします。
内皮弛緩因子の局所放出。 それは隣接する平滑筋細胞に浸透し、グアニル酸シクラーゼを活性化します。 その結果、cGMPを活性化するcGMP依存性プロテインキナーゼの濃度が増加し、細胞内カルシウムの減少につながります。 カルシウムレベルの低下とcGMPレベルの増加が同時に起こると、毛細血管後細静脈の平滑筋細胞が弛緩し、浮腫や紅斑が発生します。
ホスホリパーゼA2が活性化されると、主にプロスタサイクリン血管拡張剤であるプロスタグランジンの合成が増加し、これも浮腫や紅斑の形成に寄与します。
抗ヒスタミン薬の分類
抗ヒスタミン薬(ヒスタミンH 1受容体遮断薬)にはいくつかの分類がありますが、一般的には認められていません。 最も人気のある分類によると、 抗ヒスタミン剤 作成時に、I世代とII世代の薬物に分けられます。 第2世代の非鎮静薬とは対照的に、私世代の薬は(主な副作用により)鎮静薬とも呼ばれます。 第1世代の抗ヒスタミン剤には、ジフェンヒドラミン(ジフェンヒドラミン*)、プロメタジン(ジプラジン*、ピポルフェン*)、クレマスチン、クロロピラミン(スプラスチン*)、キフェナジン(フェンカロール*)、セキフェナジン(ビカルフェン*)が含まれます。 II世代の抗ヒスタミン剤:テルフェナジン*、アステミゾール*、セチリジン、ロラタジン、エバスチン、シプロヘプタジン、オキサトマイド* 9、アゼラスチン、アクリバスチン、メブヒドロリン、ジメチンデン。
現在、抗ヒスタミン剤のIII世代を分離するのが通例です。 これには根本的に新しい薬物が含まれます-活性な代謝物は、高い抗ヒスタミン活性、鎮静作用の欠如、第二世代の薬物に特徴的な心毒性作用に加えて特徴付けられます。 フェキソフェナジン(telfast *)、デスロラタジンは、抗ヒスタミン薬の第3世代と呼ばれています。
さらに、抗ヒスタミン剤の化学構造はいくつかのグループ(エタノールアミン、エチレンジアミン、アルキルアミン、アルファカルボリンの誘導体、キヌクリジン、フェノチアジン*、ピペラジン*およびピペリジン*)に分類されます。
作用機序と抗ヒスタミン剤の主な薬力学的効果
使用されるほとんどの抗ヒスタミン薬は、別のグループとしてそれらを特徴付ける特定の薬理学的特性を持っています。 これらには、以下の効果が含まれます:かゆみ止め、充血緩和、鎮痙、抗コリン作用、抗セロトニン、鎮静および局所麻酔、ならびにヒスタミン誘発性気管支痙攣の予防。
抗ヒスタミン薬はヒスタミンH 1受容体の拮抗薬であり、これらの受容体に対する親和性はヒスタミンよりも著しく低い(表19-2)。 そのため、これらの薬物は受容体に関連するヒスタミンを置換することができず、空いている受容体または放出された受容体のみを遮断します。
表19-2。遮断の程度による抗ヒスタミン剤の有効性の比較 H 1ヒスタミン受容体
 したがって、ブロッカー H 1ヒスタミン受容体は、即時型のアレルギー反応の防止に最も効果的であり、反応が進行した場合、ヒスタミンの新しい部分の放出が防止されます。 受容体への抗ヒスタミン剤の結合は可逆的であり、ブロックされた受容体の数は、受容体の位置での薬物の濃度に正比例します。
したがって、ブロッカー H 1ヒスタミン受容体は、即時型のアレルギー反応の防止に最も効果的であり、反応が進行した場合、ヒスタミンの新しい部分の放出が防止されます。 受容体への抗ヒスタミン剤の結合は可逆的であり、ブロックされた受容体の数は、受容体の位置での薬物の濃度に正比例します。
抗ヒスタミン剤の作用の分子メカニズムは、スキームの形で表すことができます。H1受容体の遮断-細胞内のホスホイノシチド経路の遮断-ヒスタミンの効果の遮断。 ヒスタミンH 1受容体への薬物の結合は、受容体の遮断、すなわち ヒスタミンの受容体への結合とホスホイノシチド経路に沿った細胞内のカスケードの開始を妨害します。 したがって、抗ヒスタミン薬が受容体に結合すると、ホスホリパーゼCの活性化が遅くなり、ホスファチジルイノシトールからのイノシトール三リン酸とジアシルグリセロールの形成が減少し、その結果、細胞内蓄積からのカルシウム放出が遅くなります。 さまざまな種類の細胞で細胞内小器官から細胞質へのカルシウムの放出が減少すると、これらの細胞でヒスタミンの作用を媒介する活性化酵素の割合が減少します。 気管支の平滑筋(および消化管と大血管)では、ミオシン軽鎖のカルシウムカルモジュリン依存性キナーゼの活性化が遅くなります。 これにより、特に喘息の患者では、ヒスタミンによる平滑筋収縮が防止されます。 しかしながら、気管支喘息では、肺組織中のヒスタミンの濃度が非常に高いため、現代のN 1遮断薬はこのメカニズムによって気管支に対するヒスタミンの影響を遮断することができません。 すべての毛細血管後細静脈の内皮細胞において、抗ヒスタミン剤は局所および全身性アレルギー反応におけるヒスタミン(直接およびプロスタグランジン経由)の血管拡張作用を阻害します(ヒスタミンは平滑筋細胞のヒスタミンH 2受容体を介しても作用します)
アデニル酸シクラーゼ経路に沿った細静脈)。 これらの細胞でのヒスタミンH 1受容体の遮断は、細胞内カルシウムレベルの増加を防ぎ、最終的にホスホリパーゼA2の活性化を遅くします。これにより、次の効果が発現します。
隣接する平滑筋細胞に浸透してグアニル酸シクラーゼを活性化する内皮弛緩因子の局所放出を遅くします。 グアニル酸シクラーゼの活性化を阻害すると、cGMPの濃度が低下し、活性化されたcGMP依存性プロテインキナーゼの割合が減少し、カルシウムレベルの低下を防ぎます。 同時に、カルシウムとcGMPの正常化は、毛細血管後細静脈の平滑筋細胞の弛緩を防ぎます。つまり、ヒスタミンによって引き起こされる浮腫と紅斑の発生を防ぎます。
ホスホリパーゼA2の活性化画分を減らし、プロスタグランジン(主にプロスタサイクリン)の合成を減らすと、血管拡張が阻止され、これらの細胞に対する2番目の作用機序によってヒスタミンによって引き起こされる浮腫と紅斑の発生を防ぎます。
抗ヒスタミン剤の作用機序に基づいて、これらの薬物は、レギン型のアレルギー反応を防ぐために処方されるべきです。 発症したアレルギー反応を伴うこれらの薬物の指定は、それらが発症したアレルギーの症状を排除しないが、それらの出現を妨げるので、あまり効果的ではありません。 ヒスタミンH 1受容体遮断薬は、気管支の平滑筋のヒスタミンへの反応を防ぎ、かゆみを減らし、ヒスタミンによって媒介される小血管とその透過性の拡大を防ぎます。
抗ヒスタミン薬の薬物動態
第1世代のヒスタミンH 1受容体遮断薬の薬物動態は、第2世代の薬物の薬物動態とは根本的に異なります(表19-3)。
第一世代の抗ヒスタミン剤がBBBを通過すると、顕著な鎮静効果が現れます。これは、このグループの薬物の重大な欠点と見なされ、使用が著しく制限されます。
II世代の抗ヒスタミン剤は、相対的な親水性を特徴とするため、BBBに浸透せず、鎮静効果を引き起こしません。 *アステミゾールの80%は最後の投与の14日後に排泄され、テルフェナジンは*-12日後に排泄されます。
生理学的pH値でのジフェンヒドラミンの顕著なイオン化および血清との活発な非特異的相互作用
経口アルブミンは、さまざまな組織にあるヒスタミンH 1受容体への影響を決定します。これは、この薬の非常に顕著な副作用につながります。 血漿では、薬物の最大濃度は投与後4時間で決定され、75〜90 ng / lに相当します(50 mgの用量で)。 消失半減期は7時間です。
クレマスチンのピーク濃度は、2 mgの単回経口投与の3〜5時間後に達成されます。 排泄半減期は4-6時間です。
テルフェナジン*は摂取により急速に吸収されます。 肝臓で代謝される。 組織内の最大濃度は、薬を服用してから0.5〜1時間後に決定され、半減期は
変化のないアステミゾールの最大レベル*は、服用後1〜4時間以内に記録されます。 食品はアステミゾール*吸収を60%減らします。 単回経口投与による血中薬物のピーク濃度は1時間後に発生します。薬物の半減期は104時間です。ヒドロキシアステミゾールとノルアステミゾールがその活性代謝物です。 アステミゾール*は胎盤を通過し、少量で母乳になります。
血中のオキサトマイド*の最大濃度は、投与後2〜4時間で測定されます。 消失半減期は32〜48時間で、主な代謝経路は芳香族ヒドロキシル化と窒素での酸化的脱アルキル化です。 吸収された薬物の76%は血漿アルブミンに付着し、5〜15%は母乳に排泄されます。
表19-3。いくつかの抗ヒスタミン薬の薬物動態パラメータ
 血中のセチリジンの最大レベル(0.3μg/ ml)は、この薬剤を10 mgの用量で摂取してから30〜60分後に決定されます。 腎臓
血中のセチリジンの最大レベル(0.3μg/ ml)は、この薬剤を10 mgの用量で摂取してから30〜60分後に決定されます。 腎臓
セチリジンのクリアランスは30 mg /分、半減期は約9時間で、血液タンパク質に安定的に結合します。
血漿中のアクリバスチンのピーク濃度は、投与後1.4〜2時間に達します。 半減期は1.5〜1.7時間で、薬物の3分の2は変化せずに腎臓から排泄されます。
ロラタジンは消化管によく吸収され、15分後に血漿で測定されます。 食物は薬物の吸収の程度に影響を与えません。 薬物の半減期は24時間です。
第一世代抗ヒスタミン薬
ヒスタミンI世代のH 1受容体遮断薬には、いくつかの特徴があります。
鎮静作用。第1世代のほとんどの抗ヒスタミン薬は、脂質に溶けやすく、BBBをよく通過して脳のH 1受容体に結合します。 どうやら、鎮静効果は中枢のセロトニンとm-コリン作動性受容体の遮断により発生します。 鎮静効果の発現の程度は中程度から重度に変化し、アルコールや向精神薬と組み合わせると増強されます。 このグループのいくつかの薬は睡眠薬(ドキシラミン)として使用されます。 まれに、鎮静の代わりに精神運動性興奮が発生します(多くの場合、子供では中程度の治療量で、成人では高毒性量で)。 薬の鎮静作用があるため、注意が必要な作業期間中は使用できません。 ヒスタミンI生成のH 1受容体のすべての遮断薬は、鎮静薬および催眠薬、麻薬性および非麻薬性鎮痛薬、モノアミン酸化酵素阻害薬、アルコールの効果を増強します。
抗不安作用ヒドロキシジンに固有。 この効果は、おそらく、ヒドロキシジンによる脳の皮質下層の特定の部分の活動の抑制が原因で発生します。
アトロピンのような作用。この効果は、エタノールアミンとエチレンジアミンに最も特徴的なm-コリン作動性受容体の遮断に関連しています。 口渇、尿閉、便秘、頻脈、視覚障害が特徴的です。 非アレルギー性鼻炎では、m-コリン作動性受容体の遮断により、これらの薬の効果が高まります。 しかしながら、気管支喘息にとって危険な痰の粘度の増加により、気管支閉塞を増加させる可能性があります。 ジェネレーションIヒスタミンH 1受容体遮断薬は、緑内障を悪化させ、前立腺腺腫の急性尿閉を引き起こす可能性があります。
制吐剤と抗ポンプ作用。これらの効果は、これらの薬物の中枢m-抗コリン作用にも関連している可能性があります。 ジフェンヒドラミン、プロメタジン、シクリジン*、メクリ-
zine *前庭受容体の刺激を減らし、迷路の機能を阻害するため、乗り物酔いに使用できます。
一部のヒスタミンH 1受容体遮断薬は、中枢m-コリン作動性受容体の遮断によるパーキンソニズムの症状を軽減します。
鎮咳効果。ジフェンヒドラミンの最も特徴的なものは、延髄の咳の中心に直接作用するためです。
抗セロトニン作用。シプロヘプタジンが最も多く、片頭痛に使用されます。
末梢血管拡張を伴う1-アドレナリン受容体の遮断の効果は、フェノチアジン製剤に特に特徴的です。 これにより、血圧が一時的に低下することがあります。
局所麻酔薬この作用は、このグループのほとんどの薬物に特徴的です。 ジフェンヒドラミンとプロメタジンの局所麻酔の効果は、ノボカインの効果よりも強力です*。
タキフィラキシー-長期間使用すると抗ヒスタミン効果が低下し、2〜3週間ごとに薬剤を交換する必要があることが確認されます。
ヒスタミンI世代のH 1ブロッカーの薬力学
ヒスタミンI世代IのH 1受容体のすべての遮断薬は親油性であり、ヒスタミンのH 1受容体に加えて、m-コリン作動性受容体とセロトニン受容体も遮断します。
ヒスタミン受容体遮断薬を処方するときは、アレルギー過程の段階的経過を考慮する必要があります。 ヒスタミン受容体のヒスタミンH 1ブロッカーは、主に患者がアレルゲンと会うことが予想される場合の病原性変化の予防に使用する必要があります。
第一世代のヒスタミンH 1受容体遮断薬はヒスタミン合成に影響を与えません。 高濃度では、これらの薬物はマスト細胞の脱顆粒を引き起こし、ヒスタミンが放出されます。 ヒスタミンH 1受容体遮断薬は、ヒスタミンの作用を防止する上で、その作用の影響を排除するよりも効果的です。 これらの薬物は、ヒスタミンに対する気管支の平滑筋の反応を阻害し、かゆみを軽減し、血管ヒスタミンの拡大の増加を防ぎ、それらの透過性を増加させ、内分泌腺の分泌を減少させます。 ヒスタミンI世代のH 1受容体の遮断薬は直接気管支拡張作用を有することが証明されており、最も重要なことには、これらの薬の使用の基礎と考えられている肥満細胞および好塩基球からのヒスタミンの放出を妨げます
予防薬として。 治療用量では、それらは心血管系に大きな影響を与えません。 強制静脈内投与では、血圧の低下を引き起こす可能性があります。
ヒスタミンI生成のH 1受容体の遮断薬は、アレルギー性鼻炎(効率約80%)、結膜炎、掻痒症、皮膚炎およびじんま疹、血管性浮腫、ある種の湿疹、アナフィラキシーショック、低体温によって引き起こされる浮腫の予防と治療に効果的です。 第一世代のヒスタミンH 1受容体遮断薬は、アレルギー性鼻漏において交感神経刺激薬と組み合わせて使用\u200b\u200bされます。 ピペラジン*とフェノチアジン*の誘導体は、メニエール病、麻酔後の嘔吐、放射線病、妊娠中の女性の朝の嘔吐を伴う、突然の動きによる吐き気、嘔吐、めまいを防ぐために使用されます。
これらの薬物の局所適用は、それらの鎮痒効果、麻酔効果および鎮痛効果を考慮に入れています。 それらの多くは過敏症を引き起こす可能性があり、光線感作効果を持っているので、それらを長期間使用することは推奨されません。
第1世代のヒスタミンI遮断薬の薬物動態
ヒスタミンI世代のH 1受容体の遮断薬は、作用の持続時間が比較的短く、臨床効果の発現が比較的速い第二世代薬とは異なります。 これらの薬の効果は、平均して薬を服用してから30分後に発生し、1〜2時間以内にピークに達します。第1世代の抗ヒスタミン薬の作用期間は4〜12時間です。第1世代の抗ヒスタミン薬の臨床効果の短い期間は、まず第一に、速い 腎臓による代謝と排泄。
第一世代のヒスタミンH 1受容体遮断薬のほとんどは、消化管によく吸収されます。 これらの薬は、BBB、胎盤に浸透し、母乳にも浸透します。 これらの薬物の最高濃度は、肺、肝臓、脳、腎臓、脾臓、筋肉に見られます。
ヒスタミンI生成のH 1受容体のほとんどの遮断薬は、肝臓で70〜90%代謝されます。 それらはミクロソーム酵素を誘発し、長期の使用によりそれらの治療効果ならびに他の薬物の効果を低下させる可能性がある。 多くの抗ヒスタミン薬の代謝物は、24時間以内に尿とともに排泄され、変化はほとんどありません。
副作用と禁忌
ヒスタミンI世代のH 1受容体の遮断薬によって引き起こされる副作用を表に示します。 19-4。
表19-4。第一世代の抗ヒスタミン剤の望ましくない薬物反応
 大量のヒスタミンH 1受容体遮断薬は、特に子供の場合、興奮と発作を引き起こす可能性があります。 これらの症状では、バルビツール酸塩は使用できません。これは、呼吸中枢の相加効果と有意な抑制を引き起こすためです。 シクリジン*とクロロシクリシン*は催奇形作用があるため、妊婦の嘔吐には使用できません。
大量のヒスタミンH 1受容体遮断薬は、特に子供の場合、興奮と発作を引き起こす可能性があります。 これらの症状では、バルビツール酸塩は使用できません。これは、呼吸中枢の相加効果と有意な抑制を引き起こすためです。 シクリジン*とクロロシクリシン*は催奇形作用があるため、妊婦の嘔吐には使用できません。
薬物相互作用
第一世代のヒスタミンH 1受容体遮断薬は、麻薬性鎮痛薬、エタノール、睡眠薬、鎮静剤の効果を増強します。 子供のCNSの興奮剤の行為を高めるよろしいです。 長期使用すると、これらの薬物はステロイド、抗凝固剤、フェニルブタゾン(ブタジオン*)、および肝臓で代謝されるその他の薬物の効果を低下させます。 それらを抗コリン作用薬と組み合わせて使用\u200b\u200bすると、その効果が過度に増加する可能性があります。 MAO阻害剤は抗ヒスタミン剤の効果を高めます。 一部の第1世代の薬物は、心血管系に対するアドレナリンとノルエピネフリンの効果を増強します。 ヒスタミンI世代のH 1受容体の遮断薬は、アナフィラキシーショックを和らげるために、アレルギーの臨床症状、特にアトピー性気管支喘息を伴うことが多い鼻炎の予防のために処方されています。
抗ヒスタミン剤 薬 IIおよびIII世代
第2世代の薬物には、テルフェナジン*、アステミゾール*、セチリジン、メクビパジン*、フェキソフェナジン、ロラタジン、エバスチン、および第3世代のヒスタミンH 1受容体遮断薬-フェキソフェナジン(telfast *)が含まれます。
ヒスタミンIIおよびIII世代のH 1受容体遮断薬の以下の特徴を区別できます。
セロトニンおよびm-コリン作動性受容体に影響を与えない、ヒスタミンH 1受容体に対する高い特異性と高い親和性。
臨床効果と作用期間の急速な発現。これは通常、高度なタンパク質結合、体内での薬物またはその代謝産物の蓄積、排泄の遅延によって達成されます。
薬物を治療用量で使用する場合の鎮静作用は最小限です。 一部の患者は中程度の眠気を経験する場合があり、これはめったに薬物離脱の原因ではありません。
長期使用によるタキフィラキシーの欠如;
間隔の延長に関連する心臓の伝導系の細胞のカリウムチャネルを遮断する能力 Q-Tそして、心臓のリズムの違反(ピルエット型の心室頻拍)。
テーブルの中。 19-5は、ヒスタミンII世代のH 1受容体のいくつかの遮断薬の比較特性を示す。
表19-5。H 1受容体ヒスタミンII生成阻害剤の比較特性
 テーブルの終わり。 19-5
テーブルの終わり。 19-5
 ヒスタミンII世代のH受容体の遮断薬の薬力学
ヒスタミンII世代のH受容体の遮断薬の薬力学
アステミゾール*およびテルフェナジン*には、コリンおよびβ遮断活性はありません。 アステミゾール*は、α-アドレノおよびセロトニン受容体を大量に投与した場合にのみ遮断されます。 遺伝子IIヒスタミンH 1受容体遮断薬は、ヒスタミンだけでなく、ロイコトリエン、血小板活性化因子、サイトカイン、および疾患の発症を引き起こす他のメディエーターも気管支および気管支の平滑筋に影響を与えるため、気管支喘息の治療効果は弱いです。 ヒスタミンH 1受容体遮断薬のみの使用は、アレルギー性の気管支痙攣の完全な軽減を保証するものではありません。
ヒスタミンII世代のH 1受容体遮断薬の薬物動態すべてのII世代のヒスタミンH 1受容体遮断薬は長時間(24〜48時間)作用し、効果の発現にかかる時間は短く、30〜60分です。 アステミゾールの約80%*は最終投与の14日後に排泄され、テルフェナジン*-12日後に排泄されます。 これらの薬物の累積効果は、中枢神経系の機能を変化させることなく進行するため、花粉症、じんま疹、鼻炎、神経皮膚炎などの患者の外来診療で広く使用することができます。 II世代のヒスタミンH 1受容体遮断薬は、気管支喘息患者の個別の用量選択による治療に使用されます。
第二世代のヒスタミンのH 1受容体の遮断薬では、ブロックによる心毒性効果
心筋細胞のカリウムチャネルと間隔を長くすることによって表されます Q-T心電図上の不整脈。
この副作用のリスクは、抗ヒスタミン薬とチトクロームP-450 3A4アイソエンザイムの阻害剤(付録1.3)の組み合わせで増加します:抗真菌薬(ケトコナゾールとイントラコナゾール*)、マクロライド(エリスロマイシン、オレアンドマイシンとクラリスロマイシン)、抗デプレッシン-フェロミトキシンとエリスロキセチン-トロメトリン-メトリン-メトリン-メトリン 、グレープフルーツジュースの使用、および重度の肝機能障害のある患者に。 上記のマクロライドとアステミゾール*およびテルフェナジン*を10%のケースで組み合わせて使用\u200b\u200bすると、間隔の延長に伴う心毒性効果が生じます。 Q-T。アジスロマイシンとジリスロマイシン*は、3A4アイソザイムを阻害しないマクロライドであるため、間隔の延長を引き起こしません Q-Tブロッカーで第二世代のヒスタミンH 1受容体を服用している間。
(P. Creticos、1993)。
初代 -末梢および中枢のH 1ヒスタミン受容体に作用し、鎮静効果を引き起こし、追加の抗アレルギー効果はありません。
- バミピン( ソベントル軟膏)
- ディメティンデン( フェニスティル)
- ジフェンヒドラミン( ジミメドロール, ベナドリル)
- クレマスチン( タベギル)
- メブヒドロリン( ジアゾリン、オメリル)
- オキサトミド( ティンセット)
- プロメタジン( ピポルフェン, ジプラジン)
- フェニラミン( アビル)
- チフェナジン( フェンカロール)
- クロロピラミン( スプラスチン)
抗セロトニン作用
- ディメボン( ディメボーン)
- セタスティン( ロデリックス)
- シプロヘプタジン( ペリトール)
二代目 - ヒスタミン受容体に作用し、マスト細胞膜を安定させます。
- ケトチフェン( ザディテン など)
第三世代 -末梢H 1ヒスタミン受容体のみに作用し、鎮静効果を引き起こさず、マスト細胞膜を安定させ、追加の抗アレルギー効果を発揮します。
- アクリバスチン( センプレクス)
- アステミゾール( Hismanal、Histalong、Astemisan、Astelong)
- テルフェナジン( トレキシル, テリジン, トフリン)
- フェキソフェナジン( テルファスト)
- ロラタジン( クラリチン)
- セチリジン( ジルテック)
- エバスチン( ケスティン)
- アセラスチン( アレルゴジル)
- レボカバスチン( Histimet)
表2。 現代の抗ヒスタミン薬の特徴.
表3。 抗ヒスタミン剤の選択基準
1.追加の抗アレルギー効果を持つ薬剤を選択する可能性:
- 通年のアレルギー性鼻炎;
- 季節性増悪期間が2週間を超える季節性アレルギー性鼻炎(結膜炎)。
- 慢性じんましん;
- アトピー性皮膚炎;
- アレルギー性接触皮膚炎;
- 子供の早期アトピー症候群。
2.患者に特定の問題がある:
- 12歳未満の子供:
- ロラタジン( クラリチン)
- セチリジン( ジルテック)
- テルフェナジン( トレキシル)
- アステミゾール( ヒスマナル)
- ディメティンデン( フェニスティル)
- 早期アトピー症候群の1〜4歳の子供:
- セチリジン( ジルテック)
- ロラタジン( クラリチン)
- 妊娠中の女性:
- ロラタジン( クラリチン)
- フェキソフェナジン( テルファスト)
- アステミゾール( ヒスマナル)
- 授乳中の女性:
- クレマスチン( タベギル)
- フェニラミン( アビル)
- 腎不全患者:
- ロラタジン( クラリチン)
- アステミゾール( ヒスマナル)
- テルフェナジン( トレキシル)
- 肝機能障害のある患者:
- ロラタジン( クラリチン)
- セチリジン( ザイトレック)
- フェキソフェナジン( テルファスト)
・抗ヒスタミン剤
- ...歴史的に、「抗ヒスタミン」という用語はH1ヒスタミン受容体を遮断する薬物を意味し、H2ヒスタミン受容体に作用し、抗分泌薬として使用される薬物(シメチジン、ラニチジン、ファモチジンなど)はH2と呼ばれます。 -ヒスタミン遮断薬。
1942年に、最初のN受容体拮抗薬が作成され、 薬。 この期間から、幅広い医療行為における抗ヒスタミン剤の大量使用の時代が始まりました。
古典的なN受容体拮抗薬(または第一世代薬) エタノールアミン、フェノチアジン、エチレンジアミン、アルキルアミン、ピペラジン、ピペリジンに由来する化合物の6つのグループで主に表されます。 同時に、これらの薬物の最大数十が世界の医薬品市場に存在していました。
この状況は、第一世代のH受容体拮抗薬のいくつかの一般的な特別な特性によって引き起こされました。 それらのうち最も重要なものは、次のように要約できます。 これらの治療用量の薬物はH受容体に比較的弱く結合し、競合するヒスタミン拮抗薬であるため、それらの作用の比較的短期的な効果と、日中の反復治療用量の使用の必要性を説明します。
第1世代の薬物は作用の選択性が非常に高くないため、治療用量では、他のメディエーター(M-コリン作動性受容体、5HT受容体、α-アドレナリン受容体、D-受容体)の受容体を遮断する可能性があります。 副作用 (心臓血管系、消化管、視覚、粘膜など)。 血液脳関門を通過し、鎮静効果があり、食欲を刺激するこれらの薬物の中心的な効果はよく知られています。 第1世代の薬剤の非常に重要な望ましくない特性は、タキフィラキシー、つまり長期間(7〜10日以上)使用すると抗ヒスタミン作用が低下することです。 そのため、長期の治療中に1つの薬物を別の薬物に置き換えることができるようにするために、医薬品市場に多数のH受容体拮抗薬が存在する必要がありました。
言及された第1世代H受容体拮抗薬の望ましくない特性にもかかわらず、これらの薬物はまだ広く使用されており、場合によっては高度な医学的理由でも使用されます。 臨床的および薬理学的経験の蓄積により、特定の臨床状況では、通常の条件下では望ましくない特性(鎮静効果、他のタイプの受容体を遮断する能力、作用の持続時間の短さ)を、線量分割率を使用できる場合に治療目的で使用できることがわかりました。 第一世代のH受容体の拮抗薬の間違いない利点は多様性です 剤形、注射を含む。 さらに、最新の世代の薬と比較してこれらの薬のコストが比較的低いだけでなく、巨大な医療経験を考慮せざるを得ません。
第一世代抗ヒスタミン薬:ジフェンヒドラミン(ジフェンヒドラミン、ベナドリル、アレルゲン)、クレマスチン(タベギル)、ドキシラミン(デカプリン、ドナーミル)、ジフェニルピラリン、ブロモジフェンヒドラミン、ジメンヒドリナート(デダロン、ドラミン)、クロロピラミン(フェンタミン)、フェンアンタミン、フェンアンタミン、アミンアンテアミン、アンテフェンアミン、アンテフェンアミン フェニラミン(アビル)、メブヒドロリン(ジアゾリン)、キフェナジン(フェンカロール)、セキフェナジン(ビカルフェン)、プロメタジン(フェネルガン、ジプラジン、ピポルフェン)、トリメプラジン(テラレン)、オキセマジン、アリメマジン、シクリジン、ヒドロキシジン(アチジン) シプロヘプタジン(ペリトール)。
以下の薬理学的特性は、第1世代の抗ヒスタミン剤(鎮静剤)に最も特徴的です。
鎮静作用、第1世代のほとんどの抗ヒスタミン剤は脂質に容易に溶解し、血液脳関門をよく通過して脳のH1受容体に結合するという事実によって決定されます。 おそらくそれらの鎮静効果は、中央のセロトニンとアセチルコリン受容体を遮断することからなるでしょう。 第1世代の鎮静効果の発現の程度は、薬物や患者によって中程度から重度に異なり、アルコールや向精神薬と組み合わせると増加します。 それらのいくつかは睡眠薬(ドキシラミン)として使用されます。 まれに、鎮静の代わりに精神運動性興奮が発生します(多くの場合、子供では中程度の治療量で、成人では高毒性量で)。 鎮静効果があるため、注意が必要な仕事ではほとんどの薬を使用できません。 すべての第一世代薬は、鎮静薬と催眠薬、麻薬および非麻薬性鎮痛薬、モノアミンオキシダーゼ阻害剤、アルコールの効果を増強します。
抗不安作用ヒドロキシジンの特徴は、中枢神経系の皮質下領域の特定の領域での活動の抑制が原因である可能性があります。
アトロピンのような反応薬物の抗コリン作用に関連するものは、エタノールアミンとエチレンジアミンに最も特徴的です。 口渇および鼻咽頭、尿閉、便秘、頻脈および視覚障害を伴う。 これらの特性は、非アレルギー性鼻炎のための議論された薬の有効性を提供します。 同時に、それらは(痰の粘性の増加により)気管支喘息の閉塞を増加させ、緑内障の悪化を引き起こし、前立腺腺腫の膀胱下閉塞を引き起こす可能性があります。
制吐効果と咳止め効果またおそらく薬物の中枢抗コリン作用と関連している。 一部の抗ヒスタミン薬(ジフェンヒドラミン、プロメタジン、シクリジン、メクリジン)は、前庭受容体の刺激を減らし、迷路の機能を阻害するため、運動疾患に使用できます。
多くのH1ヒスタミン遮断薬がパーキンソニズムの症状を軽減しますアセチルコリンの効果の中心的な抑制による。
鎮咳効果ジフェンヒドラミンの最も特徴的なものは、延髄の咳の中心に直接作用するためです。
抗セロトニン効果主にシプロヘプタジンに特徴的な、片頭痛におけるその使用を決定します。
α1ブロッキング効果特に抗ヒスタミンフェノチアジンシリーズに固有の末梢血管拡張を伴うと、敏感な個人の血圧が一時的に低下する可能性があります。
局所麻酔(コカインのような)作用ほとんどの抗ヒスタミン剤の特徴(ナトリウムイオンに対する膜の透過性の低下が原因で発生)。 ジフェンヒドラミンとプロメタジンは、ノボカインよりも強力な局所麻酔薬です。 しかしながら、それらは、不応期の延長および心室頻拍の発生により明らかにされる全身性キニジン様効果を有する。
タキフィラキシー:長期間使用すると抗ヒスタミン活性が低下し、2〜3週間ごとに薬剤を変更する必要があることを確認します。
注意すべき第1世代の抗ヒスタミン剤は、第2世代とは曝露期間が短く、臨床効果が比較的迅速に発現すること。 それらの多くは非経口形態で入手可能です。H受容体の不均一性が60年代後半に確立された後、新しい抗ヒスタミン剤を作成するための戦略が変更されました。 アレルギーの外部症状は、第1のタイプの受容体に対するヒスタミンの作用によって媒介されることが判明しました。 現在、これらの受容体の4種類が知られるようになりましたが、アレルギー反応の外部症状は、1番目の種類の受容体(H1受容体)に対するヒスタミンの作用の結果であることは明らかです。 したがって、タスクは、他の受容体の遮断と他の望ましくない特性、特に鎮静と頻尿の喪失がない状態で、H1受容体の選択性の高い遮断薬を作成することでした。
70年代後半に、偶然に上記の要件を満たす化合物(テルフェナジン)が見つかりました。 その後、そのような特性を持つ化合物のリストには、当時アステミゾール、ロラタジン、シテリシン、エバスチンを含む第2世代のH1受容体拮抗薬のグループを構成する新しい薬剤が補充されました。 テルフェナジンとアステミゾールは、心血管系に対する既知の望ましくない副作用のために、現在医薬品市場を去っています。
異なるタイプの化合物に属する第2世代の薬物のすべての代表は、第1世代の薬物よりも優れていることを示す類似の特性を共有しています。 第2世代の薬物はH1受容体に対して高い親和性を持ち、それらのほとんどは非競合的遮断薬です。 後者のプロパティについては、簡単な説明が必要です。 H1受容体の選択的結合のために封鎖が競争力がないという仮説は合理的であるように思われますが、ヒスタミンへの結合に関与する活動中枢の領域ではなく、他の領域ではそうです。 したがって、ヒスタミンは、結合状態で長期間保持される受容体に結合した拮抗薬に取って代わることができず、メディエーター(ヒスタミン)と相互作用して細胞へのシグナル伝達に必要な受容体の構造を妨げます。
だから、第二世代の薬は特徴的です H1受容体に対する高い親和性。 H1受容体との拮抗薬の結合力は、その作用の持続時間を保証し、したがって、日中の薬物の単回投与の可能性を保証します。 正確にH1受容体を遮断する選択性が高いため、治療用量の第2世代の薬剤は他のメディエーターの受容体を遮断せず、したがって、第1世代のH1受容体の拮抗薬に特徴的な望ましくない副作用はありません。 第二世代薬の物理化学的性質は、血液脳関門を通過するそれらの浸透を事実上排除または大幅に低減し、それによって鎮静を含む中枢効果を排除することができます。 多くの研究でプラセボ群よりもわずかに高い割合で鎮静効果を示したセチリジンでさえ、この効果はセチリジンの前駆体であるヒドロキシジンよりも比類なく顕著ではありません。 最後に、これらの薬の大部分はタキフィラキシーを示さない、つまり、他の抗ヒスタミン薬と置き換えることなく、患者が長期間使用することができます。 また、これらの薬物はより広い臨床的適応に使用できます:慢性アレルギー状態で拮抗薬を変更することなく、気管支喘息で、H1受容体拮抗薬の指定が必要な症状と組み合わせます。 最後に、第2世代のH1受容体の拮抗薬の作成により、特に重要である、注意を必要とする活動に従事する人々による抗ヒスタミン剤の使用の可能性が開かれました。
第1世代の薬のいくつかの特性は、第2世代の薬に近い。 したがって、たとえば、アクリバスチンの使用は1日3回の分割使用であり、H1受容体のかなり高度に選択的なブロッカーであり、部分的にしか代謝されず、鎮静効果を示すことはほとんどありません。 国内の研究者(M.D. Mashkovsky、M.E。Kaminka)によって作成された元のクラスの抗ヒスタミン薬は、キヌクリジン誘導体です。 このグループの有名な薬物であるフェンカロール(チフェナジン)も、H1受容体に対する親和性が高く、鎮静作用が低く、安全性が良好な第2世代の薬物に似ています。 H1受容体に対する拮抗作用に加えて、それはジアミノキシダーゼ(ヒスタミナーゼ)の活性を増加させ、したがって、アレルギー反応中に放出されるヒスタミンの破壊による追加の抗アレルギー作用があります。
II世代の抗ヒスタミン薬:アクリバスチン(センプレクス)、アステミゾール(ギスマナール)、ジメチンデン(フェニチル)、オキサトマイド(ティンセット)、テルフェナジン(ブロナル、ヒスタジン)、アゼラスチン(アレルゴジル)、レボカバスチン(ヒスチメット)、ミソラスチン、ロラタジン(クラリチン)、エピネン バスチン(ケスチン)、バミピン(ソベントル)。
II世代の最も一般的な抗ヒスタミン剤(非鎮静剤)は、次の特性です。:
H1受容体に対する高い特異性と高い親和性コリンおよびセロトニン受容体への影響がない場合。
臨床効果の迅速な発現 と行動の期間。 タンパク質結合が高いこと、体内での薬物とその代謝産物の蓄積、排泄の遅延により、延長が達成されます。
最小限の鎮静薬物を治療用量で使用する場合。 これは、これらの薬剤の構造的特徴による血液脳関門の弱い通過によって説明されます。 特に敏感な人の中には、薬物の中止の原因となることの少ない中程度の眠気を経験する人もいます。
タキフィラキシーの欠如長期使用で。
心筋のカリウムチャネルを遮断する能力これは、QT間隔の延長と心臓のリズム障害に関連しています。 この副作用のリスクは、抗ヒスタミン薬と抗真菌薬(ケトコナゾールおよびイントラコナゾール)、マクロライド薬(エリスロマイシンとクラリスロマイシン)、抗うつ薬(フルオキセチン、セルトラリン、パロキセチン)の組み合わせ、グレープフルーツジュースの使用、および重度の肝機能を持つ患者で増加します。
非経口形態の欠如ただし、それらのいくつか(アゼラスチン、レボカバスチン、バミピン)は、 局所適用.III世代の抗ヒスタミン薬(代謝物)。 H1受容体の拮抗薬を改善するためのさらなる方法は、残念ながら、否定的な状況によって促されました。 実際のところ、このシリーズのほとんどの薬物はプロドラッグでした。つまり、薬理学的に活性な代謝産物が最初の形態から体内で形成され、代謝効果があります。 最初の化合物が、その代謝産物とは異なり、望ましくない影響を与えた場合、体内でのその濃度が増加する条件の発生により、深刻な結果につながる可能性があります。 これはまさに、テルフェナジンとアステミゾールという薬で一度に起こったことです。 当時知られているH1受容体の拮抗薬のうち、セチリジンだけがプロドラッグではなく、実際の薬でした。 それはヒドロキシジンの第一世代の薬の最終的な薬理学的に活性な代謝産物です。 例としてセチリジンを使用すると、元の分子のわずかな代謝修飾により、質的に新しい薬理学的製剤を得ることができることが示されました。 同様のアプローチを使用して、テルフェナジンの最終的な薬理活性代謝物に基づいて作成された新しい抗ヒスタミン薬であるフェキソフェナジンを入手しました。 したがって、III世代の抗ヒスタミン薬の基本的な違いは、前世代の抗ヒスタミン薬の活性代謝物であることです。 それらの主な特徴は、QT間隔に影響を与えることができないことです。 現在、第三世代の製剤はセチリジンとフェキソフェナジンに代表されます。 これらの薬物は血液脳関門を通過しないため、作用しません 副作用 中枢神経系から。 さらに、現代の抗ヒスタミン剤には、いくつかの重要な追加の抗アレルギー効果があります:接着分子(ICAM-1)の発現を減らし、上皮細胞からの好酸球誘発のIL-8、GM-CSFおよびsICAM-1の分泌を抑制し、アレルゲン誘発の気管支痙攣の重症度を下げます。 気管支過敏症の現象を減らします。
III世代の抗ヒスタミン薬:セチリジン(zirtec)、フェキソフェナジン(telfast)。
このように、抗ヒスタミン剤は真に未開拓の可能性のある抗アレルギー剤です。 一方で、これらの化合物のH1受容体に対する親和性を高め、標的細胞の機能を阻害する能力を拡大および強化する研究努力を指示することで、より優れた安全性プロファイルを持つ薬物としてグルココルチコステロイドに取って代わることができる抗アレルギー性多機能薬物のアイデアを生産的に実現できるようになります。
L.A.教授 ゴリヤチキナ
RMAPO、モスクワ
60年間 抗ヒスタミン剤(AGP) 次のアレルギー性疾患の治療に使用されます:
- アレルギー性鼻炎(季節性および通年)
- アレルギー性結膜炎
- アレルギー性皮膚疾患(アトピー性皮膚炎、急性および慢性じんま疹、クインケ浮腫など)
- 虫刺されや刺されに対するアレルギー反応
- sITや他の人との合併症の防止。
新しく得られた抗ヒスタミン剤を、論理的に正当化されるよりも広く使用する試みは、ヒスタミン作動性症状の治療効果が非常に高い薬物でさえ信用を失います。
アレルギー性疾患、特に、アレルギー性鼻炎、アトピー性喘息、慢性特発性じんま疹、アトピー性皮膚炎は、ヒトで最も一般的な病的状態の一つです。 これらの疾患は通常、生命に脅威を与えるものではありませんが、それでもなお、患者の生活の質を著しく損なう可能性があります。 アレルギー性疾患にも同様の病因があり、実際、全身性アレルギー性炎症の局所的な症状と考えることができます。 ヒスタミンはアレルギー反応の主要なメディエーターの1つであるため、H 1ヒスタミン受容体の遮断薬は、アレルギー性疾患、特に鼻炎および慢性じんま疹の治療における選択の手段として残っています。