薬物動態
薬力学には、薬理作用、作用の局在化、作用メカニズムの概念が含まれます 薬用物質 (つまり、体内で薬物がどのように、どこで、どのように作用するかのアイデア)。 薬物の作用の種類の概念も薬力学に属します。
^ 2.1。 薬の作用、局在、および薬の作用メカニズム
薬理学的効果-薬によって引き起こされる身体の器官およびシステムの機能の変化。 薬物の薬理効果には、たとえば、心拍数の増加、血圧の低下、痛みの感度のしきい値の増加、体温の低下、睡眠時間の延長、妄想や幻覚の排除などがあります。 原則として、各物質は、それを特徴付けるいくつかの特定の薬理効果を引き起こします。 同時に、原薬のいくつかの薬理効果は有用です-これらの効果のおかげで、原薬は医療行為で使用されます(主効果)、および原薬によって引き起こされる他の効果は使用されず、さらに望ましくない(副作用)。
多くの物質について、体内でのそれらの主要な作用の場所は知られています-つまり アクションのローカライズ。 一部の物質は特定の脳構造に主に作用し(抗パーキンソン病薬、抗精神病薬)、主に心臓に作用する物質(強心配糖体)が知られています。
現代の教育方法のおかげで、全身および臓器だけでなく、細胞および分子レベルでの物質の作用の局在を決定することが可能です。 たとえば、強心配糖体は、心臓(臓器レベル)、心筋細胞(細胞レベル)、心筋細胞膜のNa +、K + -ATPase(分子レベル)に作用します。
同じ薬理効果がさまざまな方法で引き起こされる可能性があります。 そのため、血圧の低下、アンジオテンシンII(アンジオテンシン変換酵素阻害剤)の合成の低下、平滑筋細胞でのCa 2+の摂取の遮断(電位依存性カルシウムチャネル遮断薬)、または交感神経線維の末端からのノルエピネフリンメディエーターの放出の低下を引き起こす物質があります (同情)。 原薬が薬理効果を引き起こす方法は、原薬の作用メカニズムとして定義されています。
ほとんどの薬物の薬理効果は、特定の生化学的基質、いわゆる「標的」に対する作用によって引き起こされます。
薬物の主な「標的」には以下が含まれます。
受容体;
イオンチャンネル;
酵素;
輸送システム。
A.受容体の特性と種類。 受容体と酵素およびイオンチャネルとの相互作用
受容体は、機能的に活性な高分子またはそのフラグメント(主にタンパク質分子-リポタンパク質、糖タンパク質、核タンパク質など)です。 物質(リガンド)と受容体の相互作用では、一連の生化学反応が発生し、特定の薬理効果をもたらします。 受容体は内因性リガンド(神経伝達物質、ホルモン、他の内因性生物活性物質)のターゲットですが、薬物などの外因性生物活性物質と相互作用することもできます。 受容体は、特定の物質(特定の化学構造を持つ物質)とのみ相互作用します。 選択性の特性を持っているため、それらは呼ばれます 特定の受容体。
受容体は、細胞膜(膜受容体)または細胞内-細胞質内または核内(細胞内受容体)に配置できます。
細胞外および細胞内ドメインは、膜受容体で分離されています。 細胞外ドメインには、リガンド(受容体と相互作用する物質)の結合部位があります。
4種類の受容体が知られており、最初の3種類は膜受容体です。
^ 酵素に直接結合した受容体。 これらの受容体の細胞内ドメインは酵素活性を示すため、酵素受容体または触媒受容体とも呼ばれます。 このグループのほとんどの受容体は、チロシンキナーゼ活性を持っています。 受容体が物質に結合すると、チロシンキナーゼが活性化され、これが細胞内タンパク質をリン酸化し(チロシン残基に応じて)、したがってその活性を変化させます。 これらの受容体には、インスリン、特定の成長因子、およびサイトカインの受容体が含まれます。 グアニル酸シクラーゼに直接関連する受容体が知られています(心房性ナトリウム利尿因子がこれらの受容体に作用すると、グアニル酸シクラーゼが活性化され、細胞内のcGMPのレベルが上昇します)。
^ イオンチャネルに直接結合した受容体、 膜を貫通し、イオンチャネルを形成(周囲)するいくつかのサブユニットで構成されます。 物質が受容体の細胞外ドメインに結合すると、イオンチャネルが開き、その結果、さまざまなイオンに対する細胞膜の透過性が変化します。 そのような受容体には、H-コリン作動性受容体、GABA-A受容体、グリシン受容体、グルタミン酸受容体が含まれる。
GABA A受容体は塩素チャネルに直接結合しています。 受容体がガンマアミノ酪酸と相互作用すると、塩素チャネルが開き、C1〜イオンが細胞に入り、細胞膜の過分極を引き起こします(これにより、中枢神経系の抑制プロセスが増加します)。 グリシン受容体は同じように機能します。
^
3)と相互作用する受容体
G-タンパク質。これらの受容体は相互作用します
中間タンパク質を介した細胞の酵素およびイオンチャネルとの結合
gタンパク質と呼ばれる-GTP(CTP)結合タンパク質。 物質が作用するとき
gタンパク質αサブユニット受容体はGTPに結合します。 さらに、複雑なG
lock-GTPは、酵素またはイオンチャネルと相互作用します。 どうやって
原則として、1つの受容体はいくつかのGタンパク質に結合されており、各Gタンパク質
同時にいくつかの酵素分子と相互作用できる
またはいくつかのイオンチャネル。 この相互作用の結果は
効果の増幅(増幅)。
Gタンパク質とアデニル酸シクラーゼおよびホスホリパーゼCとの相互作用はよく研究されています。
アデニル酸シクラーゼは、ATPを加水分解する膜結合酵素です。 ATP加水分解の結果として、cAMPが形成され、細胞タンパク質をリン酸化するcAMP依存性プロテインキナーゼを活性化します。 この場合、タンパク質の活性とそれらによって調節されるプロセスが変化します。 アデニル酸シクラーゼの活性に対する効果に従って、Gタンパク質は、アデニリルシクラーゼを刺激するG sタンパク質とアデニル酸シクラーゼを阻害するGタンパク質に細分される。 Β1-アドレナリン受容体(交感神経支配の効果を媒介する)はG sタンパク質と相互作用する受容体の例であり、M 2-コリン作動性受容体(心臓の副交感神経支配の阻害効果を媒介する)はGjタンパク質と相互作用する受容体の例です。 これらの受容体は、心筋細胞の膜上にあります。
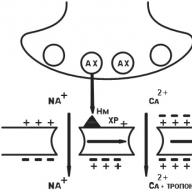
β1-アドレナリン受容体が刺激されると、アデニル酸シクラーゼ活性が増加し、心筋細胞のcAMPのレベルが増加します-その結果、プロテインキナーゼが活性化され、Ca 2+イオンが細胞に入る心筋細胞の膜のカルシウムチャネルをリン酸化します。 同時に、細胞へのCa 2+の摂取が増加し、これにより洞結節の自動化が増加し、心拍数が増加します。 心筋細胞のM 2コリン作動性受容体の刺激中に、反対の細胞内効果が発生します(洞結節および心拍数の自動化の低下)。
Gqタンパク質は、ホスホリパーゼCと相互作用します(この酵素を活性化します)。 Gqタンパク質と結合した受容体の例は、血管平滑筋細胞のα1アドレナリン受容体です(交感神経支配の血管への影響を媒介します)。 ホスホリパーゼCは、ホスファチジルイノシトール-4,5-二リン酸の\u200b\u200b細胞膜を加水分解して、細胞の筋小胞体のCa 2+チャンネルと相互作用する親水性物質イノシトール-1,4,5-三リン酸を形成します。 細胞質へのCa 2+放出。 平滑筋細胞の細胞質のCa 2+濃度が増加すると、Ca 2+-カルモジュリン複合体の形成速度が増加し、ミオシン軽鎖のキナーゼを活性化します(この酵素はミオシン軽鎖をリン酸化します)。 その結果、アクチンとミオシンの相互作用が促進され、血管平滑筋の収縮が起こります。
Mコリン作動性受容体とアドレナリン受容体に加えて、Gタンパク質と相互作用する受容体には、ドーパミン受容体、セロトニン受容体のサブタイプ、オピオイド受容体、ヒスタミン受容体などが含まれます。
^
4)DNA転写受容体、
細胞内にある
受容体。 これらの受容体は可溶性のサイトゾルまたは
核タンパク質。 細胞内受容体のリガンドは親油性物質です:ステロイドホルモン、ビタミンAおよびD。物質と細胞内受容体との相互作用の結果、多くの機能的に活性なタンパク質の合成が変化します(増加または減少)。
^ B.受容体への物質の結合。 親和性の概念
物質が受容体に作用するためには、物質が受容体に接触しなければなりません。 その結果、「物質受容体」複合体が形成されます。 複雑な「物質受容体」の形成は、分子間結合によるものです。 このような関係にはいくつかのタイプがあります。
共有結合は、分子間結合の中で最も耐久性のあるタイプです。 それらは、共通の電子対により2つの原子間で形成されます。 ほとんどの場合、共有結合は 不可逆的結合しかし、物質は、薬物と受容体の相互作用には典型的ではありません(例は、フェノキシベンザミンとα-アドレナリン受容体の不可逆的結合です)。
イオン結合-あまり強くない-異なる電荷を運ぶグループ間で発生します(静電相互作用)。
イオン-双極子および双極子-双極子結合は、本質的にイオン結合に似ています。 細胞膜の電界に入るか、またはイオンに囲まれている薬物の電気中性分子では、誘導双極子の形成が発生します。 イオン結合と双極子結合は、薬物と受容体の相互作用に特徴的です。
水素結合は、薬物と受容体の相互作用において非常に重要な役割を果たします。 水素原子は、酸素、窒素、硫黄、ハロゲンの原子と結合できます。 これらはやや弱い結合です;それらの形成のために、分子が互いに0.3nm以下の距離に位置することが必要です。
ファンデルワールス結合は、0.2 nm以下の距離にある場合、2つの原子間に形成される最も弱い結合です。 距離が長くなると、これらの結合は弱まります。
疎水性結合は、水性媒体中の非極性分子の相互作用によって形成されます。
この用語は、物質の受容体への結合を特徴付けるために使用されます。 親和性。
アフィニティ(lat。 アフルニス -関連)は、物質が受容体に結合し、「物質-受容体」複合体を形成する能力として定義されます。 さらに、親和性という用語は、物質の受容体への結合強度(すなわち、「物質-受容体」複合体の持続時間)を特徴付けるために使用されます。 親和性(物質の受容体への結合強度)の定量的尺度は 解離定数(K d)。
解離定数は、このシステムの受容体の半分が物質に関連付けられている物質の濃度に等しい。 モル/ l(M)で表されます。 親和性と解離定数の間には反比例の関係があります。Kdが低いほど親和性は高くなります。 たとえば、物質AのK \u003d 10 -3 M、物質BのK d \u003d 10 -10 Mの場合、物質Bの親和性は物質Aの親和性よりも高くなります。
^ B.薬物の内部活動。 受容体アゴニストおよびアンタゴニストの概念
親和性がある物質は 内部活動。
内部活動とは、受容体と相互作用するときに、物質を刺激して特定の効果を引き起こす物質の能力です。
内部活動の存在に応じて、原薬は次のように分類されます。 アゴニストそして 拮抗薬。
アゴニスト(ギリシャ語から アゴニスト -相手 アゴン -闘争)または 模倣物-親和性と内部活性を持つ物質。 特定の受容体と相互作用するとき、それらはそれらを刺激します。 受容体の立体構造の変化を引き起こし、一連の生化学反応を引き起こし、特定の薬理効果が発現します。
受容体と相互作用する完全なアゴニストは、可能な最大の効果を引き起こします(最大の内部活性があります)。
部分アゴニストは、受容体と相互作用する場合、最大値よりも小さい効果を引き起こします(最大の内部活性はありません)。
アンタゴニスト(ギリシャ語から 拮抗 - 競争 反-に対して アゴン -fighting)-親和性はあるが、内部活性はない物質。 それらは受容体に結合し、受容体に対する内因性アゴニスト(神経伝達物質、ホルモン)の作用を阻害します。 したがって、それらは受容体遮断薬とも呼ばれます。 拮抗薬の薬理効果は、これらの受容体の内因性作動薬の作用の除去または減少によるものです。 この場合、主にアゴニストの効果と反対の効果。 そのため、アセチルコリンは徐脈を引き起こし、Mコリン作動性受容体のアトロピン拮抗薬は、心臓に対するアセチルコリンの作用を排除し、心拍数を増加させます。
拮抗薬が作動薬と同じ受容体を占有している場合、それらは相互に受容体との通信を強制することができます。 このような拮抗作用は競合的拮抗薬と呼ばれ、拮抗薬は競合的拮抗薬と呼ばれます。 競合的な拮抗作用は、競合する物質の相対的な親和性とその濃度に依存します。 十分に高い濃度では、親和性の低い物質でさえ、受容体から親和性の高い物質に置き換わることがあります。 薬の毒性作用を排除するために、しばしば拮抗薬が使用されます。
部分アンタゴニストは、結合部位について完全アゴニストと競合する可能性もあります。 受容体への結合から完全なアゴニストを置き換えることにより、部分的アゴニストは完全なアゴニストの効果を低減するため、臨床現場でアンタゴニストの代わりに使用できます。 例えば、部分βアドレナリン作動薬(オクスプレノロール、ピンドロール)およびこれらの受容体の拮抗薬(プロプラノロール、アテノロール)は、高血圧の治療に使用されます。
拮抗薬が特定の受容体に関連していないが、相互作用している高分子の他の部分を占める場合、それらは非競合的拮抗薬と呼ばれます。
一部の薬物は、1つの受容体サブタイプを刺激し、別の受容体サブタイプをブロックする能力を組み合わせています。 そのような物質は
アンタゴニストアゴニスト。 そのため、麻薬性鎮痛薬ペンタゾシンはμ拮抗薬です -, およびδ-およびκ-オピオイド受容体のアゴニスト。
^ 薬物のその他の「ターゲット」
医薬物質は、イオンチャネル、酵素、輸送タンパク質など、他の「標的」に作用する可能性があります。
薬物の主な「標的」の1つは、電位依存性イオンチャネルです。これは、Na +、Ca 2 +、K +およびその他のイオンを細胞膜を通して選択的に伝導します。 物質が受容体と相互作用するときに開く受容体駆動型イオンチャネル(「受容体」セクションを参照)とは異なり、これらのチャネルは活動電位によって調節されます(細胞膜が脱分極すると開く)。 薬用物質は、電位依存性イオンチャネルをブロックし、細胞膜を通るこれらのチャネルを通るイオンの浸透を妨害するか、またはこれらのチャネルを活性化することができます。 それらの開放とイオン電流の通過を促進するため。 医療現場で広く使用されている多くの医薬品は、イオンチャネル遮断薬です。
局所麻酔薬は、電位依存性のNa + -Kaチャネルを遮断することが知られています。 Na +チャネルの遮断薬には、多くの抗不整脈薬(キニジン、リドカイン、プロカインアミド)が含まれます。 一部の抗てんかん薬(ジフェニン、カルバマゼピン)も電位依存性Na +チャネルをブロックし、その抗けいれん作用はこれに関連しています。 ナトリウムチャネルロケーターは、Na +イオンの細胞への侵入を妨害し、細胞膜の脱分極を防ぎます。
Ca 2+チャンネルのブロッカー(ニフェジピン、ベラパミルなど)は、多くの心血管疾患(高血圧、不整脈、狭心症)の治療に非常に効果的であることが判明しました。 Ca 2+イオンは、多くの生理学的プロセスに関与します。平滑筋の収縮、洞房結節でのインパルスの発生、房室結節の興奮、血小板凝集など。Ca2+チャネル遮断薬は、Ca 2+イオンの侵入を防ぎます 細胞は電位依存性チャネルを通過し、血管の平滑筋の弛緩、心臓の収縮頻度の低下、房室伝導を引き起こし、血小板凝集を破壊します。 一部のカルシウムチャネル遮断薬(ニモジピン、シンナリジン)は、主に脳の血管を拡張し、神経保護効果があります(ニューロンへの過剰なCa 2+の侵入を防ぎます)。
医薬物質の中には、電位依存性K +チャネルの活性化剤と遮断薬の両方があります。
K +チャネルの活性化剤(ミノキシジル、ジアゾキシド)は、降圧剤として使用されます。 それらは、K +チャネルの開口と細胞からのK +イオンの放出に寄与します。これは、細胞膜の過分極と血管平滑筋の緊張の低下につながります。 その結果、血圧が低下します。
電位依存性K +チャネルを遮断するいくつかの物質(アミノダロン、ソタロール)は、不整脈の治療に使用されます。 それらは心筋細胞からのK +の放出を防ぎ、その結果、活動電位の持続時間を延長し、効果的な不応期を延長します。
膵臓ベータ細\u200b\u200b胞のATP依存性K +チャネル(これらのチャネルはATPの影響下で開く)はインスリン分泌を調節します。 彼らのブロック
はい、インスリンの分泌増加につながります。 これらのチャネルのブロッカー(スルホニル尿素誘導体)は、抗糖尿病薬として使用されます。
多くの薬物は酵素阻害剤です。 モノアミン酸化酵素(MAO)阻害剤は、カテコールアミン(ノルエピネフリン、ドーパミン、セロトニン)の代謝(酸化的脱アミノ化)を破壊し、中枢神経系の内容を増加させます。 抗うつ薬の作用-MAO阻害薬(ニアラミド、ピラジドール)は、この原則に基づいています。 非ステロイド系抗炎症薬の作用機序はシクロオキシゲナーゼの阻害と関連しており、その結果、炎症誘発効果を持つプロスタグランジンE 2およびプロスタサイクリンの生合成が減少します。 アセチルコリンエステラーゼ阻害剤(抗コリンエステラーゼ剤)は、アセチルコリンの加水分解を阻害し、シナプス間隙におけるその含有量を増加させます。 これらの薬は、平滑筋器官(胃腸管、膀胱)と骨格筋の緊張を高めるために使用されます。
薬は、細胞膜を横切って特定の物質またはイオンの分子を移動させる輸送システム(輸送タンパク質)に作用することができます。 たとえば、三環系抗うつ薬は、非特異的シナプス前膜を介してノルエピネフリンとセロトニンを運ぶ輸送タンパク質をブロックします(ノルエピネフリンとセロトニンの逆ニューロン取り込みをブロックします)。 強心配糖体は、心筋細胞膜のNa +、K + -ATPaseをブロックし、心筋細胞はK +と引き換えにNa + H3細胞を輸送します。
薬物が作用する可能性のある他の「標的」があります。 そのため、制酸剤は胃の塩酸に作用して中和し、胃液の酸性度を高めるために使用されます(過酸胃炎、胃潰瘍)。
有望な「ターゲット」 薬 遺伝子です。 選択的に作用する薬物の助けを借りて、提供することが可能です 直接的な影響 特定の遺伝子の機能について。
^ 2.2。 薬の作用の種類
次のタイプのアクションが区別されます:ローカルおよび再吸収、反射、直接および間接、一次および二次、および他のいくつか。
薬は、適用部位の組織との接触時に局所的な効果を持ちます(通常は皮膚または粘膜です)。 例えば、表面麻酔では、局所麻酔薬は粘膜への適用部位でのみ感覚神経の末端に作用します。 局所作用を提供するために、薬用物質は軟膏、ローション、リンス、プラスターの形で処方されます。 特定の薬を点眼薬または点耳薬の形で処方する場合、それらは局所効果にも依存します。 ただし、一定量の原薬は通常、塗布場所から血液に吸収され、一般的な(吸収)効果があります。 局所的に適用すると、反射効果も可能です。
再吸収作用(lat。 レソルベオ -私は吸収します)-これらは、血液への吸収または血流への直接注射および体内での分布後に原薬が引き起こす効果です。 吸収作用により、局所物質と同様に、敏感な受容体を興奮させ、反射反応を引き起こすことができます。
反射アクション。 いくつかの薬用物質は、皮膚の敏感な神経、粘膜(外受容器)、血管化学受容器(インターレセプター)の末端を興奮させ、物質が敏感な受容体と直接接触する場所から離れた器官から反射反応を引き起こすことができます。 エッセンシャルマスタードオイルの作用下での皮膚の外部受容体の興奮の例は、呼吸器系の病理におけるマスタードの使用であり、その結果、栄養組織が反射します。 血管化学受容体は、ロベリンの作用により興奮し(静脈内投与)、呼吸中枢および血管運動中枢の反射刺激につながります。
心臓、血管、腸、およびその他の臓器に対する薬用物質の直接(一次)効果は、これらの臓器の細胞に直接影響を与えるときに発生します。 たとえば、強心配糖体は、心筋細胞に直接作用するため、強心作用(心筋収縮の増加)を引き起こします。 同時に、心不全患者の強心配糖体による利尿の増加は、心拍出量の増加と血行動態の改善によるものです。 薬用物質が他の臓器に作用することにより一部の臓器の機能を変化させるような行為は、間接的(二次的)効果と呼ばれます。
メインアクション。 この病気の治療に医薬品が使用されるアクション。 たとえば、フェニトイン(ジフェニン)には、抗けいれん作用と抗不整脈作用があります。 てんかんの患者では、フェニトインの主な効果は抗けいれん薬であり、強心配糖体の過剰摂取によって引き起こされる心不整脈の患者では、抗不整脈薬です。
治療用量で服用したときに発生する原薬の他のすべての効果(主要なものを除く)は、副作用の発現とみなされます。 これらの影響は、多くの場合、悪影響(負)です(第5章を参照)。 たとえば、アセチルサリチル酸は、胃粘膜の潰瘍、アミノグリコシドのグループからの抗生物質(カナマイシン、ゲンタマイシンなど)を引き起こす可能性があります-聴覚を損ないます。 負の副作用は、多くの場合、特定の医薬品の使用を制限したり、薬のリストから除外したりする理由です。
原薬の選択効果は、主に身体の1つの器官またはシステムに向けられます。 したがって、強心配糖体は、心筋、オキシトシン-子宮、催眠薬-中枢神経系に選択的な効果があります。
中枢神経系(脳および脊髄)に対する薬物の直接的な効果により、中枢作用が発生します。 中心的な作用は、血液脳関門を貫通する物質の特徴です。 睡眠薬、抗うつ薬、抗不安薬、麻酔薬、その他の薬の場合、中心的な効果が第一です。 同時に、中央のアクションはサイド(望ましくない)になります。 そのため、多くの抗ヒスタミン薬(抗アレルギー薬)は、その中枢作用により眠気を引き起こします。
末梢効果は、末梢神経系に対する薬物の影響、または臓器や組織に対する直接的な効果によるものです。 Cur状薬(末梢筋弛緩薬
チェスキーアクション)骨格筋を弛緩させ、神経筋シナプスの興奮の伝達をブロックします。一部の末梢血管拡張薬は血管を拡張し、平滑筋細胞に直接作用します。 主要な中枢作用を持つ物質の場合、末梢作用はほとんどの場合副作用です。 たとえば、抗精神病薬のクロルプロマジン(クロルプロマジン)は血管を拡張し、血圧の低下(望ましくない効果)を引き起こし、末梢のα-アドレナリン受容体を遮断します。
可逆効果は、原薬の「標的」(受容体、酵素)への可逆的結合の結果です。 そのような物質の作用は、別の化合物との結合からそれを移動させることにより終了させることができます。
不可逆的なアクションは、原則として、原薬の「ターゲット」への強い(共有)結合の結果として発生します。 たとえば、アセチルサリチル酸は血小板シクロオキシゲナーゼを不可逆的にブロックし、この酵素の機能は新しい細胞の形成後にのみ回復します。
第3章
^ 薬の薬力学および薬動力学に対するさまざまな要因の影響
薬物の効果に影響する要因には、物質の特性(化学構造、物理化学的特性、薬物の用量と濃度)、剤形とその技術の特徴、生物の個々の特性(性別)が含まれます 、年齢、遺伝的要因など)、および投与方法と医薬物質の使用条件(繰り返し投与、併用、時刻、環境の状態:季節、気温、気圧、e ologicheskaya条件、など)。
^ 3.1。 薬の性質
薬物の作用に影響を与える要因には、化学構造、物理化学的特性、薬物の用量および濃度が含まれます。
薬物の化学構造は、その作用の性質(薬理効果)と薬物動態の特徴を決定します。 原則として、化学構造が近い物質(ベンゾジアゼピン、バルビツール酸、ジヒドロピリジンなど、同じ化学グループの物質)は、同じ薬理作用を引き起こします。 これは主に、物質と「標的」との相互作用が、その化学構造、機能的に活性な基の存在、分子の空間的配向およびサイズによって決定されるという事実によるものです。 したがって、物質が受容体に作用するためには、適切な化学構造を持つだけでなく、この受容体に空間的に対応する必要があります。 彼にとっては無料だった
タルノ。 薬物の作用に対する相補性の効果の例は、分子が反対の空間配向を有する立体異性体の作用の違いです(それらは互いの鏡像です)。 L異性体であるヒオスシアミンは、活性L異性体と低活性D異性体の混合物であるアトロピンよりも2倍活性があります。 機能的に活性な物質のグループ間の距離も重要です。
現在までに、薬物の作用の化学構造への依存について十分な情報が蓄積されています。 この依存性を知って、特定の薬理学的特性を持つ医薬品を合成することが可能です。
薬物の薬物動態と薬力学は、物理化学的特性にも依存しています:親油性、親水性、極性、イオン化度。 したがって、物質の親油性は、血液脳関門を貫通し、中枢神経系に効果を及ぼす能力を決定します。
薬の効果(薬理効果の発現率、その重症度、持続時間、さらには性質)は用量に依存します。
線量(ギリシャ語から 線量
-部分)-一度に薬の量。 用量は、重量または体積単位で与えられます。 用量は、体重1 kgあたりまたは体表面1 m 2あたりの物質量として表すことができます(たとえば、1 mg / kg、1 mg / m 2)。 これにより、薬物をより正確に投与できます。 液体の薬には、大さじ、デザート、または小さじ1杯、およびドロップが投与されます。 特定の抗生物質およびホルモンの投与量は、作用単位で表されます(U)。
^ 図 3.1。 線量効果曲線。
A)緩やかな依存。 B)片対数依存。 ED 50
-半分の最大効果を引き起こす用量。 E ああ -最大効果の大きさ。
原薬の投与量が増加すると、その効果は増加し、特定の時間が経過すると最大(一定)値(E max)に達します。 したがって、算術線量スケールでは、線量効果依存性は双曲線特性(次数依存性)を持ちます。 対数線量スケールでは、この依存性はS字曲線で表されます(図3.1を参照)。 特定の値の効果を引き起こす用量の大きさにより、 活動物質。 通常、これらの目的のために、用量反応プロットでは、50%(最大の半分)の効果を決定する用量が決定され、ED 50(ED 50)として指定されます。 そのような用量の原薬は、その活性を比較するために使用されます。 ED 50値が低いほど、物質の活性は高くなります(物質AのED 50が物質BのED 50よりも10倍小さい場合、物質A
物質Bの10倍の活性。 活性に加えて、原薬は 有効性(最大効果の大きさ、E maxによって決定されます)。 物質Aの最大効果が物質Bの最大効果の2倍であれば、物質Aは物質Bの2倍の効果があります。
治療、毒性、致死量があります。
以下の治療用量が区別されます:最小有効用量、平均治療用量、およびより高い治療用量。
最小有効量(閾値)は、最小限の治療効果をもたらします。 通常、それらは平均治療用量の2〜3分の1です。
ほとんどの患者の平均治療用量には、必要な薬物療法効果があります。 一度に薬物の投与量を計算する-単回投与 (プロ ドシ), 患者が1日あたりに服用すべき用量-1日の用量 (プロ 死ぬ). 患者の個々の感受性と疾患の重症度は異なる可能性があるため、平均治療用量は通常、用量制限として表されます(たとえば、ジクロフェナクナトリウムの単回投与は0.025〜0.05 gです)。
通常、抗生物質、スルファニラミド、および特定の他の薬物を使用する場合、治療は平均治療用量を超える負荷用量の投与から始まります。 これは、血中に高濃度の物質を迅速に生成するために行われます。 特定の治療効果を達成した後、彼らは維持量に切り替えます。
で 長期使用 薬用物質は、治療コースごとの用量(コース用量)を示します。
中用量の使用が必要な効果をもたらさない場合には、より高い治療用量が処方される。 これらは、それを超えると有毒な線量の領域が位置する線量限度です(この物質は毒性作用を引き起こす可能性があります)。 有毒で強力な物質の場合、法律は最高の1日あたりの最高用量を定めています。 重度の副作用のリスクに関連付けられているため、より高い治療用量の薬剤の指定は、細心の注意を払って処理する必要があります。 医師が処方箋に特定の処方箋を持っている場合を除き、薬剤師は最高の1日1回投与量を超える薬剤を投与しないでください。
体に毒性のある用量は毒性と呼ばれます。 死を引き起こす用量は致死と呼ばれます(lat。 たわごと-死)。
最小作用薬から最高治療薬までの用量範囲は、 治療効果の幅。治療効果の幅が大きければ大きいほど、薬物の使用はより安全になります。
^ 剤形。 医薬品がさまざまな剤形に含まれる場合、その作用の性質を保存する必要があります。 しかし、剤形およびその製造の技術的プロセスは、活性物質の放出速度、吸収の場所および速度、したがって効果の発現速度およびその持続時間に影響を及ぼします。 さまざまな技術プロセスの助けを借りて、薬物の調整可能な放出速度を備えた既製の長時間作用型剤形を作成できます。 剤形には、形成物質だけでなく、不快な味を軽減するさまざまな添加剤も含まれています。
局所刺激効果など。したがって、医薬品の使用により最適な条件を作り出すために、製薬技術が使用されます。
薬物の物理化学的特性、剤形、および薬物の薬物動態および薬力学に対するそれらの調製プロセスの影響の研究は、生物薬局によって実施されています。
^ 3.2。 身体特性
薬物の効果に影響を与える要因には、性別、年齢、体重、体調、遺伝的特徴が含まれます。
ポール 薬物の薬理作用の性依存性の問題は十分に研究されていません。 動物実験と臨床観察は、薬物の代謝における特定の性差と特定の薬理効果に対する感受性を示しています。 そのため、男性の性ホルモンはミクロソームの肝臓酵素の合成を刺激するという事実により、特定の薬物(アセトアミノフェン、ベラパミル、ベンゾジアゼピン、プロプラノロール)の除去は男性でより早く起こります。 エタノール代謝における既存の性差は、男性アルコール脱水素酵素活性のより高いレベルと関連しています。 女性は男性よりも特定の薬物に敏感であるという臨床的証拠があります。 抗不整脈薬の不整脈誘発効果(「ピルエット」などの心室性不整脈)は女性でより頻繁に発生し、モルヒネの鎮痛効果(例えば術後の痛みを和らげる)は男性よりも低用量の女性に現れます。 中枢神経系を抑制する薬(モルヒネおよびバルビツール酸塩)は、女性では覚醒状態を引き起こすことがありますが、男性ではそのような効果はありません。
年齢。 年齢に関連する薬物の効果の変化は、特に極端な年齢層の人々、すなわち新生児と60歳以上の人々で顕著です。
小児の身体に対する物質の作用の特性を研究する薬理学の分野は、小児薬理学と呼ばれています。 新生児(生後4週間まで)および妊娠末期の胎児(周産期薬理学)に対する薬物の影響は、別に考慮されます。 生後1か月の新生児は、薬物に対する感受性が高くなっています。 物質の吸収、分布、代謝、排泄に関しては、成人とは大きく異なります。 これは主に、代謝プロセスの低強度(薬物を代謝する酵素の不足による)、腎機能の低下、血液脳関門の透過性の増加、および内分泌系、神経系および他の身体系の発達不足によるものです。 したがって、新生児にはクロラムフェニコール(クロラムフェニコール)の抱合に関与する酵素はなく、この薬剤の毒性効果を高めます。 新生児はモルヒネとネオスチグミンに対してより敏感です。 したがって、子供は大人よりも低用量で薬を処方されます(一部の薬はまったく処方されていません)。 子供の薬の投与量を減らすことはまた、彼らが大人よりも体重が少ないという事実によるものです。 毒と暴力を処方するとき
不活性な医薬品は、州薬局方に記載されている特別な表に基づいています。 これらの表は、さまざまな年齢の子供に対する薬物の投与量を示しています。 各薬剤は、特定の年齢に推奨される用量で使用する必要があります。
高齢者および老年期では、薬物動態プロセスはゆっくりと進行します。 吸収率の変化は、主に胃液の酸性度の低下、腸内の血流の減少、能動吸収システムの阻害などに関連しています。高齢者における薬物の分布は、血漿タンパク質への結合の変化と臓器および組織の血流の減少により変化します。 加齢に伴う薬物の代謝の低下は、肝臓酵素の活性の低下と肝血流の低下に関連しています。 腎機能の低下は、薬物の排泄の遅延につながります。 したがって、60歳以上の患者、中枢神経系を抑制する物質の用量(睡眠薬、モルヒネ群の薬物)、強心配糖体の用量、利尿薬は1/2、他の強力で毒性のある薬物の用量は推奨用量の2/3まで減らす必要があります 中年の人々のために。 老年薬理学は、高齢者および老人における薬物の作用および使用の特徴の研究に従事しています。
血漿中、臓器および組織中の薬物の濃度、したがって、ある程度の効果は体重に依存します。 原則として、体重の増加に伴い、医薬品の処方用量も増加するはずです。 したがって、必要に応じて、より正確な投与量、特定の物質の投与量は体重1 kgごとに計算されます。
体の状態。 さまざまな病理学的状態は、薬物の薬物動態および薬力学の変化を引き起こす可能性があります。 消化管の病気では、薬物の吸収速度と吸収度の低下が起こる可能性があります。 いくつかの肺疾患および心血管疾患は、血行動態に大きな変化をもたらし、薬物の分布の性質に影響します。
腎機能障害の場合、腎臓によって排泄される物質の作用が長くなります(たとえば、正常な腎機能の場合、アンピシリンの半除去期間(t] / 2)は1.3時間、腎不全の場合は13-20時間)、および肝疾患の場合 これは主に肝臓で代謝される物質で起こります。 この場合、注射を繰り返した後、体内に物質が蓄積(蓄積)する可能性があり、これにより、従来の投与レジメンでは毒性効果のリスクが高まります。
炎症の焦点では\u200b\u200b、局所麻酔薬の作用が急激に弱まり、化膿性創傷ではスルホンアミドの効果が低下します。
一部の医薬品は、病的状態でのみ作用します。 たとえば、強心配糖体の強心作用は心不全で現れ、アセチルサリチル酸は発熱を抑えます。
病理学的プロセスは、原則として、薬物に対する体の感受性と反応性を変化させます。 病気の体は、健康な人とは薬物に対する反応が異なります。 実験におけるこれらの現象の研究は、1920年代にN.P. Kravkov、その後MPを続けた ニコラエフとA.N. クドリン。 これは科学的な方向です。
病的状態における薬物の効果の研究は、病的薬理学と呼ばれます。 これは、実験的および臨床的薬物療法の科学的基盤です。
薬理反応は、身体の機能状態に依存します。 患者の身体の発達と栄養も重要です。 身体的に強い人々は、ほとんどの薬物の投与量を1.5〜2倍減らす必要がある衰弱した、消耗した、脱水した患者よりも薬物に反応しにくい。
妊娠中および授乳中の女性への薬物の処方には大きな注意が必要です。 ここでは、体の感受性の変化だけでなく、胎盤関門を通る薬剤物質の浸透の可能性、そのミルクによる排泄、および胎児と子供への有害な影響も考慮に入れる必要があります。
遺伝的要因。 薬物に対する人々の個々の感受性には大きな違いがあり、それは遺伝的要因によって決まります。 薬理学のセクションが登場しました-医薬品遺伝学、そのタスクは、薬物の作用を変える際の遺伝因子の役割を研究することです。 非常に多くの場合、薬物の作用の個人差は代謝の違いによるものです。 これは、主にこれらの酵素の合成を制御する遺伝子の突然変異に関連する、薬物を代謝する酵素の活性の変化のために起こります。 酵素の構造と機能の違反は、酵素障害(酵素障害)と呼ばれます。 エニモパシーでは、酵素活性を増加させることができます(この場合、薬物の代謝プロセスが加速されて効果が低下します)または減少します(この場合、薬物の代謝が遅くなり、その作用と毒性効果の出現につながります)。 一部の酵素の遺伝的欠損により、物質への非定型反応(特異性)が発生する可能性があります。 典型的な特異性は、赤血球中のグルコース-6-リン酸デヒドロゲナーゼの遺伝的欠損を伴ういくつかの抗マラリア薬(キニーネ、プリマキン、クロロキン)の溶血作用です。 この酵素の不足の結果として、赤血球溶血を引き起こす「イノン」が形成されます。
^ 3.3。 薬の宛先モード
薬物の効果は、反復投与と薬物の併用(併用、同時)の両方の影響を受けます。
^ A.薬物の再利用
同じ原薬を繰り返し注射すると、薬理効果の定量的(増加または減少)および定性的変化につながる可能性があります。
薬物の反復注射中に観察される現象の中で、累積、感作、嗜癖(耐性)および薬物依存が区別されます。
累積(緯度から 累積 - 増加、蓄積)-薬理学的に活性な物質の体内での蓄積またはそれが引き起こす効果。
薬剤の新しい投与ごとに、血液および/または組織の濃度が前の投与と比較して増加する場合、この現象は物質蓄積と呼ばれます。 ゆっくりと不活性化され、体からゆっくりと排泄される薬物は、繰り返し注射中に蓄積する可能性があります。また、血漿タンパク質または組織貯蔵部にしっかりと結合する薬物、例えばバルビツール酸系の睡眠薬、ジギタリス強心配糖体 これは毒性作用を引き起こす可能性があるため、そのような薬物は、蓄積する能力を考慮して投与する必要があります。
薬物の繰り返し注射中に、血液および/または組織内の物質の濃度を増加させることなく効果の増加が観察される場合、この現象は機能的蓄積と呼ばれます。 このタイプの蓄積は、アルコールの反復投与で発生します。 影響を受けやすい人にアルコール性精神病(せん妄)が発生すると、エチルアルコールがすでに代謝されて体内で検出されないときに妄想と幻覚が発生します。 ただし、中枢神経系機能の変化が増加します。 機能的蓄積もMAO阻害剤の特徴です。
感作。 多くの医薬品物質は、特定の条件下で抗原性を獲得する血漿タンパク質と複合体を形成します。 これには、抗体の形成と感作が伴います。 感作された生物への同じ薬用物質の繰り返し投与は、アレルギー反応によって現れます。 多くの場合、そのような反応は、ペニシリン、プロカイン、水溶性ビタミン、スルホンアミドなどを繰り返し注射すると起こります。
中毒(寛容、緯度から。 寛容 -忍耐)-同じ用量での薬物の繰り返し注射による薬理効果の減少。 中毒は、薬物の薬物動態の変化(吸収の低下、代謝率の増加および排泄)、ならびに受容体の感度の低下および/またはシナプス後膜上の密度の低下による可能性があります。 例えば、バルビツール酸塩への中毒は、バルビツール酸塩自体の影響下での酵素の誘導による代謝の強度の増加の結果である可能性があります。 薬物中毒は、数日から数ヶ月で発症する可能性があります。 中毒の場合、同じ薬理効果を得るためには、薬物の用量を増やす必要があり、それは副作用の増加につながる可能性があります。 したがって、彼らはしばしばこの物質の使用を中断し、必要に応じて、同様の効果を持つが異なる化学グループからの薬物による治療を続けます。 ある物質を別の物質に置き換える場合、その化学構造に関係なく、これらの物質が同じ基質(受容体や酵素など)と相互作用すると、相互馴化が発生する可能性があります
中毒の特別なケースはタキフィラキシーです(ギリシャ語から。 chy -速い 走化性 -保護)-短い間隔(10〜15分)で薬物を繰り返し注射することによる嗜癖の急速な発達。 エフェドリンへのタキフィラキシーはよく知られていますが、これは交感神経線維の末端にあるアドレナリンの枯渇によって引き起こされます。 エフェドリンの後続の各投与で、シナプス間隙に放出されるノルエピネフリンの量が減少し、2回目または3回目の注射後に薬物の高血圧効果(血圧の上昇)が減少します。
嗜癖の別の特定のケースはミトリダチズムです-薬物と毒の作用に対する無感覚性の漸進的な発達であり、最初は非常に小さく、その後は用量を増やして、薬物と毒の長期使用から生じます。 古代ギリシャの伝説によると、ミトリダテス王はこのように多くの毒に対する無感覚を獲得しました。
非常に心地よい感覚(陶酔感)を引き起こす特定の物質を繰り返し使用すると、素因のある人は薬物依存症になります。
薬物依存-特定の薬物物質または物質群の絶え間ない、または定期的な更新摂取の緊急の必要性(抵抗できない欲求)。
最初は、レセプションは多幸感の状態を達成し、痛みを伴う経験と感覚を排除し、幸福感と快適さを達成し、幻覚の発生中に新しい感覚を得るという目標に関連付けられています。 しかし、一定の時間が経過すると、繰り返し摂取する必要がなくなります。これは禁断症候群によって悪化します-この物質が停止すると深刻な状態が発生し、精神球の変化だけでなく、身体障害(臓器および身体系の機能障害)にも関連します。 この状態は「撤回」という用語で示されます(lat。 禁欲 - 禁欲)。
精神的および身体的薬物依存を区別します。
精神的薬物依存は、気分の急激な悪化と感情的な不快感、薬物を奪われている間の疲労感を特徴としています。 コカインおよび他の精神刺激薬(アンフェタミン)、幻覚剤(リセルグ酸ジエチルアミド-LSD-25)、ニコチン、インド麻(anasha、hashish、plan、marijuana)を使用すると発生します。
物理的な薬物依存は、感情的な不快感だけでなく、禁断症状の発生も特徴とします。
物理的な薬物依存は、オピオイド(ヘロイン、モルヒネ)、バルビツール酸塩、ベンゾジアゼピン、アルコール(エチルアルコール)に進行します。 、 で 薬物依存は中毒と組み合わされることが多く、幸福感を得るためにはますます多くの用量の物質が必要になります。 最も困難な薬物依存は、精神依存、身体依存、および依存症の組み合わせの場合に発生します。
麻薬の効果を得るための物質の使用は、薬物乱用と呼ばれます。
薬物中毒は、薬物が薬物として使用される場合の薬物乱用の特殊なケースであり、薬物依存を引き起こす物質(麻薬物質)のリストを参照し、管理の対象となります。
^ B.併用
および薬物相互作用
薬物の併用により、それらの効果は強化(相乗作用)または弱化(拮抗作用)する可能性があります。
相乗効果(ギリシャ語から syn - 一緒に エルグ -仕事)-2つ以上の薬用物質の一方向性効果、個別の各物質よりも顕著な薬理効果があります
メモ。 薬物の相乗作用は、効果の合計と増強の2つの形で現れます。
同等に作用する薬用物質の同時使用の効果が、組み合わせ内の個々の物質の効果の合計に等しい場合、そのようなアクションは合計または加算効果として定義されます。
同じ基質(受容体、細胞など)に影響を及ぼす薬物が体内に導入されると、合計が観察されます。 たとえば、末梢血管のαアドレナリン受容体に作用するノルエピネフリンとメソンの血管収縮作用と高血圧作用がまとめられています。 神経細胞に抑制効果がある吸入麻酔薬の効果をまとめています。
ある物質が別の物質の薬理効果を著しく高める場合、この相互作用は増強作用と呼ばれます。 増強されると、2つの物質の組み合わせの全体的な効果は、個々の物質の効果の合計を超えます。 たとえば、クロルプロマジン(抗精神病薬)は麻酔薬の効果を高め(増強し)、麻酔薬の濃度を低下させます。
医薬物質は、同じ基質に作用する場合があります(直接相乗作用)、または作用の局在が異なる場合があります(間接相乗作用)。
相乗効果の現象は、複数の薬をより少ない用量で処方するときに望ましい薬理効果を得ることができるため、医療現場でよく使用されます。 この場合、望ましくない副作用のリスクが減少します。
拮抗(ギリシャ語から 反 - に対して アゴン -闘争)-一緒に使用した場合、1つの原薬の薬理効果を別の原薬によって低減または完全に排除する。
拮抗作用の現象は、中毒の治療に使用され、望ましくない薬物反応を排除します。
以下のタイプの拮抗作用が区別されます。
直接的な機能的拮抗作用は、薬用物質が同じ機能的要素(受容体、酵素、輸送システムなど)に対して反対の(多方向の)効果を持つ場合に発生します。 例えば、機能的アンタゴニストは、β-アドレナリン受容体の刺激薬および遮断薬、M-コリン作動性受容体の刺激薬および遮断薬です。 直接的な敵対関係の特別な場合は 競争力のある拮抗。 薬用物質の化学構造が緊密であり、受容体との通信をめぐってそれらの間で競合がある場合に起こります。 したがって、ナロキソンはモルヒネおよび他の麻薬性鎮痛薬の競合的拮抗薬です。
一部の薬物は、微生物および腫瘍細胞の代謝産物と類似した化学構造を持ち、生化学プロセス(タンパク質合成)のリンクの1つに影響を与えるためにそれらと競合します。 それらは代謝拮抗薬と呼ばれます。 代謝拮抗剤は、生化学合成チェーンの要素の1つを置き換えると、微生物、腫瘍細胞の繁殖を妨害します。 たとえば、スルホンアミドは微生物細胞内のパラアミノ安息香酸の競合的拮抗薬であり、メトトレキサートは腫瘍細胞内の競合的ジヒドロ葉酸還元酵素拮抗薬です(対応するセクションを参照)。
間接的な機能的拮抗作用は、薬用物質が臓器の機能に反対の効果をもたらし、同時にその作用が異なるメカニズムによって実現される場合に発生します。 たとえば、アセクリジン(Mコリン作動性受容体の興奮により平滑筋器官の緊張を高める)およびパパベリン(直接的な筋刺激作用により平滑筋器官の緊張を低下させる)は、平滑筋器官に対する作用に対する間接的な拮抗薬です。
物理的拮抗作用は、薬物の物理的相互作用に起因します。ある薬物が別の薬物の表面に吸着し、不活性または吸収の悪い複合体が形成されます(たとえば、活性炭の表面に薬物と毒素が吸着します)。 物理的拮抗作用は、消化管に閉じ込められた毒素による中毒に使用されます。
化学的拮抗作用は、物質間の化学反応の結果として発生し、不活性化合物または不活性複合体の形成をもたらします。 このように作用する拮抗薬は解毒剤と呼ばれます。 たとえば、ヒ素、水銀、および鉛化合物による中毒の場合、化学反応の結果として、無毒性の亜硫酸塩が形成されるチオ硫酸ナトリウムが使用されます。 強心配糖体による過剰摂取または中毒の場合、ユニチオールが使用され、それはそれらと不活性な複合化合物を形成します。 ヘパリンの過剰摂取の場合、硫酸プロタミンが導入され、その陽イオン基はヘパリンの陰イオン中心に結合し、その抗凝固効果を中和します。
1つまたは複数の薬を処方するとき、それらの間に拮抗効果がないことを確認する必要があります。 同時使用は除外されます。 いくつかの薬物の同時投与(多剤併用)は、薬理効果の発現率、その重症度および期間の変化につながる可能性があります。 )(薬用物質を組み合わせて使用\u200b\u200bした結果、より顕著な治療効果を得ることができ、悪影響を軽減または防止できる場合、この組み合わせ 薬 合理的で治療的に適切です。 合理的な組み合わせにより、活性医薬物質の投与量を減らすことができ、その結果、望ましくない副作用が減少するか、現れません。
通常、薬物の組み合わせは、より顕著な薬理効果を生み出すように処方されます。
医薬品も組み合わせて、個々の成分の望ましくない影響を排除します。 たとえば、イソニアジドの神経毒性作用を防ぐために、ビタミンB 6が追加で処方されています。 カンジダ症の予防のため、広域抗生物質-ナイスタチンまたはレボリンの治療; 利尿薬の治療における低カリウム血症を防ぐために-塩化カリウム。
それどころか、いくつかの薬物の同時使用の結果が治療効果の弱体化、不在、ゆがみ、または望ましくない悪影響の出現である場合、そのような薬物の組み合わせは不合理で治療的に不適切と呼ばれます (薬物の非互換性)。
薬物の相互作用は、2つのグループに分類できます。
薬剤相互作用;
薬理学的相互作用。
薬物をさらに使用できなくなる薬物相互作用は、薬物不適合と呼ばれます。 この非適合性の理由は、薬物の不活性または毒性化合物の形成との化学的相互作用、薬物の溶解度の低下、コロイド系の凝固、エマルジョンの分離、粉末の湿しおよび融解、1つの薬物の別の表面への吸着などである可能性があります。 色、匂い、薬物の変化の一貫性。 そのような不合理な処方は薬剤師に知られています。 したがって、そのような処方は行われないか、またはそれらの医薬的修正が実行され、その結果、患者は十分に準備された薬を受け取ります。
^ 薬理学的相互作用 薬物は、患者の体内に導入された後に発生します。 この相互作用の結果として、同時に投与される薬物の薬理効果が変化する可能性があります。
薬理学的相互作用には、薬物動態と薬力学の2つのタイプがあります。
A)薬物動態タイプの相互作用は、薬物の吸収、分布、代謝、排泄の段階で現れます。 この場合、1つ以上の薬物動態パラメーターが変化する可能性があります。 薬物動態学的相互作用の結果として、血液および組織中の原薬の活性型の濃度が最も頻繁に変化し、この結果として、最終的な薬理効果が変化します。
消化管からの吸収中の薬物の相互作用(GIT)
胃と小腸の内腔にいくつかの薬物が同時に存在するため、吸収の程度と速度、またはその両方が同時に変化する可能性があります。 このような変更の理由はさまざまです。
PH変更 "
ほとんどの薬物は、毛皮によって消化管から血液に吸収されます
低単純拡散。 このようにして、親油性および非イオン性
薬物の分子。 多くの医薬品
弱塩基または弱酸とそのイオン化度
培地のpHに依存します。 胃や腸のpHを変えると、次のことができます
分子のイオン化の程度、したがって吸収を変更します。 たとえば、
胃酸のpHを上げ、吸収を遅らせる酸剤
弱酸性化合物(ジゴキシン、バルビツール酸、ラニチジン)、弱化
それにより、それらの薬理効果。
吸収しにくい複合体の形成
吸着特性を持つ薬(石炭ak
ドープ)、陰イオン交換樹脂(コレスチラミン)、Ca 2 +、Mg 2 +、Al 3+イオン
困難な多くの医薬品と複合体を形成する
消化管から吸収されます。
胃腸運動の変化
コリン作動薬および抗コリンエステラーゼ薬、下剤の影響下での腸の運動性の刺激、および関連する腸内容物の加速により、ジゴキシンの吸収が低下し、
コルチコステロイド。 反対に、アトロピンMコリン作動性遮断薬は、胃内容排出を遅くし、ジゴキシンの吸収を促進します。
血漿タンパク質への結合段階での薬物の相互作用
全身循環に入ると、多くの薬用物質が血漿タンパク質に可逆的に結合します。 この段階で、薬物の相互作用が発生する可能性があります。これは、タンパク質との複合体からの、ある薬物物質の別の薬物物質の競合的置換に基づいています。 したがって、アセチルサリチル酸(アスピリン)は、タンパク質との複合体からトルブタミドを置換し、その結果、遊離トブタミド分子の濃度が増加し、血糖降下作用が強まります。
代謝過程における薬物の相互作用
多くの薬物の代謝は、ミクロソームの肝臓酵素によって行われます。 一部の医薬品は、その活動を変えることができます。 肝臓酵素フェノバルビタール、リファンピシン、フェニトインの活性を誘発(増加)します。 それらの背景に対して、特定の薬用物質(ジゴキシン、ドキシサイクリン、キニジン)の代謝が増加し、急速な不活性化と治療効果の低下につながります。 肝酵素クロラムフェニコール、ブタジオン、シメチジンの活性を阻害(低減)します。 この場合、フェニトイン、トルブタミド、テオフィリン、カフェインなどの物質の代謝が低下し、その効果が高まり、毒性効果が現れることがあります。 一部の薬物は、非ミクロソーム酵素の活性に影響を与えます。 したがって、アロプリノールは、メルカプトプリンの代謝に関与するキサンチンオキシダーゼ酵素を阻害し、造血系に対する後者の毒性効果が急激に増加します。
体からの排泄の過程における薬物の相互作用
薬用物質とその代謝物の排泄の主な器官は腎臓であるため、尿のpHは多くの薬用物質の排泄に大きな役割を果たします。 この指標は分子のイオン化の程度を調節し、イオン化は分子の再吸収を決定します。 腎尿細管での逆吸収。 尿の低pH値(酸性環境)では、弱アルカリ性物質(カフェイン、モルヒネ、エリスロマイシン)の排泄が増加するため、その効果は弱まり、短くなります。 アルカリ環境に対応する尿のpH値では、弱酸(バルビツール酸、ブタジオン、テトラサイクリン、スルファニルアミド)の排泄が加速され、その影響が低減されます。
B)薬物物質の相互作用の薬力学的タイプは、それらの薬理効果の実施に現れます。 ほとんどの場合、この相互作用は、対応する受容体に関連するアゴニストとアンタゴニストの同時使用で観察されます。 たとえば、アドレナリン受容体遮断薬(フェントラミン、プロプラノロール)は、アドレナリン受容体刺激薬(それぞれノルエピネフリン、イサドリン)の作用を軽減または完全に排除します。
交感神経遮断薬(レセルピン、グアネチジン)は交感神経刺激性エフェドリンの効果を弱めます。 にアドレナリン作動性神経の末端からのノルエピネフリンの配分。
効果の弱体化は、体のシステムで反対の方法で作用する薬物の同時使用によって引き起こされます。
一例として、中枢神経系の抑制(睡眠薬、鎮静剤)および刺激(精神刺激薬)。
同じ効果を引き起こす薬物を同時に使用すると、作用が増加します。
薬剤相互作用のタイプを明確に理解しているので、薬剤師は、2種類以上の薬剤を服用しながら、患者にとって望ましくない結果を修正できます。 これには次のオプションがあります。
同時にではなく、30〜40〜60分間隔で薬を服用します。
薬の1つを別のものと交換します。
薬物の投与計画を変更する(投与間の投与量と間隔を変更する);
薬物の1つをキャンセルします(最初の3つのアクションで、同時に処方される薬物の組み合わせの相互作用による悪影響を排除できない場合)。
薬物の薬物動態と薬力学は時刻に依存します。時刻は、酵素や他の内因性の生物学的活性物質の活動の周期的(周期的)変化、および体内の他のリズムプロセスに関連しています。 生物のリズミカルなプロセスと生物学的プロセスにおける時間因子の役割の研究は、時間生物学(ギリシャ語から。 クロノス -時間)は、前世紀の60年代に出現した生物学の比較的新しい方向です。 時間生物学のセクションの1つは時間薬理学であり、これは投与の時期および生物学的リズムに対する薬物の効果に応じて、薬物の活性の周期的な変化を研究します。
生物学的リズムは、生物学的プロセスの性質と強度の周期的に繰り返される変化です。
アクロフェーズ-調査対象の機能またはプロセスが最大値に達する時間。 bathyphase-調査された機能またはプロセスが最小値に達する時間。 振幅-調査したインジケータの平均からの両方向の偏差の程度。 Mesor(lat。 メソス - 単語の真ん中と最初の文字 リズム)-これは、毎日の平均リズムレベルです。 日中に調査した指標の平均値(図3.2)。
生物学的リズムの周期は、特定の時間、たとえば概日(概日、緯度から 年頃 -について 死ぬ -日)-20〜28時間の期間。 24時間-3〜20時間の期間。 インフララジアン-期間28〜96時間。 1週間あたり-4〜10日。 1か月あたり-25〜35日など
人体の生物学的プロセスの最も研究されている概日リズム(表3.1)。
次の用語が時間薬理学で受け入れられています:時間薬物動態(時間運動学)、時間感覚感覚および時間学。
経時薬物動態には、薬物の吸収、分布、代謝、排泄のリズムの変化が含まれます。
色覚異常は、日中の薬用物質に対する生物の感受性と反応性のリズミカルな変化です。
P細胞、器官、生理学的システム、生物全体の機能 
表3.1。健康な人のサーカディアンシステム(F. Halbergによる)
| 指標 | アクロフェーズ(時間 最大値、h) |
| 温度(t) | 16-18 |
| パルス(pi) | 15-16 |
| 呼吸数 | 13-15 |
| 血圧(収縮期) | 15-18 |
| 赤血球 | 11-12 |
| 白血球 | 21-23 |
| Tリンパ球 | 0-1 |
| Bリンパ球 | 4-5 |
| 血漿ホルモン: | |
| コルチゾール | 8-11 |
| 17-ヒドロキシコルチコステロン | 8-11 |
| キャンプ | 8-11 |
| レニン | 18 |
| テストステロン | 8-9 |
| チロキシン | 14-15 |
| 総血中タンパク質 | 17-9 |
| フィブリノゲン | 18 |
| ビリルビン | 10 |
| トランスアミナーゼ | 8-9 |
| コレステロール | 18 |
| 尿素窒素 | 22-23 |
クロナジーとは、原薬の薬理効果の大きさに対するクロノキネティクスと時間感覚の複合効果です。 同じ用量の物質を使用した場合の効果は、1日の異なる時間に不均等に現れます。その強度と持続時間は、数時間、および他の時間で大きくなります。
日数が大幅に短縮されました。 したがって、ニトログリセリンは、午後よりも午前中に狭心症の発作をより効果的に排除します。 グルココルチコイドは午前8時に最も活性が高く、モルフィンは16時に活性があります。
一部の薬物では、時刻に応じた薬物動態パラメーター(吸収、生体内変化、排泄)の変化が知られています。 そのため、抗真菌薬グリセオフルビンは正午頃に吸収されやすくなり、大量のアンフェタミンは早朝に腎臓から排泄されます。
日中の特定の薬物の濃度の変化に関するデータを表3.2に示します。
表3.2。 経時薬物動態(A.ラインバーグ、M。スモレンスキー)
| 麻薬 | 投与時間、h | 研究指標 | 薬物動態パラメーターの毎日の変化 |
| アセチルサリチル (1.5 g 1回) | 6 10 18 20 | 血漿濃度 | ピーク濃度と薬物動態曲線下の面積は、午前6時が最大、23時が最小 |
| インドメタシン (100 mg 1回) | 7; 11 15; 19 | 血漿濃度 | 8時間で最高のピーク濃度、19時間で薬剤物質の最速消失 |
| テオフィリン (4 mg / kg繰り返し) | 7 | 血漿および唾液中の濃度 | 7時間で高いピーク |
| プロプラノロール(アナプリリン、インデラル、オブジダン-80 mg 1回) | 2 8 | 血漿濃度 | 薬物動態曲線の下のピーク濃度と面積は、夜間の8、20および2時間と比較して、14時間での薬物の投与後は小さくなります。 |
| エリスロマイシン(250 mg x 4) | 2 | 血漿濃度 | ピーク濃度は最大〜11時間30分、S-最大12時間 |
| シスプラチン(60 mg / m 2 iv) | 6 | 尿中排泄と尿クレアチン | ピーク濃度と薬物動態曲線下面積は6時間で最大になり、腎毒性は18時間で最小になります |
薬剤を処方するための時間薬理学的アプローチは、投与時期に応じて、薬剤の合理的な投与量にとって重要です。 従来の治療法では、処方された用量が処方され(たとえば、1錠を1日3回)、時間療法では、身体の感度と反応性のサーカディアン変動と薬物動態プロセスのリズムを考慮して動的用量が使用されます。
クロノセラピーの目標は、薬物の最低コストで最大の治療効果を達成し、その結果、副作用を減らすことです。
薬局の薬理学部で行われた実験および臨床研究に基づいて、MMAは I.M. SechenovとVMAそれら。 SM キーロフは、多くの薬物の作用における時間薬理学的特徴を明らかにした。 だから、行動に対する最大の感度
静脈内ストリキニーネのレベルは16時に現れ、午前10時に最大の安定性を示しました。
特定の薬物の作用における季節要因の役割も確立されています。 植物アダプトゲンの適応効\u200b\u200b果:高麗人参、バイオ人参、エレウテロコッカス、ロディオラロゼア、アラリア、異なる季節(1月から3月、5月、7月)の動物実験および外科的および神経病理学的患者の1月から3月、および 夏には、それらの適応効果は著しく低下します。 さらに、春夏の期間には、研究された広範囲の用量で、高麗人参とエウロコッカスの抗低酸素効果は見られません。
身体に作用する薬用物質は、特定の臓器やシステムの活動に変化を引き起こします。 たとえば、薬は心臓の収縮を増加させ、気管支痙攣をなくし、血圧を上げ、恐怖と精神的緊張を取り除き、痛みを軽減し、精神活動を刺激する、などができます。 薬理効果".
各薬物について、特定の薬理効果が特徴的です。 いずれの場合も、治療目的で、薬物の特定の効果のみが使用されます。 このような効果は 主な薬理効果。 残りの(未使用、望ましくない)薬理効果は、 担保.
薬理効果のすべてを知らずに薬物を使用することは受け入れられません。 したがって、気管支喘息にエフェドリン(第4章を参照)を使用するには、エフェドリンが気管支を拡張することを知るだけでは不十分です。 この薬はまた、心臓の自動化(頻脈性不整脈に禁忌)を増加させ、血圧(高血圧に禁忌)を増加させ、中枢神経系を刺激します(不眠症を引き起こす可能性があるため、エフェドリンは夜に処方されるべきではありません)。
同じ薬理効果 さまざまな物質 多くの方法で呼び出すことができます。 たとえば、血圧を下げるには、心臓の仕事を減らし、血管を拡張し、血漿量を減らします。 同様に、これらの機能はさまざまな方法で実装できます。 そのため、血管の平滑筋に直接作用するか、交感神経支配の血管収縮効果をブロックすることにより、血管を拡張できます。 後者は、交感神経系の興奮が伝達される交感神経節、交感神経の末端または血管の受容体を遮断することにより達成することができます。
医薬品が特定の薬理効果を引き起こす方法は、「 作用機序".
ほとんどの薬用物質は、さまざまな臓器の機能を刺激または阻害し、それらに影響を与えます 特定の受容体。 これらの受容体は、ほとんどの場合、これらの機能が関連付けられているタンパク質分子です。 特定の受容体の例には、コリン作動性受容体(第3章を参照)、アドレナリン受容体(第4章を参照)、オピエート受容体(第10章を参照)などがあります。 たとえば、抗コリンエステラーゼ剤の場合(第3章を参照)、アセチルコリンエステラーゼは特定の受容体です。
特定の受容体に対する物質の作用に直接関係する変化は、「一次薬理反応」という用語で示されます。 主要な薬理反応は、特定の生理学的機能の刺激または抑制につながる一連の反応の始まり、すなわち、所定の原薬に特有の薬理効果であり得る。
特定の薬物(浸透圧利尿薬など、第16章を参照)は、特定の受容体に関係なく効果を示します。
さまざまな薬物の作用メカニズムがさまざまな程度で研究されています。 実際、物質の作用メカニズムが完全に知られているとは言えません。 したがって、薬物の作用機序の研究は進行中です。 同時に、1つまたは別の医薬品の作用メカニズムに関するアイデアは、より詳細になるだけでなく、大幅に変化する可能性があります。 ただし、薬物の作用機序に関する知識は、薬物の適切な使用のために貴重な支援を提供します。
必須医薬品のディレクトリElena Yuryevna Hramova
薬理学的および副作用
一般に、薬物は特定の物理化学的特性を持ち、特定の形態で放出され、身体に治癒効果をもたらす物質および(または)その混合物です。
薬理効果は、組織または細胞レベルでの身体に対する薬物(より正確には、含まれる活性物質)の影響によって決定されます。 理想的には、薬理効果には副作用が伴わないようにする必要があります。つまり、ある臓器を助け、別の臓器に害を与えるべきではありません。
特定の薬物の薬理効果は、その化学組成、濃度、放出される形態、および体内に導入される量によって決定されます(残念ながら、薬物の過剰摂取は頻繁な現象です)。 実際、薬物の薬理効果は、この薬物の影響下で発達する、人体の細胞および組織、ならびにその器官またはシステムの代謝および機能における特定の変化です。
多くの薬物は、一連のいわゆる有害反応または作用を引き起こします。 一部の薬物は非常に毒性があるため、他の臓器(またはシステム)の機能を不可逆的に破壊する可能性があるため、例外的な場合に限られた用量で医師の監督下でのみ使用されます。
薬を使用または処方する前に、注釈を注意深く読む必要があります。これは、消化不良性障害、注意力の低下などの副作用が頻繁に示されるためです。 最後の状況は、仕事が常に迅速な反応の必要性と関係している人々(ドライバーなど)に特に注意を払う必要があります。 多くの場合、薬物の可能性のある望ましくない(サ\u200b\u200bイド)アクションのリストは、それに付随する注釈に数行かかる場合があります。
本ホメオパシーから。 パートI.ホメオパシーの基礎 著者GerhardKöller3.薬物の副作用薬物の副作用は、類似性ルールが厳密に守られておらず、患者の感度が急激に上昇した場合に発生する可能性があります。 例。 患者は、大中手指節関節の痛みを伴う炎症を報告した
甲状腺の回復患者ガイドの本から 著者 アンドレイ・ヴァレレヴィッチ・ウシャコフ硬化の副作用硬化の最小の損傷効果に関係なく、この手順は積極的な効果と見なされる必要があります。 そのリスクとそれに伴うトラブルとは何ですか?痛みの少ない手順にもかかわらず、すべて
ブックからヘルプまで 著者 ナタリア・レドネバ副作用 化学療法脱毛細胞毒性薬(特に高用量)は、血液細胞だけでなく、発毛の原因となる細胞にも作用します。 通常、治療後または化学療法の投与量が次のようになると、髪が元に戻ります
本「調和のために自分でコーディングする」から 著者 ミハイル・ボリソヴィッチ・インゲルレイブ手術の副作用
著者 アッラ・ヴィクトロヴナ・ネステロワ副作用スルファニルアミド薬はめったに副作用を引き起こしませんが、場合によっては白血球減少や血小板減少、皮膚アレルギー反応、肝機能障害、胃腸障害があります。 薬物の過剰摂取
「糖尿病の臨床栄養」の本から 著者 アッラ・ヴィクトロヴナ・ネステロワ副作用副作用の中でも、患者が口、吐き気、嘔吐、および下痢に金属味を感じている場合、胃腸管の機能障害に注意する必要があります。 これらの薬は、肝機能障害、アレルギーを引き起こす可能性もあります
本「ヨウ素-あなたの内科医」から 著者 アンナ・ヴィャチェスラヴォヴナ・シェグロワヨウ素含有薬物の禁忌と副作用前述のように、ヨウ素は誰にとっても有用ではありません。 それを含む薬が健康状態を悪化させることがあります。 そして、以前のヨウ素の許容用量の単純な過剰でさえ
本「足の病気と静脈瘤の治療」から 著者 エフゲニア・ミハイロフナ・スビトネヴァ軟骨保護剤の副作用ほとんどの場合、軟骨保護剤を服用した後、副作用はありません。 しかし、一部の患者では、腸の違反があり、悪心、嘔吐、痛み、下痢の形で現れました。 非常にまれなアレルギー
著者ヴァディム・ラプシチェフ ヒーリングハニーの本から 著者 ニコライ・イラリオノヴィッチ・ダニコフ医学的治療中の副作用医学的治療中の副作用は、身体の皮膚、呼吸器および胃腸の反応に表れます。 それらは、蜂蜜の遺伝性または後天性過敏症、ミツバチが集まる蜂蜜植物の種類に依存します
ザルマノフによると、さらに容器をきれいにし、さらにクリーナーの本から 著者 オルガ・カラシニコワ毛細血管の薬理学的治療:医療従事者に人気のあるVidalとM.D. Mashkovskyは、別の章で毛細血管の治療のための資金を割り当てていません。 これは改善する薬という意味ではありません
百病からの本フキタンポポから 著者 ユーリ・コンスタンティノフ禁忌と副作用民間療法の母と継母は非常に好きです、煎じ薬、注入はそれから準備され、彼らはまたジュースを作ります。 しかし、フキタンポポに基づいた製剤を使用する場合、グリコシドが葉に含まれていることを覚えておく必要があります。 そして、それは常にあふれています
本「危険な薬」から。 伝統的な治療の危機 著者 アルシャク・アルチュノフナ・ナリャン副作用 必須医薬品ワクチンワクチンは、望ましくない効果が最初に現れます。 予防接種に対する多くの議論がありますが、これを確認する1つの例があります。 1960年代から1980年代までのほとんどのワクチンと抗菌剤
地球上で最も健康的な飲み物の本から。 辛口の赤ワイン。 私たちから隠されている真実! 著者 ウラジミール・サマリン 本低血圧から 著者 アナスタシア・ゲンナディエヴナ・クラシチコワ副作用副作用の発生は、セルフメディケーションの最も一般的で深刻な結果の1つです。 アレルギー反応 アナフィラキシーショック、吐き気、腹痛、嘔吐、軟便、便秘、頻脈、心の痛み、競馬まで
本から悪い習慣を取り除く最も信頼できる真実の方法。 シチコ法 著者ヴァディム・ラプシチェフ方法の「副作用」アルコール依存症と喫煙をなくす過程が正常に完了すると、「24歳のときの体重を取り戻したい」という賞が待っていました。 考えるべきことがありました一時禁煙した後
第2章薬力学
薬力学には、薬理効果の概念、薬物の作用の局在化、および薬物の作用のメカニズム(すなわち、薬物が体内でどのように、どこで、どのように作用するかについてのアイデア)が含まれます 薬力学には、薬物の作用の種類の概念も含まれます。
2.1。 薬物の薬理効果、局在化および作用機序
薬理効果とは、薬物によって引き起こされる臓器および身体の機能の変化です。 薬物の薬理効果には、たとえば、心拍数の増加、血圧の低下、痛みの感度のしきい値の増加、体温の低下、睡眠時間の延長、妄想や幻覚の排除などがあります。 原則として、各物質は、それを特徴付けるいくつかの特定の薬理効果を引き起こします。 さらに、薬のいくつかの薬理効果は有用です-それらのおかげで、薬は医療行為で使用されます(主な効果)、
その他は使用されておらず、さらに望ましくありません(副作用)。
多くの物質について、体内でのそれらの主要な作用の場所は知られています-つまり アクションのローカライズ。 一部の物質は主に特定の脳構造に作用し(抗パーキンソン病、抗精神病薬)、他の物質は主に心臓に作用します(強心配糖体)。
最新の方法論的手法のおかげで、全身および臓器だけでなく、細胞および分子レベルでの物質の作用の局在を決定することが可能です。 たとえば、強心配糖体は、心臓(臓器レベル)、心筋細胞(細胞レベル)、心筋細胞膜のNa +-、K + -ATPase(分子レベル)に作用します。
同じ薬理効果がさまざまな方法で引き起こされる可能性があります。 したがって、血圧の低下、アンジオテンシンIIの合成の低下(ACE阻害薬)、平滑筋細胞でのCa 2+の摂取の遮断(電位依存性カルシウムチャネル遮断薬)、または交感神経の端からのノルエピネフリンの放出を減らす(交感神経遮断薬)物質があります。 薬物が薬理効果を引き起こす方法は、メカニズムとアクションとして定義されます。
ほとんどの薬物の薬理効果は、特定の分子基質、いわゆる「標的」に対する作用によって引き起こされます。
薬物の主な分子「標的」には、受容体、イオンチャネル、酵素、輸送システムが含まれます。
受容体
A.受容体の特性と種類。 受容体と酵素およびイオンチャネルとの相互作用
受容体は、機能的に活性な高分子またはそのフラグメント(主にタンパク質分子-リポタンパク質、糖タンパク質、核タンパク質など)です。 物質(リガンド)と受容体の相互作用では、一連の生化学反応が起こり、特定の
薬理効果。 受容体は、内因性リガンド(神経伝達物質、ホルモン、他の内因性の生物活性物質)の標的として機能しますが、薬物などの外因性の生物活性物質と相互作用することもできます。 受容体は、特定の化学物質(特定の化学構造と空間的方向性を持つ)とのみ相互作用します。 選択性があるため、 特定の受容体。
受容体は安定した、既存の細胞構造ではありません。 それらの数は、受容体タンパク質の合成の優位性のために増加するか、またはそれらの分解プロセスのvalence延のために減少するかもしれません。 さらに、受容体は機能的活性を失う可能性があります。 (減感作)その結果、受容体がリガンドと相互作用する場合、生化学反応は起こらず、薬理学的効果につながります。 これらのプロセスはすべて、リガンドの濃度と受容体に対する効果の持続時間によって規制されています。 リガンドへの長期暴露により、受容体の脱感作および/またはその数の減少が発生する (ダウンレギュレーション)そして逆に、リガンドの不在(またはその濃度の減少)は、受容体の数の増加につながります (アップレギュレーション)。
受容体は、細胞膜(膜受容体)または細胞質または核の細胞内(細胞内受容体)に配置できます(図2-1)。
膜受容体。 細胞外および細胞内ドメインは、膜受容体で分離されています。 細胞外ドメインには、リガンド(受容体と相互作用する物質)の結合部位があります。 細胞内ドメインは、エフェクタータンパク質(酵素またはイオンチャネル)と相互作用するか、それ自体が酵素活性を持っています。
3種類の膜受容体が知られています。
1. 酵素に直接結合した受容体。これらの受容体の細胞内ドメインは酵素活性を示すため、酵素受容体または触媒受容体とも呼ばれます。 このグループのほとんどの受容体には チロシンキナーゼアクティビティ。 受容体が物質に結合すると、チロシンキナーゼが活性化され、それが細胞内タンパク質をリン酸化し、したがってその活性を変化させます。 これらの受容体には、インスリン、特定の成長因子、およびサイトカインの受容体が含まれます。 受容体はグアニル酸シクラーゼと直接関連しています(心房性ナトリウム利尿因子にさらされると、グアニル酸シクラーゼが活性化され、細胞内の環状グアノシン一リン酸の含有量が増加します)。
2. イオンチャネルに直接結合した受容体、細胞膜を貫通し、イオンチャネルを形成するいくつかのサブユニットで構成されています。 物質が受容体の細胞外ドメインに結合すると、イオンチャネルが開き、その結果、さまざまなイオンに対する細胞膜の透過性が変化します。 そのような受容体には、H-コリン作動性受容体、サブタイプAに関連するγ-アミノ酪酸(GABA)の受容体、グリシン受容体、グルタミン酸受容体が含まれます。
Nコリン受容体は、細胞膜を貫通する5つのサブユニットで構成されています。 2つのアセチルコリン分子が受容体の2つのαサブユニットに結合すると、ナトリウムチャネルが開き、ナトリウムイオンが細胞に入り、細胞膜の脱分極を引き起こします(骨格筋では、筋肉の収縮につながります)。
GABA A受容体は塩素チャネルに直接結合しています。 受容体がGABAと相互作用すると、塩素チャネルが開き、塩素イオンが細胞に入り、
細胞膜の過分極(これにより、中枢神経系の抑制プロセスが増加します)。 グリシン受容体は同じように機能します。 3。 Gタンパク質と相互作用する受容体。これらの受容体は、タンパク質(Gタンパク質-グアノシン三リン酸(GTP)結合タンパク質)を介して酵素および細胞のイオンチャネルと相互作用します。 物質が受容体に作用すると、Gタンパク質のαサブユニットがグアノシン三リン酸に結合します。 この場合、Gタンパク質グアノシン三リン酸複合体は酵素またはイオンチャネルと相互作用します。 原則として、1つの受容体はいくつかのGタンパク質に結合しており、各Gタンパク質はいくつかの酵素分子またはいくつかのイオンチャネルと同時に相互作用できます。 この相互作用の結果として、効果は増幅されます(増幅されます)。
Gタンパク質とアデニル酸シクラーゼおよびホスホリパーゼCとの相互作用はよく研究されています。
アデニル酸シクラーゼは、ATPを加水分解する膜結合酵素です。 ATP加水分解の結果として、環状アデノシン一リン酸(cAMP)が形成され、これが細胞タンパク質をリン酸化するcAMP依存性プロテインキナーゼを活性化します。 この場合、タンパク質の活性とそれらによって調節されるプロセスが変化します。 アデニル酸シクラーゼの活性に対する効果に従って、Gタンパク質は、アデニル酸シクラーゼを刺激するG sタンパク質とこの酵素を阻害するG iタンパク質に細分されます。 Β1-アドレナリン受容体(交感神経支配の心臓への刺激効果を媒介する)はG sタンパク質と相互作用する受容体の例であり、M 2-コリン受容体はG i-タンパク質と相互作用します(心臓の副交感神経支配の抑制効果を媒介する)。 これらの受容体は、心筋細胞の膜に局在しています。
β1-アドレナリン受容体が刺激されると、アデニル酸シクラーゼ活性が増加し、心筋細胞のcAMPの含有量が増加します。 その結果、プロテインキナーゼが活性化され、心筋細胞の膜のカルシウムチャネルをリン酸化します。 これらのチャネルを介して、カルシウムイオンが細胞に入ります。 細胞へのCa 2+の侵入が増加し、これにより洞結節の自動化が増加し、心拍数が増加します。 反対方向の細胞内効果は、心筋細胞のM 2-コリン作動性受容体の刺激中に発生し、その結果、洞結節および心拍数の自動化が低下します。
Gqタンパク質はホスホリパーゼCと相互作用し、その活性化を引き起こします。 Gqタンパク質と結合した受容体の例は、血管平滑筋細胞のgアドレナリン受容体です(交感神経支配の血管への影響を媒介します)。 ホスホリパーゼCは細胞膜のホスファチジルイノシトール-4,5-二リン酸を加水分解し、親水性物質であるイノシトール-1,4,5-三リン酸を形成し、細胞の筋小胞体のカルシウムチャネルと相互作用してCa 2の放出を引き起こします。 +細胞質内。 平滑筋細胞の細胞質内のCa 2+濃度が増加すると、ミオシン軽鎖のキナーゼを活性化するCa 2+-カルモジュリン複合体の形成速度が増加します。 この酵素はミオシンの軽鎖をリン酸化し、その結果、アクチンとミオシンの相互作用が促進され、血管平滑筋収縮が起こります。
Gタンパク質と相互作用する受容体には、ドーパミン受容体、セロトニン(5-HT)受容体のいくつかのサブタイプ、オピオイド受容体、ヒスタミン受容体、ほとんどのペプチドホルモンの受容体なども含まれます。
細胞内受容体 物質の調節作用を媒介する可溶性の細胞質または核タンパク質 dNA転写用。細胞内受容体のリガンドは、親油性物質(ステロイドおよび甲状腺ホルモン、ビタミンA、D)です。
リガンド(糖質コルチコイドなど)と細胞質受容体の相互作用により、物質受容体複合体が細胞核に移動し、DNA分子の特定のセクションに結合するため、立体構造の変化が生じます。 さまざまな機能的に活性なタンパク質(酵素、サイトカインなど)の合成をコードする遺伝子の転写に変化(活性化または抑制)があります。 酵素および他のタンパク質の合成の増加(または減少)は、細胞内の生化学プロセスの変化と薬理効果の出現につながります。 したがって、糖新生酵素の合成に関与する遺伝子を活性化する糖質コルチコイドは、グルコース合成を刺激し、それが高血糖症の発症に寄与します。 サイトカイン、細胞間接着分子、シクロオキシゲナーゼ、グルココルチコイドの合成をコードする遺伝子の抑制の結果として、免疫抑制および抗炎症効果があります。 薬理学
細胞内受容体との相互作用中の物質の効果はゆっくりと(数時間、さらには数日かけて)発達します。
核内受容体との相互作用は、甲状腺ホルモン、ビタミンA(レチノイド)およびDに特徴的です。核内受容体の新しいサブタイプが発見されました- ペルオキシソーム増殖因子によって活性化される受容体。これらの受容体は、脂質代謝および他の代謝プロセスの調節に関与しており、クロフィブラート(脂質低下薬)の標的です。
B.受容体への物質の結合。 親和性の概念
薬物が受容体に作用するためには、薬物に接触する必要があります。 その結果、「物質受容体」複合体が形成されます。 そのような複合体の形成は、分子間結合を使用して実行されます。 このような関係にはいくつかのタイプがあります。
共有結合は、分子間結合の中で最も耐久性のあるタイプです。 それらは、共通の電子対により2つの原子間で形成されます。 ほとんどの場合、共有結合は 不可逆的結合しかし、物質は薬物と受容体の相互作用に特徴的ではありません。
イオン結合はあまり強くありません;電荷とは異なるグループ間で生じます(静電相互作用)。
イオン-双極子および双極子-双極子結合は、本質的にイオン結合に似ています。 細胞膜の電界に入るか、またはイオンに囲まれた電気中性薬物分子では、誘導双極子の形成が発生します。 イオン結合と双極子結合は、薬物と受容体の相互作用に特徴的です。
水素結合は、薬物と受容体の相互作用において非常に重要な役割を果たします。 水素原子は、酸素、窒素、硫黄、ハロゲンの原子と結合できます。 水素結合は弱く、その形成のために、分子は0.3 nm以下の距離で互いに離れている必要があります。
ファンデルワールス結合は、0.2 nm以下の距離にある場合、2つの原子間に形成される最も弱い結合です。 距離が長くなると、これらの結合は弱まります。
疎水性結合は、水性媒体中の非極性分子の相互作用によって形成されます。
親和性という用語は、物質の受容体への結合を特徴付けるために使用されます。
アフィニティ(lat。 アフィニス-関連)-物質が受容体に結合し、「物質-受容体」複合体を形成する能力。 さらに、「親和性」という用語は、物質の受容体への結合強度(すなわち、「物質-受容体」複合体の持続時間)を特徴付けるために使用されます。 物質の受容体への結合強度としての親和性の定量的尺度は 解離定数(K d)。
解離定数は、このシステムの受容体の半分が物質に関連付けられている物質の濃度に等しい。 この指標は、モル/ l(M)で表されます。 親和性と解離定数の間には反比例の関係があります。Kdが小さいほど親和性が高くなります。 たとえば、 に d 物質Aの親和性は10 -3 Mに等しく、物質BのK dは10 -10 Mであり、物質Bの親和性は物質Aの親和性よりも高い。
B.薬物の内部活動。 受容体アゴニストおよびアンタゴニストの概念
親和性を持つ物質には、内部活性がある場合があります。
内部活動とは、受容体と相互作用するときに、物質を刺激して特定の効果を引き起こす物質の能力です。
内部活動の存在に応じて、薬物は アゴニストそして 拮抗薬受容体。
アゴニスト(ギリシャ語から アゴニスト-相手 アゴン-闘争)または 擬態-親和性と内部活性を持つ物質。 特定の受容体と相互作用するとき、それらはそれらを刺激します。 受容体の立体構造の変化を引き起こし、一連の生化学反応と特定の薬理効果をもたらします。
受容体と相互作用する完全なアゴニストは、可能な最大の効果を引き起こします(最大の内部活性があります)。
部分アゴニストは、受容体と相互作用する場合、最大値よりも小さい効果を引き起こします(最大の内部活性はありません)。
アンタゴニスト(ギリシャ語から 拮抗-競争 反-に対して アゴン-闘争)-親和性はあるが、内部活性を欠く物質。 受容体に結合することにより、これらの受容体に対する内因性アゴニスト(神経伝達物質、ホルモン)の作用を阻害します。 したがって、アンタゴニストは受容体および受容体とも呼ばれます。 アンタゴニストの薬理効果は、これらの受容体の内因性アゴニストの作用の排除または減衰によるものです。 この場合、アゴニストの効果と反対の効果が生じます。 したがって、アセチルコリンは徐脈を引き起こし、心臓に対するアセチルコリンの作用を排除するM-コリン受容体のアトロピン拮抗薬は心拍数を増加させます。
拮抗薬が作動薬と同じ結合部位を占有している場合、それらは受容体との通信を互いに強制することができます。 同様のタイプの拮抗作用は競合的拮抗作用と呼ばれ、拮抗薬は競合的拮抗薬と呼ばれます。 拮抗作用は、特定の受容体に対する競合物質の親和性とその濃度に依存します。 十分に高い濃度では、親和性の低い物質でさえ、受容体から親和性の高い物質に置き換わることがあります。 だから 拮抗作用があると、アゴニストの効果は培地中の濃度が増加すると完全に回復します。薬の毒性作用を排除するために、しばしば拮抗作用が使用されます。
部分アンタゴニストは、結合部位について完全アゴニストと競合する可能性もあります。 完全なアゴニストを受容体への結合から置き換えることにより、部分的アゴニストはその効果を低下させるため、アンタゴニストの代わりに臨床で使用できます。 例えば、部分的なβ-アドレナリン受容体アゴニスト(ピンドロール)およびこれらの受容体のアンタゴニスト(プロプラノロール、アテノロール)は、高血圧の治療に使用されます。
拮抗薬が受容体のいわゆるアロステリック結合部位(作動薬の結合部位ではないが受容体活性を調節する高分子部位)を占有すると、非競合的拮抗作用が発現します。 非競合的拮抗薬は受容体の立体構造を変化させる
アゴニストと相互作用する能力を失うような方法で。 この場合、アゴニストの濃度の増加は、その効果の完全な回復につながることはできません。 物質の受容体への不可逆的(共有)結合により、非競合的拮抗作用も発生します。
一部の薬物は、1つの受容体サブタイプを刺激し、別の受容体サブタイプをブロックする能力を組み合わせています。 そのような物質は、アンタゴニストアゴニストとして指定されている(例えば、ブトルファノール、μのアンタゴニストおよびκオピオイド受容体のアゴニスト)。
薬物のその他の「ターゲット」
その他の「標的」には、イオンチャネル、酵素、輸送タンパク質が含まれます。
イオンチャンネル。薬物の主な「標的」の1つは、細胞膜を介してNa +、Ca 2 +、K +およびその他のイオンを選択的に伝導する電位依存性イオンチャネルです。 物質が受容体と相互作用すると開く受容体駆動型イオンチャネルとは異なり、これらのチャネルは活動電位によって調節されます(細胞膜が脱分極すると開く)。 薬物は、電位依存性のイオンチャネルをブロックし、それにより、それらを通るイオンの流れを妨害するか、または活性化、すなわち イオン電流の通過を促進します。 ほとんどの薬物はイオンチャネルをブロックします。
局所麻酔薬は、電位依存性のNa +チャネルを遮断します。 Na +チャネルの遮断薬には、多くの抗不整脈薬(キニジン、リドカイン、プロカインアミド)が含まれます。 一部の抗てんかん薬(フェニトイン、カルバマゼピン)も電位依存性のNa +チャネルをブロックし、その抗痙攣作用はこれに関連しています。 ナトリウムチャネル遮断薬は、Na +の細胞への侵入を妨害し、細胞膜の脱分極を防ぎます。
Ca 2+チャンネルのブロッカー(ニフェジピン、ベラパミルなど)は、多くの心血管疾患(高血圧、不整脈、狭心症)の治療に非常に効果的であることが判明しました。 カルシウムイオンは、多くの生理学的プロセスに関与します。平滑筋の収縮、洞房結節でのインパルスの生成、房室結節の興奮、血小板凝集など。遅いカルシウム遮断薬
チャネルは、電圧依存性チャネルを介した細胞へのカルシウムイオンの侵入を妨げ、血管の平滑筋の弛緩、心臓の収縮頻度の低下、AV伝導を引き起こし、血小板凝集を破壊します。 一部のカルシウムチャネル遮断薬(ニモジピン、シンナリジン)は、主に脳の血管を拡張し、神経保護効果があります(ニューロンへの過剰なCa 2+の侵入を防ぎます)。
薬として、活性化剤とカリウムチャネル遮断薬の両方が使用されます。 カリウムチャネルの活性化剤(ミノキシジル)は、降圧剤として使用されます。 それらは細胞からのカリウムイオンの放出に寄与し、細胞膜の過分極と血管平滑筋の緊張の低下をもたらします。 その結果、血圧が低下します。 電位依存性カリウムチャネル(アミオダロン、ソタロール)をブロックする薬剤は、不整脈の治療に使用されています。 それらは、心筋細胞からのK +の放出を防ぎ、その結果、活動電位の持続時間を延長し、有効不応期(ERP)を延長します。 膵臓のβ細胞におけるATP依存性カリウムチャネルの遮断は、インスリンの分泌増加につながります。 これらのチャネルのブロッカー(スルホニル尿素誘導体)は、抗糖尿病薬として使用されます。
酵素。多くの薬物は酵素阻害剤です。 MAO阻害剤は、カテコールアミン(ノルエピネフリン、ドーパミン、セロトニン)の代謝(酸化的脱アミノ化)を破壊し、中枢神経系の含有量を増加させます。 抗うつ剤の作用-MAO阻害剤(例えば、ニアラミド)はこの原理に基づいています。 非ステロイド系抗炎症薬の作用機序はシクロオキシゲナーゼの阻害に関連し、その結果、プロスタグランジンE 2およびI 2の生合成が減少し、炎症誘発効果が発現します。 アセチルコリンエステラーゼ阻害剤(抗コリンエステラーゼ剤)は、アセチルコリンの加水分解を阻害し、シナプス間隙の内容物を増加させます。 このグループの準備は、平滑筋器官(胃腸管、膀胱)と骨格筋の緊張を高めるために使用されます。
輸送システム。薬物は、細胞膜を介して特定の物質またはイオンの分子を輸送する輸送システム(輸送タンパク質)に作用します。 たとえば、三環系抗うつ薬は、シナプス前膜を介してノルエピネフリンとセロトニンを運ぶ輸送タンパク質をブロックします。
神経終末傷(ノルエピネフリンとセロトニンの逆ニューロン取り込みをブロックする)。 強心配糖体は心筋細胞膜のK + -ATPaseをブロックし、K +と引き換えに細胞からNa +を輸送します。
薬物が作用する他の「標的」が可能です。 そのため、制酸剤は胃の塩酸を中和し、胃液の酸性度を高めるために使用されます(過酸胃炎、胃潰瘍)。
薬物の有望な標的は遺伝子です。 選択的に作用する薬物の助けを借りて、特定の遺伝子の機能に直接影響を与えることが可能です。
PVは、身体に対する物質の作用の最終結果です。 すべての効果は2つのグループに分けられます。
・基本-医療行為で薬用物質が使用されるもの。 提供する効果 治療効果。 いくつかあるかもしれません。
・副作用-基本的ではない他のすべての効果。 原則として、治療用量の薬物で発生する望ましくない効果。
薬物療法の種類.
薬物はどのような目的で使用されますか:
好中球療法-病気の原因、病原体(最も効果的)
・病原性-病理発生のメカニズムを目的とする
症候性-病気の症状(高熱、下痢、脱水、けいれんなど)を目的としたもの-主なものはできません。
・置換-体内の不足している物質(インスリン、ビタミン、ホルモン)の置換を目的としています。
薬物の作用機序.
国際規格に合格したすべての薬は、有効性→作用機序が証明されています。
ほとんどの薬 受容体の作用機序 つまり 受容体に対する作用または受容体を介した作用。 受容体は受容薬です。 受容体は膜(それらに作用することにより、媒介物を介して細胞の機能を変える)、細胞質ゾルである。 受容体と相互作用する内因性物質-リガンドまたはメディエーター。 生理学的条件下では、これらのメディエーターは受容体と相互作用し、細胞に影響を及ぼします。 外部から来る薬はリガンドのように振る舞うことができ、この場合は呼ばれます アゴニスト つまり 受容体を刺激する、別名- 擬態。 受容体に応じて、H-コリン様物質、M-コリン様物質があります。
逆の方法で作用する物質- 拮抗薬 (ブロッカー)、彼らは受容体結合部位、別の名前の内因性物質と競合します- littics.
酵素の作用機序 -酵素の活性に対する薬物の効果。 それらは、組織、器官、システムの酵素を刺激または阻害することができます。 刺激されたら、 インダクタ -NOを含む製剤→アデニル酸シクラーゼを活性化→血管を拡張(ニトロソルビド)。 もし 阻害する -抗コリンエステラーゼ→ACHE活性を阻害→アセチルコルジン(プロセリン)が蓄積します。 モナアミンオキシダーゼ阻害剤(ニラミド)、アンジオテンシン変換酵素阻害剤-酵素をブロック→アンジオテンシン変換をブロック→圧力低下、シクロオキシゲナーゼブロッカー-NSAID。
イオンチャネルへの影響 -Kチャネルの活性化因子-細胞へのKの摂取を活性化→ナトリウム濃度を減少→Ca(ミノキシジル)の摂取を減少。 カリウムチャネル遮断薬(アミダロン)は抗不整脈薬です。 Caチャンネル遮断薬(ニフェジピン)もあります→筋収縮の強度を低下させます。
細胞輸送システムに影響を与える薬物 -例:胃の内層細胞の水素ポンプに影響を与える薬物。 ポンプは、Hイオンを胃の内腔(オメプラゾール)に輸送します。
薬物の繰り返し投与と突然の離脱による身体の反応。
· 中毒性の (耐性、抵抗、滑り効果)-薬理効果の急速な弱体化(バルビツール酸塩、精神安定剤、薬物、利尿薬、抗ヒスタミン薬)。 エフェドリン、アドレナリン、オクタジン-エスケープの現象(タキフィラキシーは急速な依存症です)。 中毒は生化学プロセスに基づいています-薬物を破壊する酵素の出現、細菌は抗生物質に慣れます。
· 累積(蓄積)-不活性化の遅延。 物質の蓄積は、血漿中の薬物の蓄積です。 機能的蓄積-薬物の効果の保存と合計-物質自体は蓄積しません(金属塩、強心配糖体、ビタミンA、D、フェノバルビタール、抗凝固剤、ステロイド、アルコール)。
· 感作とアレルギー -繰り返し投与される薬剤に対する感受性の向上(抗生物質、抗精神病薬、局所麻酔薬)。
· 薬物中毒-身体が何らかの物質に依存していること、その繰り返しの使用に対する抵抗できない欲求(向精神薬、麻薬、睡眠薬)。 麻酔科医は、精神的および肉体的依存を分けます。 精神的中毒-薬物を服用することで「喜び」を体験したいという願望 身体的依存はより深く、その発達は体内の代謝変化を示します。 この物質を使用しても、CCC、内分泌腺の機能に違反することはありません。 すべてのサイレントプロセスは以下に基づいています。 多幸感 -高い気分、満足した状態、穏やかな状態、問題からの離脱、 中毒 -繰り返したいという願望 離脱症状 -禁酒症候群は、依存症を発症した人に発症します。
· 離脱症候群 -薬物の突然の離脱、臓器機能の阻害による身体の反応。 副腎ホルモン製剤の長期使用で報告されています。
· リコイル症候群 -薬物の急激な中止後の疾患の症状の悪化によって明らかにされる。
薬物と共同使用の相互作用。
相互作用は最終的な効果を変える可能性があります。
次のタイプの相互作用が区別されます。
1.医薬品-製剤中の薬物相互作用 剤形
2.薬理学的(生理学的)-人体に。
・薬物動態-投与、吸収、生体内変化、排泄、薬物の濃度、および組成物自体の経路における薬物間の相互作用は変化する可能性があります。
・薬力学的-受容体レベルおよび他の作用メカニズムでの薬物の相互作用。 バイオアベイラビリティの変化にはつながりません。
相互作用により、 相乗効果 -相互作用するとき、お互いを強化します。 相乗効果の種類:
・合計-薬物の組み合わせが単純な算術合計に等しい効果を与える場合。
・強化-両方の薬物の効果は、両方の薬物の合計を超えます。
・付加的作用-合計すると、薬の効果はそれらの合計よりも少なくなります。
拮抗作用 -ある薬物の効果を別の薬物の効果の減少または完全な排除に導く薬物の反対の効果。 物理的拮抗、化学的、生理学的に基づいています。
拮抗作用の種類:
・直接-薬物は同じ基質に対して競合し、反対方向に作用します。
・間接-薬物は異なる基質に作用し、同時に反対の効果を引き起こします。
・片側-物質に有利
・いずれかが受容体に接触でき、用量が決定的である双方向。
薬物の副作用。
タイプA:薬理学的特性に関連する物質の有害反応、全PEの75%(コリン作動性拮抗薬使用時の口内乾燥、NSAID使用時の胃潰瘍)
タイプB:PE-免疫アレルギー性(予測不能)、25%。 用量に依存しないでください、繰り返し使用すると表示され、危険です。
タイプC:長時間の使用、特に不適切な使用による合併症。 薬物は、肝臓、腎臓、耳、神経などに毒性を及ぼし始めます。
タイプD: (遅延)-発がん性反応、変異原性反応、生殖系の欠陥。
薬物が胎児に及ぼす悪影響.
・胚毒性効果(1〜3週間):流産(アスピリン、バルビツール酸、代謝拮抗物質、スルホンアミド)を引き起こす未移植胚盤胞への損傷
・催奇形性(3〜10週間)-組織分化、発達障害、胎児が持続する場合がある(細胞増殖抑制剤、ホルモン、向精神薬)
・胎児毒性効果(3〜4か月)-精神発達の違反。
トピック: 末梢神経系の機能に影響を及ぼす医薬品。