بعض الأدوية تعزز أو تمنع نشاط إنزيمات معينة (داخل الخلايا أو خارج الخلية). يتم لعب الدور الرائد في ضمان وظائف الخلية عن طريق نظام سيكلز أدينيل العالمي من الخلايا ، ويرتبط تأثير العديد من الأدوية مع نشاط إنزيمات سيكلاز أدينيلات أو إنزيمات فسفودايستراز التي تنظم تركيز أحادي فوسفات أدينوسين دوري داخل الخلايا (cAMP).
يمكن للأدوية أن تحفز أو تمنع الإنزيمات ، تتفاعل معها بدرجات مختلفة ، بشكل معكوس أو لا رجعة فيه ، مما يؤثر على شدة ومدة التأثير الدوائي.
التأثير الفيزيائي الكيميائي للعقاقير على أغشية الخلايا
التأثير الفيزيائي الكيميائي على أغشية الخلايا هو تغيّر في إمكانات الغشاء الكهربائي نتيجة للتأثير على نقل الأيونات عبر غشاء الخلية. هذا مهم لنشاط خلايا الجهازين العصبي والعضلي: يتم تعطيل توصيل النبضات العصبية من خلال المشابك العصبية ، ويتم إعاقة النشاط الكهربائي للخلايا.
وبالتالي ، تعمل الأدوية المضادة لاضطراب النظم ومضادات الاختلاج وعوامل التخدير العام والتخدير الموضعي.
الآثار الكيميائية المباشرة (السامة للخلايا) للأدوية
يمكن أن تتفاعل الأدوية مباشرة مع جزيئات أو هياكل صغيرة داخل الخلايا ، مما يؤدي إلى تعطيل نشاط الخلايا.
الأدوية المضادة للبكتيريا والعوامل المضادة للفيروسات والخلايا لها تأثير مماثل.
قد لا يرتبط تأثير الأدوية بتغيير في وظائف الخلايا (على سبيل المثال ، تحييد حمض الهيدروكلوريك بمضادات الحموضة أو تأثير المسهلات الزيتية).
انتقائية المخدرات
يتم تحقيق انتقائية عمل المخدرات من خلال توزيع وتراكم الأدوية المختلفة في الأعضاء والأنسجة والخلايا وانتقائية آلية عملها.
الانتقائية هي القدرة على ممارسة تأثير معين معيّن ولا تتسبب في تأثيرات غير مرغوب فيها أخرى بسبب التأثير على الأنواع الفردية أو الأنواع الفرعية من المستقبلات. على سبيل المثال ، تعمل عوامل الحجب الأدرينالية met (الميتوبرولول ، الأتينولول) ، مضادات مستقبلات السيروتونين (الكيتانسيرين) على نوع فرعي محدد من المستقبلات المناظرة ، ولكن انتقائية مثل هذه الأدوية غالباً ما تكون نسبية ، مع زيادة في جرعة نفس عوامل الحجب الأدرينالية ، يمكن فقدانها جزئيًا. هناك طريقة أخرى لضمان الانتقائية النسبية لعمل الدواء وهي الإدارة الانتقائية لـ LF المطابق في موقع التأثير المطلوب (على سبيل المثال ، التدبير داخل النتروجليسرين للمرضى الذين يعانون من مرض الشريان التاجي).
لا توجد أدوية تعمل بشكل انتقائي على مستقبل معين أو عضو أو عملية مرضية. كلما زادت انتقائية الدواء ، زادت فعاليته.
تؤثر الأدوية ذات الانتقائية المنخفضة للعمل على العديد من الأنسجة والأعضاء والأجهزة ، مما يسبب العديد من ردود الفعل السلبية. كل دواء له طيف واسع أو أقل من الإجراءات ويمكن أن يسبب عددًا من ردود الفعل المرغوبة أو غير المرغوب فيها.
على سبيل المثال ، المورفين ، الذي له نشاط مسكن واضح ، ينتمي إلى مجموعة المسكنات المخدرة. ومع ذلك ، فإنه يمنع التنفس ، وقمع منعكس السعال ، له تأثير مهدئ ، يسبب القيء ، والإمساك ، تشنج قصبي ، وإطلاق الهستامين ، له تأثير مضاد لإدرار البول ، إلخ.
عوامل مضادات الأورام ، التي تعمل على الخلايا التي تنقسم بسرعة ، لا تلحق الضرر فقط بأنسجة الورم ، ولكن أيضًا في نخاع العظام ، وظهارة الأمعاء ، مما يؤدي إلى ردود فعل سلبية شديدة.
وكلما ارتفعت انتقائية عمل الأدوية ، كان المرضى يتحملون بشكل أفضل وانخفض عدد ردود الفعل السلبية التي يسببها.
مثال على ذلك هو حاصرات مستقبلات H2 من الجيل الثالث ، وموانع الكوليني ، ومثبطات H + ، K + -ATPase.
انتقائية الدواء يعتمد على جرعته. كلما كان ذلك أعلى ، كلما كان الدواء أقل انتقائية.
لذلك ، تؤثر حاصرات ad1 - الأدرينالية الانتقائية في الغالب على عضلة القلب ، ولكن مع زيادة الجرعة ، فإنها تؤثر أيضًا على مستقبلات ad 2 - الأدرينالية الموجودة في الشعب الهوائية والأوعية الدموية والبنكرياس والأعضاء الأخرى ، مما يؤدي إلى تطوير تفاعلات غير مرغوب فيها (تشنج قصبي ، تضيق الأوعية).
تعتمد انتقائية عمل الأدوية المضادة للفيروسات ، مثل الأسيكلوفير ، أيضًا على الجرعة: يحدث قمع بوليميريز الحمض النووي الفيروسي بتركيزات الدواء 3000 مرة أقل من تلك التي تؤثر على بوليميريز الحمض النووي للخلايا البشرية ، وبالتالي فإن الأسيكلوفير في الجرعات العلاجية غير سامة.
5. الإجراءات المحلية والإجرائية للأدوية. العمل المباشر والانعكاس. التنظيم وآلية العمل. أهداف للأدوية. العمل عكسها ولا رجعة فيه. عمل انتقائي
5. الإجراءات المحلية والإجرائية للأدوية. العمل المباشر والانعكاس. التنظيم وآلية العمل. أهداف للأدوية. العمل عكسها ولا رجعة فيه. عمل انتقائي
يُطلق على إجراء المادة التي تحدث في موقع تطبيقه محلي. على سبيل المثال ، تغطي العوامل المغلفة الغشاء المخاطي ، مما يمنع تهيج نهايات الأعصاب الوراثية. مع التخدير السطحي ، يؤدي تطبيق مخدر موضعي على الغشاء المخاطي إلى كتلة نهايات الأعصاب الحسية فقط في موقع تطبيق الدواء. ومع ذلك ، فإن التأثير المحلي الحقيقي نادر للغاية ، حيث يمكن إما امتصاص المواد جزئيًا أو بذلها تأثير المنعكس.
يسمى عمل المادة التي تتطور بعد امتصاصها ، والدخول إلى مجرى الدم العام ثم إلى الأنسجة ، resorptive 2. العمل الاستباقي
1 من الانجليزية تخليص- التنظيف.
2 من اللات. resorbeo- أنا أستوعب.
التأثير يعتمد على طريق الإدارة المخدرات وقدرتهم على عبور الحواجز البيولوجية.
من خلال الإجراءات المحلية والإحيائية ، يكون للعقاقير تأثير مباشر أو منعكس. يتم تحقيق الأول في مكان التلامس المباشر للمادة مع الأنسجة. مع التأثير المنعكس للمادة ، تؤثر exoeroles أو اعتراضية على التأثير ويظهر التأثير من خلال التغيير في حالة المراكز العصبية المقابلة أو الأجهزة التنفيذية. لذلك ، فإن استخدام الخردل في أمراض الجهاز التنفسي يعمل على تحسين رده الكأس (يحفز زيت الخردل الأساسي مستقبلات الجلد الخارجية). لوبيلين الدواء ، الذي يُعطى عن طريق الوريد ، له تأثير مثير على المستقبِلات الكيميائية للكبيبات السباتية ، وهو يحفز بشكل انعكاسي مركز التنفس ، ويزيد من حجم وتواتر التنفس.
تتمثل المهمة الرئيسية للديناميكا الدوائية في معرفة أين وكيف تعمل العقاقير ، مسببة تأثيرات معينة. بفضل تحسين التقنيات المنهجية ، يتم حل هذه المشكلات ليس فقط على مستوى الجهاز والعضوية ، ولكن أيضًا على المستويات الخلوية ودون الخلوية والجزيئية والجزيئية. لذلك ، بالنسبة للعقاقير العصبية ، يتم إنشاء تلك الهياكل في الجهاز العصبي والتي تكون للتكوينات التشابكية أعلى حساسية لهذه المركبات. بالنسبة للمواد التي تؤثر على التمثيل الغذائي ، يتم تحديد توطين الإنزيمات في الأنسجة والخلايا والتكوينات الخلوية المختلفة ، ويتغير نشاطها بشكل خاص. في جميع الحالات ، نحن نتحدث عن تلك الركائز البيولوجية ، "الأهداف" التي يتفاعل بها الدواء.
المستقبلات والقنوات الأيونية والإنزيمات وأنظمة النقل والجينات بمثابة "أهداف" للعقاقير.
المستقبلات هي مجموعات نشطة من الجزيئات الكبيرة من الركائز التي تتفاعل المادة. وتسمى المستقبلات التي توفر مظهر من عمل المواد محددة.
الأنواع الأربعة التالية من المستقبلات تتميز (الشكل.
1. المستقبلات التي تتحكم مباشرة في وظيفة القنوات الأيونية. يشتمل هذا النوع من المستقبلات المقترنة مباشرة بالقنوات الأيونية على مستقبلات n-cholinergic ، ومستقبلات GABA A ، ومستقبلات الجلوتامات.
II. المستقبلات مترافق مع المستجيب من خلال أجهزة الإرسال الثانوية G- البروتينات أو نظام قنوات G-proteinins-ion. تتوفر هذه المستقبلات للعديد من الهرمونات والوسطاء (مستقبلات m-cholinergic ، مستقبلات الأدرينالية).
III. المستقبلات التي تتحكم مباشرة في وظيفة إنزيم المستجيب. ترتبط مباشرة مع التيروزين كيناز وتنظيم فسفرة البروتين. وفقًا لهذا المبدأ ، يتم ترتيب مستقبلات الأنسولين ، وعدد من عوامل النمو.
IV. المستقبلات التي تتحكم في نسخ الحمض النووي. على عكس مستقبلات الغشاء من الأنواع I-III ، فهذه هي مستقبلات داخل الخلايا (البروتينات الخلوية القابلة للذوبان أو النووية). تتفاعل هرمونات الستيرويد والغدة الدرقية مع هذه المستقبلات.
أثبتت دراسة الأنواع الفرعية للمستقبلات (الجدول II.1) والآثار ذات الصلة أنها مثمرة للغاية. من بين الدراسات الأولى من هذا النوع كان العمل على تخليق العديد من حاصرات، ، والتي تستخدم على نطاق واسع في أمراض مختلفة من نظام القلب والأوعية الدموية. ثم ، ظهرت حاصرات مستقبلات الهيستامين H 2 ، فعالة في علاج قرحة المعدة وقرحة الاثني عشر. بعد ذلك ، تم تصنيعه
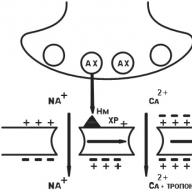
التين.مبادئ عمل منبهين على العمليات التي تسيطر عليها المستقبلات.
أنا - تأثير مباشر على نفاذية القنوات الأيونية (مستقبلات n-cholinergic ، مستقبلات GABA A) ؛ II - التأثير غير المباشر (عبر البروتينات G) على نفاذية القنوات الأيونية أو على نشاط الإنزيمات التي تنظم تكوين أجهزة الإرسال الثانوية (مستقبلات m-cholinergic ، مستقبلات الأدرينالية) ؛ III - تأثير مباشر على نشاط إنزيم مستقبلة التيروزين كيناز (مستقبلات الأنسولين ، مستقبلات عدد من عوامل النمو) ؛ IV - التأثير على نسخ الحمض النووي (هرمونات الستيرويد ، هرمونات الغدة الدرقية).
ولكن العديد من الأدوية الأخرى التي تعمل على أنواع فرعية مختلفة من مستقبلات ألفا الأدرينالية ، الدوبامين ، مستقبلات الأفيون ، إلخ. وقد لعبت هذه الدراسات دورًا كبيرًا في إنشاء مجموعات جديدة من الأدوية التي تعمل بشكل انتقائي والتي تستخدم على نطاق واسع في الممارسة الطبية.
بالنظر إلى تأثير المواد على مستقبلات ما بعد المشبك ، تجدر الإشارة إلى إمكانية الربط الخيفي للمواد على حد سواء (مثل الجليكاين) والخارجي (مثل مزيل القلق من سلسلة البنزوديازيبين ؛ انظر الفصل 11.4 ، الشكل 11.3) من المنشأ. تفاعل Allosteric 1 مع المستقبل لا يسبب "إشارة". ومع ذلك ، هناك تعديل لتأثير الوسيط الرئيسي ، والذي يمكن أن يزيد وينقص. إنشاء مواد من هذا النوع يفتح إمكانيات جديدة لتنظيم وظائف الجهاز العصبي المركزي. تتمثل إحدى ميزات أجهزة التحفيز العصبي للعمل الخيفي في أنها لا تؤثر بشكل مباشر على انتقال الوسيط الرئيسي ، ولكنها تعدلها فقط في الاتجاه المطلوب.
لعبت دورًا مهمًا لفهم آليات تنظيم انتقال التشابك العصبي بواسطة اكتشاف مستقبلات ما قبل المشبكي (الجدول II.2). تمت دراسة طرق التحسس الذاتي المتماثل (عمل الوسيط المفرز على مستقبلات ما قبل المشبكية من نفس النهايات العصبية) والتنظيم المتغاير (التنظيم قبل المشبكي بسبب وسيط آخر) لإطلاق الوسطاء ، مما جعل من الممكن إعادة تقييم ميزات عمل العديد من المواد. كانت هذه المعلومات أيضًا بمثابة أساس للبحث المستهدف عن عدد من الأدوية (على سبيل المثال ، برازوسين).
1 من اليونانية. ألوس- مختلف ، مختلف ، ستريو- المكاني.
الجدول II.1أمثلة على بعض المستقبلات وأنواعها الفرعية

يُشار إلى تقارب أي مادة لمستقبلات ، مما يؤدي إلى تكوين مجمع "مستقبلات المادة" بها ، بمصطلح "التقارب" 1. تدعى قدرة المادة عند التفاعل مع مستقبلات لتحفيزها والتسبب في تأثير معين النشاط الداخلي.
1 من اللات. affinis- عزيزة.
المواد التي ، عند التفاعل مع مستقبلات محددة ، تسبب تغييرات فيها تؤدي إلى تأثير بيولوجي ، تسمى منبهات 1 (لديهم أيضًا نشاط داخلي). يمكن أن يؤدي التأثير التحفيزي للناهض على المستقبلات إلى تنشيط أو تثبيط وظيفة الخلية. إذا تسبب ناهض يتفاعل مع المستقبلات في الحد الأقصى للتأثير ، فإنه يطلق عليه ناهض كامل. على النقيض من الأخير ، لا تسبب ناهضات جزئية تتفاعل مع نفس المستقبلات التأثير الأقصى. المواد التي ترتبط بالمستقبلات ولكنها لا تحفزها تسمى الخصوم 2. ليس لديهم أي نشاط داخلي (يساوي 0). تنجم آثارها الدوائية عن الخصومة مع بروابط داخلية (وسطاء ، هرمونات) ، وكذلك مع مواد منبه خارجية. إذا كانوا يشغلون المستقبلات نفسها التي يتفاعل بها منبهون ، فإننا نتحدث عنها الخصوم التنافسيةإذا - أجزاء أخرى من الجزيء الكبير التي لا تتعلق بمستقبلات معينة ، ولكن مترابطة مع ذلك ، ثم - الخصوم غير التنافسيين.عندما تكون مادة ما بمثابة ناهض على نوع فرعي من المستقبلات وكمضاد على آخر ، فإنها تُعتبر ناهضًا مضادًا. على سبيل المثال ، يعتبر البنتازوسين المسكن مضادًا لمستقبلات مستقبلات الأفيون μ ونافذة الأفيون.
يتم التفاعل بين مستقبلات المادة بسبب الروابط بين الجزيئات. واحدة من الروابط الأكثر دواما هو التساهمية. ومن المعروف عن عدد قليل من الأدوية (ألفا مانع الفينوكسي بنزين ، بعض العوامل المضادة للانفجار). أقل استقرارا هو الرابطة الأيونية على نطاق واسع بسبب التفاعل الكهربائي للمواد مع المستقبلات. هذا الأخير هو نموذجي لحاصرات العقدة ، وكلاء curariform ، أستيل. تلعب قوى فان دير فال دورًا مهمًا ، والتي تشكل أساس تفاعلات الكارهة للماء ، وكذلك روابط الهيدروجين (الجدول II.3).
الجدول II.3.أنواع تفاعل المواد مع المستقبلات

1 هذا يشير إلى تفاعل الجزيئات غير القطبية في وسط مائي. * 0.7 سعر حراري (3 كيلو جول) لكل مجموعة CH 2.
اعتمادًا على قوة الرابطة "لمستقبلات المواد" ، يتم التمييز بين الفعل القابل للانعكاس (خاصية معظم المواد) والذي لا رجعة فيه (عادة في حالة الرابطة التساهمية).
1 من اليونانية. agonistes- منافس (AGON- النضال).
2 من اليونانية. antagonisma- النضال ، التنافس (المضادة- ضد صراع بين شخصيات المسرحية- النضال).
إذا تفاعلت مادة ما فقط مع مستقبلات فريدة وظيفية لتوطين معين ولم تؤثر على مستقبلات أخرى ، عندئذٍ يعتبر عمل هذه المادة انتقائيًا. لذا ، فإن بعض العوامل الشبيهة بالكروية تمنع مستقبلات الكولين الصفائحية بشكل انتقائي ، مما يسبب استرخاء العضلات الهيكلية. في الجرعات التي لها تأثير عضلي حلقي ، يكون لها تأثير ضئيل على المستقبلات الأخرى.
أساس انتقائية العمل هو تقارب (تقارب) المادة للمستقبل. ويرجع ذلك إلى وجود مجموعات وظيفية معينة ، فضلاً عن التنظيم الهيكلي العام للمادة الأكثر ملاءمة للتفاعل مع هذا المستقبل ، أي تكاملها. في كثير من الأحيان ، يتم استبدال مصطلح "الإجراء الانتقائي" لسبب وجيه بمصطلح "الإجراء التفضيلي" ، لأن الانتقائية المطلقة لعمل المواد غير موجودة عملياً.
عند تقييم تفاعل المواد مع مستقبلات الغشاء التي تنقل إشارة من السطح الخارجي للغشاء إلى الداخل ، من الضروري أيضًا مراعاة تلك الروابط الوسيطة التي تربط المستقبِل بالمستجيب. أهم مكونات هذا النظام هي البروتينات G-1 ، وهي مجموعة من الإنزيمات (سيكلز أدينيلات ، سيكلياز جوانييلات ، فسفوليباز C) وأجهزة إرسال ثانوية (cAMP ، cGMP ، IF 3 ، DAG ، Ca 2+). تؤدي الزيادة في تكوين أجهزة الإرسال الثانوية إلى تنشيط كينيات البروتين ، والتي توفر الفسفرة داخل الخلايا من البروتينات التنظيمية المهمة وتطور التأثيرات المختلفة.
يمكن أن تكون معظم الروابط في هذه السلسلة المعقدة هي نقطة التطبيق لعمل المواد الدوائية. ومع ذلك ، لا تزال هذه الأمثلة محدودة للغاية. بالنسبة إلى البروتينات G ، من المعروف أن السموم فقط هي التي ترتبط بها. مع زالصورة تفاعل بروتين الكوليرا بالضمة الدهنية مع Gأنا - البروتين - سم لعصي السعال الديكي.
هناك مواد فردية تؤثر بشكل مباشر على الإنزيمات المشاركة في تنظيم التخليق الحيوي للمرسلات الثانوية. لذلك ، ديتربين من أصل النبات forskolin ، المستخدمة في الدراسات التجريبية ، ويحفز cyclase أدينيلات (تأثير مباشر). يثبط فسفوديستريز الميثيل زانتين. في كلتا الحالتين ، يرتفع تركيز cAMP داخل الخلية.
واحدة من "الأهداف" المهمة لعمل المواد هي القنوات الأيونية. يرتبط التقدم في هذا المجال إلى حد كبير بتطوير طرق لتسجيل وظيفة القنوات الأيونية الفردية. لم يحفز هذا البحث الأساسي فقط على حركية العمليات الأيونية ، ولكنه ساهم أيضًا في خلق أدوية جديدة تنظم التيارات الأيونية (الجدول II.4).
بالفعل في منتصف القرن العشرين ، وجد أن أدوية التخدير الموضعي تحظر قنوات Na + التي تعتمد على الإمكانات. تشمل حاصرات قنوات Na + العديد من الأدوية المضادة لاضطراب النظم. بالإضافة إلى ذلك ، فقد تبين أن هناك عددًا من الأدوية المضادة للصرع (الديفينين ، كاربامازيبين) تمنع أيضًا قنوات Na + التي تعتمد على الإمكانات ويرتبط نشاطها المضاد للاختلاج على ما يبدو بهذا.
1 أنواع بعض البروتينات G ووظائفها: G S - اقتران مستقبلات الإثارة مع cyclase adenylate ؛ G i - اقتران مستقبلات المثبطة مع cyclase adenylate؛ G o - اقتران المستقبلات بقنوات الأيونات (التيار المخفض Ca 2+) ؛ Gف- اقتران المستقبلات التي تنشط فسفوليباز C ؛ تتكون البروتينات G من 3 وحدات فرعية - α و β و γ.
الجدول II.4.وسائل تؤثر على القنوات الأيونية

في السنوات الثلاثين إلى الأربعين الماضية ، تم إيلاء اهتمام كبير لحاصرات القناة Ca 2+ ، والتي تعطل دخول أيونات Ca 2+ إلى الخلية من خلال قنوات Ca 2+ المعتمدة على الجهد. يرجع الاهتمام المتزايد بهذه المجموعة من المواد إلى حد كبير إلى حقيقة أن أيونات Ca 2+ تشارك في العديد من العمليات الفسيولوجية: تقلص العضلات ، النشاط الإفرازي للخلايا ، انتقال العصب العضلي ، وظيفة الصفائح الدموية ، إلخ.
العديد من الأدوية في هذه المجموعة كانت فعالة للغاية في علاج أمراض شائعة مثل الذبحة الصدرية وعدم انتظام ضربات القلب وارتفاع ضغط الدم الشرياني. عقاقير معترف بها على نطاق واسع مثل فيراباميل ، ديلتيازيم ، فينيجدين وغيرها الكثير.
تجذب منشطات قنوات Ca 2+ ، على سبيل المثال ، مشتقات ديهيدروبيريدين ، الانتباه أيضًا. يمكن استخدام هذه المواد كأدوات للقلب ، وعوامل تضيق الأوعية ، والمواد التي تحفز إفراز الهرمونات والوسطاء ، فضلاً عن منشطات الجهاز العصبي المركزي.
من الأمور ذات الأهمية الخاصة البحث عن حاصرات ومنشطات Ca 2+ التي لها تأثير سائد على القلب والأوعية الدموية في مناطق مختلفة (المخ والقلب وما إلى ذلك) والجهاز العصبي المركزي. هناك بعض المتطلبات المسبقة لهذا ، لأن قنوات Ca 2+ غير متجانسة.
في السنوات الأخيرة ، جذبت المواد التي تنظم وظيفة قنوات K + اهتمامًا كبيرًا. تبين أن قنوات البوتاسيوم متنوعة للغاية في خصائصها الوظيفية. من ناحية ، يؤدي هذا إلى تعقيد الدراسات الدوائية بشكل كبير ، ومن ناحية أخرى ، فإنه يخلق متطلبات مسبقة حقيقية للبحث عن المواد الفعالة بشكل انتقائي. كل من المنشطات وحاصرات قناة البوتاسيوم معروفة.
يساهم منشطو قنوات البوتاسيوم في فتحها وإطلاق أيونات K + من الخلية. إذا حدث هذا في العضلات الملساء ، يتطور فرط الاستقطاب في الغشاء وينخفض \u200b\u200bلون العضلات. بفضل هذه الآلية ، يتم استخدام المينوكسيديل والديازوكسيد كعوامل مضادة لارتفاع ضغط الدم ، وكذلك عقار نيكورانديل المضاد للذبحة الصدرية.
تعتبر حاصرات قنوات البوتاسيوم ذات أهمية مثل الأدوية المضادة لاضطراب النظم (الأميودارون ، الأورنييد ، السوتالول).
حاصرات قنوات البوتاسيوم المعتمدة على ATP في البنكرياس تزيد من إفراز الأنسولين. وفقًا لهذا المبدأ ، تعمل الأدوية المضادة لمرض السكر من مجموعة السلفونيل يوريا (كلوربروباميد ، بوتاميد ، إلخ).
يرتبط التأثير المنبه للأمينوبيريدين على الجهاز العصبي المركزي والانتقال العصبي العضلي أيضًا بتأثيرها المعوق على قنوات البوتاسيوم.
وبالتالي ، فإن التعرض للقنوات الأيونية يكمن وراء آثار الأدوية المختلفة.
الإنزيمات هي "هدف" مهم لعمل المواد. لقد تم بالفعل الإشارة إلى إمكانية التعرض للإنزيمات التي تنظم تكوين المرسلات الثانوية (على سبيل المثال ، cAMP). لقد ثبت أن آلية عمل الأدوية المضادة للالتهابات غير الستيرويدية ناتجة عن تثبيط إنزيمات الأكسدة الحلقية وانخفاض في التخليق الحيوي للبروستاغلاندين. تستخدم مثبطات الإنزيم المحول للأنجيوتنسين (كابتوبريل وغيرها) كعوامل خافضة للضغط. عوامل مضادات الكولين التي تسد أستيل كولينستريز وتثبط أستيل كولين معروفة جيداً.
يقوم العامل المضاد للانفجار الميثوتريكسيت (مضادات حمض الفوليك) بعرقلة إنزيم ثنائي هيدروفولات ، ويمنع تكوين رباعي هيدروفولات ، وهو أمر ضروري لتخليق نيوكليوتيدات البيورين ، الثيميدات. إن عقار الأسيكلوفير المضاد للحك ، الذي يتحول إلى ثلاثي أسفات الفوسفات ، يمنع البلمرة الحمض النووي الفيروسي.
هناك "هدف" محتمل آخر لعمل المخدرات وهو أنظمة نقل الجزيئات القطبية والأيونات والجزيئات المحبة للماء. وتشمل هذه ما يسمى بروتينات النقل التي تحمل المواد عبر غشاء الخلية. لديهم مواقع الاعتراف للمواد الداخلية. هذه المواقع يمكن أن تتفاعل مع المخدرات. لذلك ، تمنع مضادات الاكتئاب ثلاثية الحلقات امتصاص الخلايا العصبية من بافراز. ريزيربين كتل ترسب بافراز في الحويصلات. أحد الإنجازات المهمة هو إنشاء مثبطات مضخة البروتون في الغشاء المخاطي في المعدة (أوميبرازول ، إلخ) ، والتي ثبت أنها فعالة للغاية في قرحة المعدة والاثني عشر ، وكذلك في التهاب المعدة المفرط الحموضة.
في الآونة الأخيرة ، فيما يتعلق بفك تشفير الجينوم البشري ، أجريت دراسات مكثفة تتعلق باستخدام كهدف الجينات.لا شك في ذلك العلاج الجينيهي واحدة من أهم مجالات الصيدلة الحديثة والمستقبلية. فكرة هذا العلاج هي تنظيم وظيفة الجينات التي ثبت دورها المسببة للأمراض الوراثية. المبادئ الأساسية للعلاج الجيني هي زيادة أو تقليل أو إيقاف التعبير الجيني ، وكذلك لاستبدال الجينات المتحولة.
أصبح حل هذه المشكلات حقيقيًا بفضل القدرة على استنساخ السلاسل بتسلسل معين من النيوكليوتيدات. ويهدف إدخال هذه السلاسل المعدلة إلى تطبيع تخليق البروتينات التي تحدد هذه الحالة المرضية ، وبالتالي استعادة وظيفة الخلايا الضعيفة.
تتمثل المشكلة الرئيسية في التطور الناجح للعلاج الجيني في توصيل الأحماض النووية إلى الخلايا المستهدفة. يجب أن تدخل الأحماض النووية إلى البلازما من مسافات خارج الخلية ، وبعد ذلك تمر عبر أغشية الخلايا ، وتخترق النواة وتندمج في الكروموسومات. يُقترح استخدام بعض الفيروسات (على سبيل المثال ، الفيروسات القهقرية ، الفيروسات الغدانية) كناقلات ، أو ناقلات. علاوة على ذلك ، وبمساعدة الهندسة الوراثية ، تفقد فيروسات المتجهات قدرتها على التكاثر ، أي لا تشكلت virions منها. تم اقتراح أنظمة نقل أخرى - معقدات الحمض النووي مع الجسيمات الشحمية ، والبروتينات ، والحمض النووي البلازميد ، وغيرها من الجسيمات المجهرية والمجهرية.
بطبيعة الحال ، يجب أن يعمل الجين المدمج لفترة طويلة بما فيه الكفاية ، أي يجب أن يكون التعبير الجيني ثابتًا.
العلاج الجيني المحتمل يتعلق بالكثير من الأمراض الموروثة. ويشمل ذلك حالات نقص المناعة ، وبعض أنواع أمراض الكبد (بما في ذلك الهيموفيليا) ، وأمراض الهيموغلوبين ، وأمراض الرئة (مثل التليف الكيسي) ، والأنسجة العضلية (ضمور دوشين العضلي) ، إلخ.
الأبحاث جارية على جبهة واسعة لتوضيح الطرق المحتملة لاستخدام العلاج الجيني لعلاج أمراض الورم. هذه الاحتمالات هي لمنع التعبير عن البروتينات المسرطنة. في تفعيل الجينات القادرة على تثبيط نمو الورم ؛ في تحفيز تكوين إنزيمات خاصة في الأورام التي تحول العقاقير الأولية إلى مركبات سامة فقط لخلايا الورم ؛ زيادة مقاومة خلايا نخاع العظم للتأثير المثبط للعوامل المضادة للانفجار ؛ تعزيز المناعة ضد الخلايا السرطانية ، إلخ.
في الحالات التي يصبح فيها من الضروري منع التعبير عن جينات معينة ، يتم استخدام تقنية خاصة لمادة أوليجنوكليوتيدات مضادة للتأثير (أنتيسنس). هذه الأخيرة عبارة عن سلاسل قصيرة نسبيًا من النيوكليوتيدات (من 15 إلى 25 قاعدة) والتي تعد مكملة لمنطقة الحمض النووي حيث يوجد الجين المستهدف. نتيجة للتفاعل مع قليل النوكليوتيد المضاد للفيروسات ، يتم قمع التعبير عن هذا الجين. هذا المبدأ للعمل هو مصلحة في علاج الأمراض الفيروسية والورم وغيرها. يتم تطبيق أول دواء من مجموعة النيوكليوتيدات المضادة للفيروسات ، فيترافن (fomivirsen) ، موضعياً على التهاب الشبكية الناجم عن عدوى الفيروس المضخم للخلايا. يبدو أن هذا النوع من المخدرات يعالج سرطان الدم النخاعي وأمراض الدم الأخرى. إنهم يخضعون لتجارب سريرية.
حاليا ، مشكلة استخدام الجينات كأهداف للتأثيرات الدوائية هي بشكل رئيسي في مرحلة البحث الأساسي. فقط عدد قليل من المواد الواعدة من هذا النوع تخضع لتجارب سريرية أولية وأولية. ومع ذلك ، ليس هناك شك في أنه في هذا القرن ستظهر العديد من الوسائل الفعالة لعلاج الجينات ليس فقط من الأمراض الوراثية ، ولكن أيضًا الأمراض المكتسبة. ستكون هذه أدوية جديدة في الأساس لعلاج الأورام ، والأمراض الفيروسية ، ونقص المناعة ، واضطرابات الدم وتخثر الدم ، وتصلب الشرايين ، إلخ.
من السهل تقديم عملك الجيد إلى قاعدة المعرفة. استخدم النموذج أدناه
الطلاب وطلاب الدراسات العليا والعلماء الشباب الذين يستخدمون قاعدة المعرفة في دراساتهم وأعمالهم سيكونون ممتنين للغاية لك.
نشر على http://www.allbest.ru/
GOU VPO "أكاديمية نيجني نوفغورود الطبية الحكومية التابعة لوزارة الصحة والتنمية الاجتماعية في الاتحاد الروسي"
قسم الصيدلة العامة والسريرية
عمل المخدرات
1. الآثار المحلية و resorptive من المخدرات
يُطلق على إجراء المادة التي تحدث في موقع تطبيقه محلي. على سبيل المثال ، تغطي العوامل المغلفة الغشاء المخاطي ، مما يمنع تهيج نهايات الأعصاب الواعية. مع التخدير السطحي ، يؤدي تطبيق مخدر موضعي على الغشاء المخاطي إلى كتلة نهايات الأعصاب الحسية فقط في موقع تطبيق الدواء. ومع ذلك ، فإن التأثير المحلي الحقيقي نادر للغاية ، حيث يمكن إما امتصاص المواد جزئيًا أو يكون لها تأثير منعكس.
يسمى عمل المادة التي تتطور بعد امتصاصها ، والدخول إلى مجرى الدم العام ثم إلى الأنسجة ، resorptive. يعتمد التأثير الاستعادي على طريق إعطاء الأدوية وقدرتها على اختراق الحواجز البيولوجية.
2. العمل المباشر ورد الفعل
من خلال الإجراءات المحلية والإحيائية ، يكون للعقاقير تأثير مباشر أو منعكس. يتم تحقيق الأول في مكان التلامس المباشر للمادة مع الأنسجة. مع التأثير المنعكس ، تؤثر المواد على المستقبلات الخارجية أو المتداخلة ويتجلى التأثير من خلال التغيير في حالة المراكز العصبية المقابلة أو الأجهزة التنفيذية. لذلك ، فإن استخدام الخردل في أمراض الجهاز التنفسي يعمل على تحسين رده الكأس بشكل طبيعي (يعمل زيت الخردل الأساسي على تنشيط مستقبلات الجلد الخارجية). لوبيلين الدواء ، الذي يُعطى عن طريق الوريد ، له تأثير مثير على المستقبِلات الكيميائية للكبيبات السباتية ، وهو يحفز بشكل انعكاسي مركز التنفس ، ويزيد من حجم وتواتر التنفس.
عكسها الديناميكا الدوائية الانتقائية المخدرات
3. توطين وآلية العمل
تتمثل المهمة الرئيسية للديناميكا الدوائية في معرفة أين وكيف تعمل العقاقير ، مسببة تأثيرات معينة. بفضل تحسين التقنيات المنهجية ، يتم حل هذه المشكلات ليس فقط على مستوى الجهاز والعضوية ، ولكن أيضًا على المستويات الخلوية ودون الخلوية والجزيئية والجزيئية. لذلك ، بالنسبة للعقاقير العصبية ، يتم إنشاء تلك الهياكل من الجهاز العصبي الذي يكون للتكوينات متشابك أعلى حساسية لهذه المركبات. بالنسبة للمواد التي تؤثر على التمثيل الغذائي ، يتم تحديد توطين الإنزيمات في الأنسجة والخلايا والتكوينات الخلوية المختلفة ، ويتغير نشاطها بشكل خاص. في جميع الحالات ، نحن نتحدث عن تلك الركائز البيولوجية ، "الأهداف" التي يتفاعل بها الدواء.
4. "أهداف" للمخدرات
تعتبر المستقبلات والقنوات الأيونية والإنزيمات وأنظمة النقل والجينات بمثابة "أهداف" للعقاقير.
المستقبلات هي مجموعات نشطة من الجزيئات الكبيرة من الركائز التي تتفاعل المادة. وتسمى المستقبلات التي توفر مظهر من عمل المواد محددة.
الأنواع الأربعة التالية من المستقبلات تتميز (الشكل.
1. المستقبلات التي تتحكم مباشرة في وظيفة القنوات الأيونية. يتضمن هذا النوع من المستقبلات المقترنة مباشرة بالقنوات الأيونية مستقبلات n-cholinergic ، ومستقبلات GABAA ، ومستقبلات الجلوتامات.
II. المستقبلات مترافق مع المستجيب من خلال أجهزة الإرسال الثانوية G- البروتينات أو نظام قنوات G-proteinins-ion. تتوفر هذه المستقبلات للعديد من الهرمونات والوسطاء (مستقبلات m-cholinergic ، مستقبلات الأدرينالية).
III. المستقبلات التي تتحكم مباشرة في وظيفة إنزيم المستجيب. ترتبط مباشرة مع التيروزين كيناز وتنظيم فسفرة البروتين. وفقًا لهذا المبدأ ، يتم ترتيب مستقبلات الأنسولين ، وعدد من عوامل النمو.
IV. المستقبلات التي تتحكم في نسخ الحمض النووي. على عكس مستقبلات الغشاء من الأنواع I-III ، فهذه هي مستقبلات داخل الخلايا (البروتينات الخلوية القابلة للذوبان أو النووية). تتفاعل هرمونات الستيرويد والغدة الدرقية مع هذه المستقبلات.
بالنظر إلى تأثير المواد على مستقبلات ما بعد المشبك ، تجدر الإشارة إلى إمكانية الربط الخيفي للمواد ذات المنشأ الداخلي (مثل الجليكاين) والأصل الخارجي (على سبيل المثال ، مزيلات القلق من سلسلة البنزوديازيبين). تفاعل التآثر مع المستقبل لا يسبب "إشارة". ومع ذلك ، هناك تعديل لتأثير الوسيط الرئيسي ، والذي يمكن أن يزيد وينقص. إنشاء مواد من هذا النوع يفتح إمكانيات جديدة لتنظيم وظائف الجهاز العصبي المركزي. تتمثل إحدى ميزات أجهزة التحفيز العصبي للعمل الخيفي في أنه ليس لها تأثير مباشر على انتقال الوسيط الرئيسي ، ولكن تعديله فقط في الاتجاه المطلوب.
لعبت دورا هاما لفهم آليات تنظيم انتقال متشابك من خلال اكتشاف مستقبلات قبل المشبكي. تمت دراسة طرق التحفيز الذاتي الذاتي (عمل الوسيط المفرز على مستقبلات ما قبل المشبكية ذات النهاية العصبية نفسها) والتنظيم المتغاير (التنظيم قبل المشبكي بسبب وسيط آخر) لإطلاق الوسطاء ، مما جعل من الممكن إعادة تقييم ميزات عمل العديد من المواد. كانت هذه المعلومات أيضًا بمثابة أساس للبحث المستهدف عن عدد من الأدوية (على سبيل المثال ، برازوسين).
يشار مصطلح تقارب أي مادة لمستقبلات ، مما يؤدي إلى تشكيل مجمع "مستقبلات المواد" معها ، بمصطلح "تقارب". تدعى قدرة المادة عند التفاعل مع مستقبلات لتحفيزها والتسبب في تأثير معين النشاط الداخلي.
5. عكسها والعمل لا رجعة فيه. عمل انتقائي
اعتمادًا على قوة الرابطة "لمستقبلات المواد" ، يتم التمييز بين الفعل القابل للانعكاس (خاصية معظم المواد) والذي لا رجعة فيه (عادة في حالة الرابطة التساهمية).
إذا تفاعلت مادة ما فقط مع مستقبلات فريدة وظيفية لتوطين معين ولم تؤثر على مستقبلات أخرى ، عندئذٍ يعتبر عمل هذه المادة انتقائيًا. لذا ، فإن بعض العوامل الشبيهة بالكروية تحجب بشكل انتقائي مستقبلات الكولين الصفائح النهائية ، مما يؤدي إلى استرخاء العضلات الهيكلية. في الجرعات التي لها تأثير عضلي حلقي ، يكون لها تأثير ضئيل على المستقبلات الأخرى.
أساس انتقائية العمل هو تقارب (تقارب) المادة للمستقبل. ويرجع ذلك إلى وجود مجموعات وظيفية معينة ، وكذلك التنظيم الهيكلي العام للمادة الأكثر ملاءمة للتفاعل مع هذا المستقبل ، أي تكاملها. في كثير من الأحيان ، يتم استبدال مصطلح "الإجراء الانتقائي" لسبب وجيه بمصطلح "الإجراء التفضيلي" ، لأن الانتقائية المطلقة لعمل المادة غير موجودة عملياً.
نشر على Allbest.ru
وثائق مماثلة
التأثير المشترك للعقاقير. الفيتامينات K ، E ، B2 ، B6 ، C ، P: الدور البيولوجي ، المؤشرات. الوسائل التي تنظم وظيفة تقلص الرحم: تصنيف وآلية العمل. العوامل المضادة للفرط ومضادات الفيروسات.
اختبار ، تمت إضافة 09/13/2011
أنواع الأهداف الجزيئية للعمل الدوائي. تأثير الايزومرية البصرية على النشاط البيولوجي للأدوية المضادة للالتهابات غير الستيرويدية. الايزومرية الهندسية. تأثير الايزومرية الهندسية على عملها الدوائي.
تمت إضافة ورقة مصطلح 11/20/2013
الترميز الرقمي للأدوية. تأثير العوامل المختلفة على خصائص المستهلك وجودة الأدوية وطرق حماية البضائع في مراحل دورة الحياة. الدوائية العمل ، المؤشرات المخدرات بناء على chaga.
ورقة المصطلح ، تمت الإضافة بتاريخ 28/12/2011
تعريف وتاريخ ظهور العقاقير منشط الذهن ، وتصنيفها وفقا لآلية العمل والبنية الكيميائية. آلية العمل والآثار الرئيسية للأدوية منشط الذهن. فعالية استخدام هذه الأدوية في الممارسة الطبية.
الخلاصة ، تمت إضافة 12/12/2012
السمة العامة للفطريات. تصنيف الأدوية المضادة للفطريات. مراقبة جودة الأدوية المضادة للفطريات. مشتقات الإيميدازول والتريازول والمضادات الحيوية من البولين والأليلامين. آلية عمل العوامل المضادة للفطريات.
ورقة المصطلح ، تمت إضافة 10/14/2014
الديناميكا الدوائية باعتبارها واحدة من الفروع الأساسية لعلم الصيدلة. الفرق بين الآثار الرئيسية والجانبية للعقاقير. دور الروابط الأيونية في آلية عمل المخدرات. تحديد الفهرس العلاجي. تأثير العوامل الخارجية على تفاعل الدواء.
الخلاصة ، تمت إضافة 07/28/2010
تصنيف مجموعة العقاقير الدوائية ، آلية العمل والديناميكا الدوائية ، آثار جانبية، أشكال الإفراج والجرعات ، الملامح الدوائية للأدوية: حمض الصفصاف (الأسبرين) ، سيبروفلوكساسين ، فورموتيرول.
اختبار العمل ، أضيفت في 12/22/2015
الأهداف الرئيسية لعلم الصيدلة: إنشاء الأدوية ؛ دراسة آليات عمل المخدرات ؛ دراسة الديناميكا الدوائية والحرائك الدوائية للعقاقير في التجربة والممارسة السريرية. علم الأدوية من الأدوية سينوبوتروبيك.
وأضاف العرض 04/08/2013
تاريخ اكتشاف المضادات الحيوية. وصف الدوائية من العوامل المضادة للبكتيريا من العمل الانتقائي وغير الانتقائي كأشكال من المخدرات. مبادئ العلاج الكيميائي العقلاني وخصائص العوامل العلاجية المضادة للميكروبات.
عرض ، تمت إضافته في 04/28/2015
العلاج الدوائي - التعرض المواد الطبية - على أساس استخدام مجموعات من الأدوية ، وتكوين عمل الأعراض لديهم. تفاعل الأدوية: الفيزيائية والكيميائية والحركية الدوائية والدوائية الديناميكية.