Farmakodinamika
Farmakodinamika yra bendrosios farmakologijos dalis, tirianti vaistų veikimo organizme ypatumus. Būtent farmakodinamikos tyrimai:
narkotikų veikimo mechanizmai;
galutinis farmakologinis poveikis;
narkotikų veikimo priklausomybė nuo įvairių sąlygų;
narkotikų poveikis pakartotinai vartojant;
kombinuotas narkotikų veikimas;
vaistų nesuderinamumas;
šalutinis poveikis vaistinės medžiagos.
Vaistų veikimo mechanizmai yra būdai, kuriais medžiagos sukelia farmakologinį poveikį. Pagrindiniai narkotikų veikimo mechanizmai yra šie:
Fizinis.
Tiesioginės cheminės sąveikos mechanizmas.
Membranos (fizikiniai ir cheminiai).
Fermentinis (biocheminis).
Receptorius.
Tiesioginė cheminė sąveika. Tai gana retas vaistų veikimo mechanizmas, kurio esmė ta, kad vaistai tiesiogiai sąveikauja su organizmo molekulėmis ar jonais. Tokį veikimo mechanizmą turi, pavyzdžiui, unitiolis, priklausantis priešnuodžių grupei. Apsinuodijus tiolio nuodais, įskaitant sunkiųjų metalų druskas, unitiolis pradeda tiesioginę cheminę reakciją su jais, todėl susidaro netoksiški kompleksai, kurie išsiskiria su šlapimu. Taigi taip pat veikia antacidai, kurie tiesiogiai jungiasi su druskos rūgštimi, mažindami skrandžio sulčių rūgštingumą.
Membranos (fizikiniai ir cheminiai) mechanizmas. Tai siejama su vaistų poveikiu jonų srovėms (Na +, K +, Cl - ir kt.), Nuo kurių priklauso transmembraninis elektrinis potencialas. Pagal šį mechanizmą naudojami anestetikai, antiaritminiai vaistai, vietiniai anestetikai ir kt.
Fermentinis (biocheminis) mechanizmas. Šį mechanizmą lemia kai kurių vaistų gebėjimas aktyvuoti ar slopinti fermentus. Narkotikų, turinčių tokį veikimo mechanizmą, arsenalas yra labai platus. Pavyzdžiui, anticholinesterazės vaistai, monoaminooksidazės inhibitoriai, protonų siurblio blokatoriai ir kt.
Receptorių mechanizmas. Žmogaus kūne yra labai specifinių biologiškai aktyvių medžiagų (mediatorių), kurios sąveikauja su receptoriais ir keičia įvairių kūno organų ar audinių funkcijas.
Receptoriai yra makromolekulinės struktūros, turinčios selektyvų jautrumą tam tikriems cheminiams junginiams. Vaistams sąveikaujant su receptoriais, atsiranda biocheminių ir fiziologinių pokyčių organizme, kuriuos lydi vienas ar kitas klinikinis poveikis.
Vadinami mediatoriai ir vaistai, kurie aktyvina receptorius ir sukelia biologinį poveikį agonistai. Vaistinės medžiagos, kurios jungiasi su receptoriais, tačiau nesukelia jų aktyvacijos ir biologinio poveikio, mažina arba panaikina agonistų poveikį, vadinamos antagonistai. Paskirstykite taip pat antagonistų agonistai - medžiagos, kurios skirtingai veikia tų pačių receptorių potipius: stimuliuoja vienus receptorių potipius, o kitus blokuoja. Pvz., Narkotinis analgetikas nalufinas stimuliuoja opioidų kappa receptorius (todėl mažina jautrumą skausmui) ir blokuoja opioidų mu receptorius (todėl yra mažiau pavojingas priklausomybės nuo narkotikų atžvilgiu).
Medžiagų gebėjimas jungtis prie receptorių yra minimas terminu „giminingumas“. Tų pačių receptorių atžvilgiu skirtingų medžiagų afinitetas gali būti skirtingas.
Skiriami šie receptorių tipai:
Plazminės membranos receptoriai:
kanalo tipas: N tipo cholinerginiai receptoriai, raumenų tipo H cholinerginiai receptoriai, GABA receptoriai;
g-baltymų receptoriai: α- ir β-adrenerginiai receptoriai, M 3 -cholinoreceptoriai;
integracinio tipo receptoriai: NO receptorių.
Citozolinis.
Mitochondrijos.
Branduolinė
Kanalo tipo receptoriai
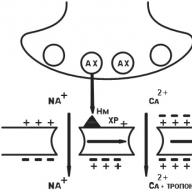
N n nervo tipo cholinerginiai receptoriai (CNS, autonominės ganglijos, sinokarotidinė zona, chromaffino antinksčių audiniai). Prijungus acetilcholinui (AX) su Hn-cholinerginiais receptoriais, Na + kanalai atsidaro ir Na bėga į ląstelę, turėdama teigiamą krūvį. Postinapsinė membrana depoliarizuota. Yra veikimo potencialas, kuris pasislenka išilgai neurono membranos, atverdamas elektriškai priklausomus Na + kanalus. Postganglioniniame pluošte atsiranda nervinis impulsas (6 pav.).
Fig. 6. N n-cholinerginiai receptoriai
N m raumenų tipo cholinerginiai receptoriai (skeleto raumenų ląstelių membranos). Pradiniai procesai yra panašūs, tačiau atidaromi nuo elektrinių priklausomi Ca ++ kanalai. Ca ++ jonai patenka į raumenų skaidulą, Ca ++ išsiskiria iš sarkoplazminio retikulumo. Ca ++ lygis pakyla, o tai sukelia raumenų susitraukimą (7 pav.).

Fig. 7. N m-cholinerginiai receptoriai
GABA receptoriai. Tai yra γ-aminosviesto rūgšties (GABA) receptoriai. GABA sąveikauja su GABA receptoriais, kurių struktūroje yra chlorido kanalai. Dėl receptorių stimuliacijos atsidaro kanalai ir chloro jonai (Cl -) laisvai patenka į ląstelę. Chloro jonų koncentracijos padidėjimas ląstelės viduje lemia membranos hiperpolarizaciją ir neuronų aktyvumo sumažėjimą. Tokią ląstelę sunkiau sužadinti (8 pav.).
 Fig. 8. GABA receptoriai:
Fig. 8. GABA receptoriai:
GABA-R - GABA receptorius, BD-R - benzodiazepino receptorius, BR - barbitūratų receptorius
Receptorių, susijusių su G baltymai
G baltymai, t. Y. GTP jungiantys (guanozino trifosfatą surišantys) baltymai yra lokalizuoti ląstelės membranoje ir susideda iš α-, β- ir γ-subvienetų. Jie (G-baltymai) reguliuoja specifinių efektorių (momentinių pasiuntinių, antrinių tarpininkų) veiklą. Šie pasiuntiniai gali būti enzimai (adenilato ciklazė, fosfolipazė); kalio, kalcio, natrio kanalai; kai kurie transportiniai baltymai. Kiekviena ląstelė gali turėti daug G baltymų, kiekviena iš jų reguliuoja įvairių pasiuntinių veiklą, tuo pačiu keisdama ląstelės funkciją.
M 3 cholinerginiai receptoriai (lygiųjų raumenų membranos (MMC) ir egzokrininės liaukos ląstelės). Acetilcholinas stimuliuoja M3-XR, sujungtą su G baltymu. Suaktyvinamas fosfolipazė-C (FLS), kuris katalizuoja PIDP (fosfatidilinozitolio difosfato) skilimą į ITP (inozitolio trifosfatą) ir DAG (diacilglicerolį). ITF, patekęs į MMC citoplazmą, išskiria Ca ++ iš urvelių .

Fig. 9. M 3 -cholinerginiai receptoriai
Ca ++ jungiasi su kalmodulinu, aktyvina miozino kinazę (MK), kuri katalizuoja miozino lengvųjų grandinių fosforilinimąsi, kuris lemia ląstelių susitraukimą (9 pav.) .Taip pat impulsas perduodamas sekretorinių liaukų sinapsėse.
Norepinefrinas stimuliuoja α 1 adrenoreceptoriusPradėjus šią įvykių grandinę:
Norepinefrinas (HA) → α 1 -adrenoreceptorius → G s-baltymo α-subvienetų aktyvinimas → FLS aktyvinimas → PIDF skilimas → ITF koncentracijos padidėjimas → Ca 2+ koncentracijos padidėjimas ląstelėje → Ca 2+ jungiasi su kalmodulinu → aktyvuota miozino kinazė → fosforiluojasi šviesos grandinės miozinas → miozinas sąveikauja su aktinu → išsivysto MMC sumažėjimas (10 pav.).

Fig. 10. α 1 -adrenoreceptorius
1 receptorius(11 pav.). Norepinefrinas → suaktyvina 1 -AP → suaktyvina G-baltymo α-subvienetą → suaktyvina AC → padidina cAMP susidarymą iš ATP → padidina cAMP koncentraciją kardiomiocituose → suaktyvina baltymų kinazes → fosforilina kalcio kanalų baltymus → padidina Ca 2+ patekimą per kanalus ir padidina Ca koncentraciją 2+ ląstelėje → padidėja širdies susitraukimų jėga.

Fig. 11. 1 receptorius
2 receptorius(12 pav.). ĮJUNGTA → 2-AR → G-baltymo α-subvieneto aktyvacija → AC aktyvinimas → padidėjęs cAMP susidarymas → stimuliuojama baltymo kinazė → skaidoma kinazė, kuri katalizuoja miozino kinazės fosforilinimą, o pastarosios veikla prarandama → miozino fosforilinimas nevyksta → MMC atsipalaidavimas.
HA išsiskyrimą iš nervų galūnių reguliuoja pats neuromediatorius, sužadindamas α 2 -AP presinapsinę membraną. HA emisija mažėja.

Fig. 12. 2 receptoriai
Integruotojo tipo receptoriai
Tai yra receptoriai, kurie yra baltymai, prasiskverbiantys į membraną. Tokiu atveju išorinė baltymo dalis atlieka receptoriaus vaidmenį, o vidinė - katalizatoriaus vaidmenį (13 pav.).

Fig. 13. Integruotojo tipo receptoriai
Citozoliniai receptoriai
Fiziologinėmis sąlygomis tokie receptoriai jungiasi su steroidiniais hormonais (lytiniais hormonais, gliukokortikoidais). Šios medžiagos patenka į ląstelę ir prisijungia prie citozolinių receptorių. Šis kompleksas prasiskverbia į branduolį ir keičia ten esančio genomo darbą. Dėl to keičiasi baltymų sintezė ląstelėje (14 pav.).

Fig. 14. Citozolinis receptorius
Mitochondrijų receptoriai
Mitochondrijose yra ir receptorių, su kuriais sąveikauja vaistinės medžiagos, pavyzdžiui, trijodtironino hidrochloridas, kurie yra natūralaus hormono T 3 analogai. Dėl šios sąveikos padidėja ATP sintezė.
Branduoliniai receptoriai
T 3 prasiskverbia į branduolį ir ten sąveikauja su šio tipo receptoriais. Dėl to keičiasi genomo darbas ir sintetinami nauji baltymai.
Galutinis farmakologinis poveikis (pasak Vershinin)
Nepaisant narkotikų gausos, jų sukelti pokyčiai organizme yra vienodi (15 pav.). Bet kurio vaisto poveikį organams galima sumažinti iki penkių pagrindinių farmakologinių poveikių (pasak N.V. Vershinino):
Raminantis - padidėjusios organų funkcijos susilpnėjimas iki normos (raminamųjų vartojimas).
Užsispyrimas - sumažėjimas žemiau kūno funkcijos normos (vaistų vartojimas anestezijai).
Paralyžius - sumažėjusios organų funkcijos nutraukimas (kvėpavimo slopinimas perdozavus narkotinių analgetikų).
Tonizuoja - sumažėjusios funkcijos stiprinimas iki normalios (β 1 -adrenomimetikų vartojimas).
Jaudulys - Organo funkcijos padidinimas, viršijantis normą (diuretikų vartojimas apsinuodijus, vaistus nuo atsikosėjimo).

Fig. 15. Galutinis farmakologinis poveikis
Narkotikų veikimo tipai
Svarbiausia yra antraeilis dalykas.
Grįžtamasis, negrįžtamasis.
Retais atvejais reikia terapinio tikslo negrįžtamas išjungia struktūrą iš savo funkcijos. Tai taikoma, pavyzdžiui, daugumai antimikrobinių, priešvėžinių agentų, kurie sugeba sudaryti stiprius (kovalentinius) ryšius su DNR spiralės ląstelių elementais („sukryžiavimu“) ar bakteriniais fermentais, dėl to ląstelės praranda gebėjimą daugintis.
Tiesioginis, netiesioginis (netiesioginis).
Ypatingas netiesioginės veiklos atvejis yra refleksas veiksmas. Pavyzdžiui, kraujagyslių išsiplėtimas ir trofinio audinio pagerėjimas dėl odos jutimo nervų galų sudirginimo.
Atrankinis, neselektyvusis.
Vietinis, rezorbcinis.
Resorptive (sisteminis) veikimas vystosi absorbavus vaistą į kraują. Didžioji dauguma narkotikų turi šį poveikį.
Veiksniai, turintys įtakos farmakokinetikai
ir farmakodinamika
I. Išoriniai veiksniai
Aplinka:
sezonas (vasarą, pavartojus tetraciklino, galimas saulės nudegimas (vaistas padidina odos jautrumą ultravioletiniams spinduliams));
aplinkos temperatūra (karštu oru pasireiškia stipresnis vaistų, slopinančių centrinę nervų sistemą, poveikis);
dalinis O 2 slėgis (kurį sukelia epinefrino (adrenalino) tachikardija yra geriau toleruojamas esant dideliam daliniam O 2 slėgiui).
Vaistų savybės:
tirpumas (tirpus Ba 2 CO 3 yra toksiškas, o netirpus Ba 2 SO 4 nėra toksiškas);
radikalai (CH 3 grupės pakeitimas azoto atomu morfino molekulėje -CH2-CH \u003d CH 2 grupe (naloksonas) lemia medžiagos morfinui priešingų savybių atsiradimą medžiagoje);
izomerija (propranololio (anaprilino) pasviręs pasukimo izomeras yra 40–60 kartų stipresnis nei besisukantis);
poliškumas (polinės molekulės paprastai blogai tirpsta lipidų membranose, todėl blogai absorbuojamos ir prasiskverbia pro ląstelių membranas).
Vaistų suvartojimas organizme:
vaisto forma (vaistas skysta forma turi didesnį biologinį prieinamumą, poveikis prasideda greičiau, ir jis yra ryškesnis);
vartojimo būdas (su į veną Vaistas veikia greičiau ir stipriau, nei išgėrus, jo veikimo trukmė yra trumpesnė);
dozė (didėjant dozei (iki tam tikros ribos) didėja vaistų veikimo stiprumas);
narkotikų derinys (galbūt silpninantis, apibendrinantis, stiprinantis kombinuotų vaistų poveikį, o kartais sustiprinantis ir silpninantis kitus narkotikų poveikius);
vartojimo trukmė (su ilgalaikis vartojimas barbitūratų jų poveikis sumažėja, nes pagreitėja jų metabolizmas kepenyse).
II. Vidiniai veiksniai
Biologinis objektas:
rūšies ypatumai (triušiai lengvai toleruoja mirtinas atropino dozes žmonėms);
etninės savybės (mongoloidų rasės žmonėms alkoholio dehidrogenazės trūkumas yra dažnesnis ir dėl to jų jautrumas etanoliui yra didesnis nei europiečių);
amžius (naujagimiams ir mažiems vaikams kepenų gebėjimas metabolizuoti vaistus yra menkas, inkstai nevisiškai funkcionuoja, o skysčių kiekis organizme yra didesnis nei suaugusiųjų; senyviems žmonėms narkotikų metabolizmas sumažėja, o inkstų funkcija mažėja su amžiumi);
lytis (daugelio vaistų pašalinimas vyrams yra greitesnis nei moterų, nes manoma, kad vyriški lytiniai hormonai aktyvina kepenų fermentus);
genotipas (žmonėms, turintiems defektyvią (neaktyvią) pseudocholinesterazę, kvėpavimo sustojimas suleidus raumenis atpalaiduojančio suksametonio (ditilino), trunka ne 2–3 minutes, kaip ir daugumai pacientų, bet 2–3 valandas ar ilgiau, dėl smarkiai sumažėjusio suksametonio sunaikinimo greičio (idiosinkrazija). );
fenotipas (nutukusiems žmonėms lipofiliniai vaistai (fenobarbitalis ir kt.) kaupiasi labiau nei plonuose).
Kūno fiziologija:
mityba (maistas gali daryti didelę įtaką vaisto farmakokinetikai, dažniausiai sulėtinti ir sumažinti vaistų absorbciją);
nėštumas (daugelis vaistų, kurie kerta placentos barjerą, gali paveikti vaisiaus vystymąsi);
žindymas (motinos ir vaiko vartojami antibiotikai gauna pieną, kuris, pavyzdžiui, gali sukelti disbiozę);
stresas (susijaudinę žmonės jautriausiai reaguoja į stimuliuojančio poveikio medžiagas);
paros ritmas (sulfonamidai lėčiau išsiskiria iš inkstų naktį, kai sumažėja šlapimo pH).
Patologinės būklės:
ligos (pacientams, sergantiems kepenų ciroze, tokie vaistai kaip barbitūratai ir chlorpromazinas gali sukelti neįprastai ilgą poveikį);
alkoholizmas (etilo alkoholis sustiprina poveikį centrinės nervų sistemos anksiolitikams, prieštraukuliniams ir antidepresantams);
rūkymas (daugelio vaistų biotransformacija rūkalių kūne yra greitesnė (sumažėja kombinuotų geriamųjų kontraceptikų veiksmingumas rūkančioms moterims)).
Dozė yra į organizmą patenkančių ir bet kokius sukeliančių vaistų kiekis farmakologinis poveikis.
Paprastai dozės išreiškiamos masės, tūrio vienetais (gramais, mililitrais). Veikimo vienetais (ED) dozuojami tam tikri biologinės kilmės vaistai su protarpiniu aktyvumu (hormonai, antibiotikai, heparinas ir kt.).
Dozės klasifikacija
Pagal vartojimo laiką:
vienkartinis;
dienpinigiai;
žinoma.
Veiksmo jėga:
medicininis ar terapinis (minimalus, vidutinis, aukštesnis);
toksiškas (minimalus, vidutinis, mirtinas).
Sotumo dozė yra dozė, kuria galima sukurti reikiamas vaistų koncentracijas audiniuose (pavyzdžiui, gydant širdies glikozidus).
Palaikomoji dozė - dozė, kuria galite palaikyti vaistų koncentraciją plazmoje ir audiniuose, kompensuodami vaisto praradimą šalinimo proceso metu (pavyzdžiui, suskaitmenindami).
Šoko dozė yra dozė, leidžianti sukurti optimalią vaisto koncentraciją, reikalingą jo konkurencijai su tam tikru endogeniniu substratu (pvz., Šoko sulfanilamidų dozė, reikalinga konkuruoti su para-aminobenzenkarboksirūgštimi (PABA) dėl vietos folio rūgšties molekulės struktūroje jos sintezės stadijoje). , vaistai skiriami vidutinėmis terapinėmis dozėmis, kurios daugeliui pacientų suteikia optimalų gydomąjį poveikį be toksinio poveikio. Paprastai tokia dozė yra 1/2 arba 1/3 didžiausios terapinės dozės.
Kviečiamas dozių diapazonas nuo minimalios terapinės iki minimalios toksiškos gydomojo poveikio plotis(SHTD) . Kuo didesnis terapinio veikimo plotis, tuo saugesni vaistai (16 pav.).
SHTD

Fig. 16. Terapinio veikimo plotis
1 - mažiausia terapinė dozė, 2 - vidutinė terapinė dozė,
3 - didžiausia terapinė dozė, 4 - mažiausia toksiška dozė
Terapinis indeksas (TI) - toksinės dozės ir vidutinės terapinės dozės santykis, apskaičiuojamas pagal formulę:
kur TD 50 yra dozė, sukelianti apsinuodijimą 50% pacientų;
ED50 - vidutinė terapinė dozė, t.y., dozė, sukelianti terapinį poveikį 50% pacientų.
Kuo daugiau TI, tuo saugesni narkotikai. Kad vaistas būtų saugus, jo TI turėtų būti didesnis nei 3.
Vaikams ir senjorams vaistų dozavimas turi savo ypatybes, kurios yra susijusios su šių grupių fiziologiniais skirtumais.
Vaiko kūno ypatybės:
kepenų metabolizmo funkcijos nepakankamumas (todėl vaistai yra toksiškesni);
oda ir gleivinės yra gausiai kraujagyslinės (todėl vaistai absorbuojami geriau nei suaugusiesiems);
BBB yra labiau pralaidus (tai sukuria gana didelę narkotikų koncentraciją smegenyse);
didelis vandens kiekis audiniuose;
mažiau riebalinio audinio
Kiek mažesniu mastu vaistai jungiasi su plazmos baltymais (tai gali sukelti toksines reakcijas, nes padidėja laisvoji (aktyvioji) frakcija);
inkstų ekskrecinė funkcija yra sumažėjusi (tai lemia ilgesnį vaistų veikimą).
Atsižvelgiant į tai, kad yra pakankamai reikšmingų vaistų farmakodinamikos ir farmakokinetikos skirtumų vaikams ir suaugusiems, skaičiuojant vaisto dozę vaikui yra nepriimtina, kad proporcingas amžių proporcingas suaugusiųjų dozės mažinimas būtų proporcingas, nes gali sukelti nenuspėjamų padarinių.
Vaikams dozė apskaičiuojama 1 kilogramui kūno svorio, per gyvenimo metus, vienam kūno paviršiaus plotui. Pvz .:
Vaiko dozė \u003d Suaugusiojo dozė × vaiko svoris / 70 kg
Senyvų žmonių fiziologinės savybės:
pažeidimas medžiagų apykaitos kepenyse dėl atrofinių ir distrofinių pokyčių;
mažas vandens kiekis organizme ir didesnis riebalinio audinio kiekis;
sumažėjęs plazmos baltymų kiekis (dėl to padidėja laisvoji vaistų dalis);
laipsniškas inkstų išsiskyrimo funkcijos sumažėjimas;
Centrinė nervų sistema ir širdies ir kraujagyslių sistema yra jautresni vaistų veikimui.
Šalutinis (nepageidaujamas) vaistų poveikis
Nepageidaujamas poveikis reiškia bet kokią organizmui pavojingų vaistų reakciją, atsirandančią, kai jie vartojami ligoms gydyti, diagnozuoti ar jų prevencijai. Nepageidaujamos reakcijos pasireiškia nuo 1 iki 30% atvejų, kai vaistai vartojami klinikinėje praktikoje. Yra narkotikų, kurių vartojimas labai dažnai sukelia nepageidaujamas reakcijas. Tai apima antibiotikus, gliukokortikoidus, nesteroidinius vaistus nuo uždegimo, priešepilepsinius, priešnavikinius ir kitus vaistus. Nepageidaujamą vaistų poveikį galima suskirstyti į kelias grupes.
Nepageidaujamas poveikis, susijęs su terapine vaistų koncentracija kraujyje:
alerginės reakcijos;
pseudoallerginės reakcijos;
genetiškai nulemtos reakcijos (idiosinkrazija);
psichinės ir fizinės priklausomybės sindromas.
Pseudoallerginės reakcijos (anafilaktoidas) pasižymi tiesioginiu vaisto poveikiu stiebo ląstelei be IgE sintezės. Skirtingai alerginės reakcijos, jie priklauso nuo dozės. Paprastai pacientui nėra sunkios alerginės anamnezės. Pseudoallergines reakcijas gali sukelti ampicilinas, jodo turinčios radioaktyviosios medžiagos, vietiniai anestetikai ir kt.
Idiosinkrazija - genetiškai nulemtas vaistų netoleravimas. Neįmanoma numatyti genetinių reakcijų. Jie yra susiję su paveldimais fermentų sistemų defektais arba su paveldimomis medžiagų apykaitos ligomis.
Pavyzdžiui, pseudocholinesterazės trūkumą lydi ditilino sunaikinimo slopinimas (dėl kurio pailgėja raumenų atpalaidavimas). Dėl gliukozės-6-fosfato dehidrogenazės trūkumo sumažėja daugelio redukuojančių fermentų (glutationo reduktazės ir kt.) Aktyvumas. Oksiduojančių vaistų (sulfonamidų, nitrofuranų, antimaliarinių vaistų - chinino, chingamino, primaquino ir kt.) Patekimas į organizmą lemia eritrocitų hemolizę ir methemoglobino susidarymą. Paveldimą sarkoplazminio retikulumo anomaliją lydi sutrikusi kalcio fiksacija ant aktomiozino ir bendroji rūgščių-šarmų būsena, kai vartojamas halotanas, barbitūratai ir kiti vaistai, kurie dažniausiai naudojami anestezijos praktikoje. Atsiranda piktybinė hipertermija, dėl kurios pacientas gali mirti.
Psichinė ir fizinė priklausomybė (priklausomybė). Narkotikus sukelia tokie vaistai kaip opijus ir jo alkaloidai (morfinas, kodeinas, heroinas), promedolis, kokainas, amfetaminas, etanolis, kai kurie barbitūratai ir kt.
Euforija yra pagrindinė nekontroliuojamo narkotikų vartojimo ar vystymosi priežastis psichinė priklausomybė. Euforijai būdingas nemalonių emocijų, baimės, nerimo jausmų išnykimas ar nuobodulys. Noras vėl patirti euforiją yra psichinės priklausomybės priežastis.
Fizinė priklausomybė susijęs su abstinencijos sindromo (abstinencijos ar deprivacijos sindromo) atsiradimu: šaltkrėtis, hipertermija, ryškūs kraujospūdžio svyravimai, raumenų ir sąnarių skausmai, vėmimas, nerimas, priešiškumas, nemiga. Be to, simptomų skaičius ir intensyvumas yra susijęs su fizinės priklausomybės laipsniu.
Galbūt fizinės priklausomybės vystymosi mechanizmas yra susijęs su tuo, kad narkotiniai analgetikai, grįžtamojo ryšio principu aktyvuodami opiatų receptorius, slopina endogeninių opiatų peptidų išsiskyrimą, palaipsniui pakeisdami jų veiklą. Panaikinus analgetikus, sutrinka ir anksčiau paskirtas analgetikas, ir endogeninis peptidas. Išsivysto atšaukimo sindromas.
Nepageidaujamas poveikis, susijęs su toksiška vaistų koncentracija kraujyje (daugiausia būdingas vaistams, kurių terapinis poveikis siauras):
nefrotoksiškumas (aminoglikozidai);
ototoksiškumas (ilgalaikis aminoglikozidų vartojimas gali sukelti klausos praradimą iki negrįžtamo kurtumo išsivystymo);
hematotoksiškumas (antibiotikas levomicetinas slopina kraujodaros sistemą);
neurotoksiškumas (antimikrobinis vaistas iš fluorokvinolonų grupės lomefloksacinas sukelia nemigą, galvos skausmą);
skrandžio toksiškumas (ilgai vartojami salicilatai gali sukelti pepsinę opą);
kepenų toksiškumas (antibiotikai-linkozamidai sukelia gelta padidėjus kepenų transaminazių koncentracijai plazmoje, tai rodo kepenų audinio pažeidimą);
kardiotoksiškumas (priešvėžiniai antibiotikai).
Nepageidaujamas poveikis, nepriklausantis nuo vaistų koncentracijos kraujyje:
disbiozė;
superinfekcija;
hipovitaminozė;
imunodeficitas.
Superinfekcija vystosi vartojant labai aktyvius antibiotikus ir kitus antimikrobinius vaistus. Jo atsiradimas susijęs su tuo, kad antibiotikai slopina jiems jautrią mikroflorą, o antibiotikams atspari mikroflora (apatogeninė ar sąlygiškai patogeniška) pradeda intensyviai daugintis ir tam tikromis sąlygomis gali sukelti naują ligą - superinfekciją.
Neigiamas vaistų poveikis embrionui ir vaisiui
Šiuolaikinėmis sąlygomis ypač aktuali yra vaistų poveikio tiek vaisiui, tiek terapinei, tiek toksinei koncentracijai, problema. Išrašyti vaistus nėščioms moterims reikia labai atsargiai, nes vaistai gali prasiskverbti pro placentos barjerą, atsirasti vaisiaus kraujyje ir turėti neigiamos įtakos.
Tokios įtakos turi:
Embriotoksinis poveikis.
Teratogeninis poveikis.
Fetotoksinis poveikis.
Teratogeninis poveikis dažniausiai atsiranda vartojant vaistus nuo 3 iki 10 nėštumo savaitės (I trimestras). Šiuo laikotarpiu vyksta histogenezė ir organogenezė. Teratogeninis poveikis yra vaisiaus audinių diferenciacijos pažeidimas, dėl kurio gali gimti vaikas, turintis galūnių, galvos ir vidaus organų apsigimimus. Atsižvelgiant į defekto ypatybes, vaikas gali būti negyvybingas ir mirti netrukus po gimimo arba likti neįgalus visam gyvenimui.
Teratogeninio poveikio pavyzdys yra galūnių neišsivystymas (židiniai) dėl talidomido vartojimo. Androgenų vartojimas nėštumo metu sukelia vaisiaus maskulinizaciją. Vartojant dideles tetraciklinų dozes, vaistas kaupiasi vaisiaus kauluose ir pažeidžiamas jų vystymasis.
Fetotoksinis poveikis - Tai yra subrendusio ar jau subrendusio vaisiaus reakcija į vaistus, kurie gali pakeisti gyvybines funkcijas. Pavyzdžiui, indometacinas ir kai kurie kiti NVNU sukelia arterinio latako uždarymą ar susiaurėjimą. Aminoglikozidiniai antibiotikai sukelia ototoksiškumą. Antikoaguliantai gali sukelti kraujavimą naujagimiui. Antitiroidinių vaistų vartojimą lydi goiterio vystymasis. Šios toksinės reakcijos gali sukelti sunkią vaisiaus ir naujagimio patologiją ir padidinti vaikų perinatalinį mirtingumą.
Reiškiniai, vystomi pakartotinai įvedant narkotikus
Klinikinėmis sąlygomis nėra daug atvejų, kai vaistai vartojami vieną kartą. Su tuo susiduriama atvaizduojant skubioji pagalba. Dažniausiai vėl skiriami vaistai. Tokiu atveju galima pastebėti šių tipų reakcijas.
Kaupimas yra medžiagos kaupimasis organizme ( materialinė kumuliacija) ar jo padarinius ( funkcinė kumuliacija) Tikimybė medžiaga kumuliacija yra didesnė, tuo lėčiau organizme inaktyvuojamas vaistas ir tuo stipriau jis jungiasi su audinių biosubstratu. Kumuliacija visada yra pavojinga dėl staigaus įvairių komplikacijų ir toksinių reakcijų skaičiaus ir sunkumo padidėjimo. Barbitūratai, širdies glikozidai ir kt. Yra labiausiai linkę į kumuliaciją. Dėl funkcinės kumuliacijos padidėjęs terapinis poveikis, kuris tampa intoksikacija, fiziškai nutraukia vaisto kaupimąsi laiku (to gali ir nebūti). Taigi, sergant alkoholizmu, didėjantys centrinės nervų sistemos funkcijos pokyčiai gali sukelti delyro tremenso vystymąsi. Tokiu atveju medžiaga (etilo alkoholis) greitai oksiduojasi ir nesiliauja audiniuose. Apibendrintas tik jo neurotropinis poveikis.
Tolerancija (priklausomybė) - tai laipsniškas silpnėjimas (iki visiško praradimo) terapinis veiksmas vaistas su ilgalaikiu vartojimu. Tolerancija gali turėti skirtingas priežastis ir paprastai vystosi lygiagrečiai su visais šios farmakologinės grupės atstovais. Tai gali būti šių reakcijų pasekmė:
receptorių skaičiaus padidėjimas ar sumažėjimas;
homeostatinių reguliavimo mechanizmų, kompensuojančių vaisto sukeltą poslinkį, veikimo gerinimas (pvz., padidėjęs kraujospūdį mažinančių kraujagyslių kraujagyslių išsiplėtimo padidėjimas hipertenzija sergantiems pacientams dėl skysčių susilaikymo, padidėjęs širdies ritmas, kitų kraujagyslių tonuso padidinimo mechanizmų įtraukimas);
pagreitėjęs vaisto inaktyvacija dėl jo indukcijos arba kito mikrosominių fermentų cheminio veiksnio.
Bandymai įveikti priklausomybę tiesiog didinant to paties vaisto dozes yra neveiksmingi ir kupini narkotikų terapijos komplikacijų.
Tachifilaksija - greito toleravimo galimybė, kai priklausomybė atsiranda greitai, per kelias valandas ar dienas. Pavyzdžiui, tolerancija efedrinui vystosi jau antrą kartą vartojant vaistą.
Nutraukimo sindromas atsiranda staiga nutraukus vaisto vartojimą šiais atvejais:
pasibaigus įprastai patogenetiškai farmakoterapijai (pavyzdžiui, paūmėjus IHD - nitratai, β blokatoriai);
panaikinus vaistus, kurie gali sukelti abstinencijos simptomus (narkotiniai analgetikai, trankvilizatoriai, psichostimuliatoriai);
baigus terapiją, vaistai, kurių analogai gaminami organizme (gliukokortikoidai, skydliaukės hormonai); šių vaistų vartojimas gali slopinti endogeninių hormonų gamybą, kurį lydi priklausomybė nuo narkotikų.
Rikošeto sindromas (atkryčio reiškinys) - yra savotiškas abstinencijos sindromas. Reiškinio esmė yra reguliavimo proceso uždraudimas arba atskira reakcija, anksčiau slopinama vaistine medžiaga. Dėl to staigus ligos paūmėjimas yra tam tikras superkompensavimas, palyginti su lygiu prieš gydymą.
Geriausias būdas išvengti yra ir laipsniškas vaisto nutraukimas.
Narkomanija (žiūrėti temą „ Šalutinis poveikis vaistinės medžiagos “).
Vaistų sąveika
Vienu metu skiriama keletas vaistai naudojama, kai tuo pat metu yra kelios problemos. Tačiau gydant vieną ligą, siekiant sustiprinti terapinį poveikį ir (ar) sumažinti, dažnai skiriami keli vaistai šalutinis poveikis.
Pvz., Norint padidinti analgetinį fentanilio poveikį, jis derinamas su droperidoliu.
Norint sumažinti hidrochlorotiazido sukeltą hipokalemiją, skiriamas pananginas (sudėtyje yra kalio asparaginato).
Norėdami padidinti terapinį poveikį ir sumažinti šalutinį poveikį, levodopa derinama su karbidopu.
Kviečiamas terapijos tipas, kai daugybė vaistų yra moksliškai nepagrįstai naudojami ligai gydyti polifarmacija.
Jei vienas vaistas patenka į organizmą, apie jo likimą (farmakokinetika) ir poveikį (farmakodinamika) galima spręsti apie 90–95% atvejų; jei du vaistai - tik 50% atvejų, o jei į organizmą patenka daugiau kaip trys vaistai - iki 10%. Reikia pridurti, kad nepageidaujamų reakcijų rizika kartu vartojant narkotikus taip pat padidėja: 5%, jei vartojama iki 5 vaistų, 20% - iki 8 vaistų ir 40% - iki 15 vaistų.
Vaistų sąveika gali būti nepageidaujama, neigiama. Galimas vaistų terapinių savybių susilpnėjimas, padidėjęs jų šalutinis poveikis ar toksinio poveikio pasireiškimas. Tokiais atvejais jie kalba apie vaistų nesuderinamumas.
Pavyzdžiui, penicilinai turi baktericidinį poveikį augančiam mikroorganizmui, o tetraciklinai sutrikdo baltymų sintezę ir slopina bakterijų augimą. Šiuo atžvilgiu tetraciklinai silpnina penicilinų poveikį.
Vaistų sąveika gali būti:
Farmacija
Farmakologinis.
Pavyzdžiui, neįmanoma sujungti aminofilino tirpalų su pipolfeno ar askorbo rūgšties tirpalais tame pačiame švirkšte, nes rūgščioje terpėje nusėda aktyvusis aminofilino principas - teufilinas.
Farmakologinis sąveika yra padalinta į:
farmakokinetika;
farmakodinaminis.
Farmakokinetinė vaistų sąveika gali pasireikšti skirtingais lygmenimis:
Siurbimas.
vaistų poveikis pH virškinimo trakte - antacidinių vaistų vartojimas sukelia pH padidėjimą skrandyje, dėl to silpnai rūgščių vaistų absorbcija, taigi ir šių medžiagų poveikis sumažėja.
vaistų poveikis virškinimo trakto motorikai - M-anticholinerginiai vaistai ir narkotiniai analgetikai sulėtina virškinimo trakto judrumą, dėl ko ilgesnis vaisto kontaktas su gleivine ir gali sukelti dirginimą (pavyzdžiui, vartojant aspiriną).
Paskirstymas.
Metabolizmas.
Išsiskyrimas.
Farmakodinaminė sąveika - tai yra vaistų sąveika, kai vienas iš jų keičia kito farmakologinio poveikio generavimo ir įgyvendinimo procesą. Farmakodinaminė sąveika gali vykti dviem būdais:
Sinergizmas.
Antagonizmas.
apibendrinta - paprastas dviejų ar daugiau vaistų poveikio pridėjimas (pvz., kartu skiriant du akrilo rūgšties ir furosemido diuretikus, susideda jų diurezinis poveikis), tokio tipo sąveika išreiškiama formule 1 + 1 \u003d 2;
potencijuotas - toks sąveikos tipas, kai vaistų derinio farmakologinis poveikis yra didesnis už matematinę kiekvieno atskirai paskirto vaisto farmakologinio poveikio sumą (pavyzdžiui, vartojant antipsichozinius antipsichozinius vaistus, droperidolis žymiai sustiprina opioidinį analgetiką fentanilį sukeliantį analgezinį poveikį); šio tipo vaistų sąveika išreiškiama formule 1 + 1 \u003d 3.
Antagonizmas - tai priešingas tuo pačiu metu vartojamų vaistų poveikis, kai jų bendras farmakologinis poveikis organizme yra mažesnis už atskirų vaistų poveikį. Šios antagonizmo rūšys yra:
fizinė, pagrįsta fizine medžiagų sąveika (pavyzdžiui, aktyvuota anglis adsorbuoja toksinus);
cheminė, pagrįsta chemine vaistų sąveika (pavyzdžiui, padidėjus rūgštingumui, druskos rūgšties neutralizavimas skrandyje su antacidiniais vaistais);
konkurencinis antagonizmas stebimas, kai medžiagos yra panašios struktūros ir konkuruoja dėl to paties receptoriaus (pavyzdžiui, M-cholino blokatorius atropinas ir M-cholinomimetinis pilokarpinas konkuruoja dėl prisijungimo prie M-cholinerginių receptorių);
pastebimas nekonkurencinis antagonizmas esant priešingam medžiagų poveikiui, veikiant skirtingus receptorius; gali būti nekonkurencinis antagonizmas funkciniskai medžiagos veikia skirtingus to paties organo receptorius (pavyzdžiui, sužadinantis adrenalino poveikis ir slopinamasis acetilcholino poveikis širdies funkcijai) ir fiziologiniskai medžiagos veikia skirtingus skirtingų organų receptorius (pavyzdžiui, aldosteronas, padidindamas kraujo spaudimą, veikdamas inkstus, o klonidinas mažina kraujospūdį, veikdamas centrinę nervų sistemą).
Farmakologija, jos skyriai, užduotys ir vieta tarp medicinos, biologinės ir specializuotų disciplinų. Vidaus farmakologijos pasiekimai.
Farmakologija - biomedicinos mokslas apie vaistines medžiagas ir jų poveikį organizmui; plačiąja prasme mokslų apie fiziologiškai aktyvias medžiagas apskritai ir jų poveikį biologinėms sistemoms.
Skyriai: Bendri ir privatūs. Bendroji dalis: 1) vaistų gamybos principai, jų sudėtis ir savybės 2) metabolizmas - farmakokinetika ir farmakodinamika, 3) toksikologija, 4) farmakogenetika 5) farmakogenomika.
Recepto apibrėžimas ir struktūra. Receptų formos. Bendros receptų skyrimo taisyklės. Toksiškų, narkotinių, stiprių vaistų skyrimo ypatybės.
Receptas- Tai gydytojo kreipimasis į vaistininką dėl vaistų išleidimo pacientui, nurodant vaisto formą, dozę ir vartojimo būdą. Tai yra medicininis, teisinis ir piniginis dokumentas nemokamo ar lengvatinio vaistų išdavimo atveju. Dozėišreiškiama dešimtainės sistemos masės arba tūrio vienetais ir nurodoma arabiškais skaitmenimis. Ištisų gramų skaičius yra atskiriamas kableliu (1.0). Dažniau naudojama: 0,1 - viena decigrama; 0,01 - viena centigrama; 1,001 vienas miligramas. Lašai, iš kurių sudarytas vaistas, žymimi romėnišku skaitmeniu, priešais kurį parašyta gtts. Taigi biologiniai veikimo vienetai recepte nurodo 500 000 vienetų. Skystos medžiagos receptuose nurodoma mililitrais (0,1 ml). Receptas patvirtintas parašu ir asmeniniu antspaudu. Recepte turi būti nurodytas: paciento amžius, jo išrašymo data, pavardė ir paciento inicialai; gydytojo pavardė ir inicialai, apmokėjimo už vaistą tvarka. Be to, lengvatiniai receptai surašomi ant specialių formų, turinčių antspaudą ir antspaudą. Ant specialių kito pavyzdžio formų taip pat skiriami vaistai iš narkotinių medžiagų sąrašo, migdomosios tabletės, anoreksigeniniai vaistai. Be to, gydytojas išrašo receptą, užrašo savo parašą ir patvirtina jį asmeniniu antspaudu. Be to, jį pasirašo vyriausiasis gydytojas arba jo pavaduotojas, recepte yra apvalus antspaudas ir medicininis antspaudas
institucijų. Ta pati paskyrimo procedūra taip pat apibrėžta anaboliniams steroidams, taip pat fenobarbitaliui, ciklodoliui, efedrino hidrochloridui ir klonidinui ( akių lašai, ampulės), sunoref tepalai. Kitoms receptinių formų rūšims skiriami antipsichoziniai vaistai, raminamieji vaistai, antidepresantai, vaistai, kurių sudėtyje yra etilo alkoholio ir kt. Ambulatoriniams pacientams draudžiama skirti eterį anestezijai, chloroetilą, fentanilį, sombreviną, ketaminą. Receptas prasideda žodžiu Receptas (Rp. - sutrumpintai), reiškiančiame „imk“, tada išvardijami išrašytų prekių pavadinimai ir kiekiai
vaistinės medžiagos genitalijų byloje. Pirmiausia vadinama pirminiu, paskui pagalbiniu. Toliau nurodoma reikiama vaisto forma. Pavyzdžiui Misce ut fiat pulvis(M. f. pulvis) - „sumaišykite, kad susidarytų milteliai“. Jei dozuojama, rašykite: " Da pasakos dozių skaičius10 "-" išrašykite tokias dozes, kurių skaičius yra 10 ". Recepto pabaigoje po žodžio Signa(S) - „paskirti“ rusų (arba nacionaline) kalba nurodykite vaisto vartojimo būdą.
Bendroji farmakologija, jo skyriai. Pavyzdžiai bendrieji mechanizmai narkotikų poveikis. Vaisto ir nuodų sąvoka.
1) vaistų gamybos principai, jų sudėtis ir savybės 2) metabolizmas - farmakokinetika (jų įsisavinimo, pasiskirstymo ir biotransformacijos organizme doktrina) ir farmakodinamika (vaistų poveikio organizmui doktrina) 3) toksikologija, 4) farmakogenetika (medicinos skyrius) genetika ir farmakologija, tiriant organizmo reakcijų į organizmą pobūdį vaistai priklausomai nuo paveldimų veiksnių). 5) farmakogenomika (farmacijos ir farmakologijos šaka, tirianti kiekvieno žmogaus genetinių variacijų poveikį jo reakcijai į vaistą)
Kai organizme vartojami vaistai, pastarieji gali veikti specifinius receptorius, fermentus, ląstelių membranas arba tiesiogiai sąveikauti su ląstelių medžiagomis. Poveikis specifiniams receptoriams visų pirma grindžiamas tuo, kad makromolekulinės struktūros yra selektyviai jautrios tam tikriems cheminiams junginiams. Cheminių medžiagų sąveiką su receptoriais lydi fiziologiniai, biocheminiai pokyčiai organizme, kurie galiausiai lemia klinikinį poveikį. Vaistai - farmakologiniai agentai (medžiagos ar medžiagų mišiniai), atlikti klinikinių tyrimų metu ir patvirtinti šalies įgaliotos įstaigos nustatytu būdu naudoti ligų prevencijai, diagnozei ir gydymui, gaunami iš kraujo, kraujo plazmos, taip pat iš žmonių ar gyvūnų organų, audinių, augalai, mineralai, sintetinant arba naudojant biotechnologijas. Taigi vaistai apima augalinės, gyvūninės ar sintetinės kilmės medžiagas, kurios turi farmakologinį poveikį ir yra skirtos gaminti ir gaminti dozavimo formos. Apsinuodijimas - medžiaga, dėl kurios dozės, net ir nedidelės, palyginti su kūno svoriu, sukelia organizmo ardymą: apsinuodijimą, intoksikaciją, ligas ir patologines būkles.
Farmakodinamika
Jis tiria vaistų veikimo mechanizmą, taip pat jų biocheminį ir fiziologinį poveikį. Jos užduotys apima cheminės ir fizinės sąveikos tarp vaisto ir tikslinės ląstelės aprašymą, taip pat visą jo farmakologinio poveikio spektrą ir sunkumą. Farmakodinaminių modelių žinojimas leidžia pasirinkti tinkamus vaistus. Farmakodinaminiai tyrimai suteikia gilesnį supratimą apie biocheminių ir fiziologinių procesų reguliavimą organizme (Katzung B.G., 1998; Lawrence D.R. ir kt., 2002).
Daugelio vaistų veikimą skatina jų prisijungimas prie organizmo makromolekulių. Šių makromolekulių funkcinės būklės pasikeitimas savo ruožtu suaktyvina biocheminių ir fiziologinių reakcijų grandinę, kuri virsta farmakologiniu poveikiu. Makromolekulės, su kuriomis sąveikauja cheminės medžiagos, vadinamos receptoriais. Taigi bet kurios funkciškai aktyvios makromolekulės gali tarnauti kaip vaistų receptoriai. Iš šio teiginio išplaukia kelios svarbios pasekmės. Pirmiausia, pasitelkę vaistus, galite pakeisti bet kurio fiziologinio proceso organizme greitį. Antra, vaistai keičia tik natūralias ląstelės fiziologines funkcijas, nesuteikdami jai naujų savybių.
Receptoriai
Dauguma receptorių yra baltymai. Tai yra hormonų receptoriai, augimo faktoriai, mediatoriai, baltymai, dalyvaujantys svarbiausiose medžiagų apykaitos ir reguliavimo reakcijose (dihidrofolato reduktazė, acetilcholinesterazė), transportiniai baltymai (Na +, K + -ATPazė), struktūriniai baltymai (tubulinas). Ląstelės komponentai, kurie yra skirtingo cheminio pobūdžio, pavyzdžiui, nukleorūgštys, su kuriomis sąveikauja priešnavikiniai agentai, taip pat gali veikti kaip receptoriai.
Endogeninių reguliavimo veiksnių receptoriai - hormonai, mediatoriai ir kt. - turi farmakologinę reikšmę. Šie receptoriai yra daugelio vaistų taikiniai, dažniausiai veikiantys selektyviai dėl didelio endogeninių ligandų receptorių specifiškumo. Vaistai, kurie, prisijungdami prie receptorių, atkuria endogeninio ligando fiziologinį poveikį, vadinami aganistais arba stimuliatoriais. Vaistai, kurie nesukelia šio efekto, bet slopina endogeninių ligandų surišimą, vadinami antagonistais arba blokatoriais. Medžiagos, kurių poveikis yra mažiau ryškus nei agonistų poveikis, vadinamos daliniais agonistais. Preparatai, stabilizuojantys receptorių neaktyvia forma, yra klasifikuojami kaip atvirkštiniai agonistai.
Struktūrinė ir funkcinė priklausomybė
Cheminė vaisto struktūra gana griežtai nustato jo afinitetą receptoriams ir vidinį aktyvumą. Nedidelis cheminės struktūros pasikeitimas gali reikšmingai paveikti farmakologines savybes.
Naujų vaistų sintezė daugiausia paremta tuo. Kadangi cheminis modifikavimas nebūtinai vienodai veikia visas farmakologines savybes, galima pagerinti vaisto veiksmingumą ir saugumą, padidinti jo selektyvumą ir pagerinti farmakokinetines savybes. Pavyzdžiui, daugelis klinikoje naudojamų hormonų ir mediatorių antagonistų yra sintetinami chemiškai modifikuojant endogenines medžiagas.
Vaistų vartojimo taškai
Kadangi vaistų poveikį tarpininkauja receptoriai, vaisto vartojimo tašką lemia ne tik jo pasiskirstymo ypatybės, bet ir receptorių lokalizacija, o farmakologinis poveikis priklauso nuo šių receptorių funkcinės reikšmės. Vaistų, kurių receptoriai yra paplitę daugelyje organų ir audinių, farmakologinis poveikis yra įvairus. Jei šie receptoriai atlieka ląstelėms gyvybiškai svarbią funkciją, tai ne tik sunku vartoti vaistą terapiniais tikslais, bet ir nesaugu. Nepaisant to, tokie vaistai gali turėti didelę klinikinę reikšmę. Taigi širdies glikozidai, plačiai naudojami sergant širdies nepakankamumu, keičia jonų pernešimą per ląstelės membraną, nuo kurios priklauso gyvybinis ląstelės aktyvumas. Jie pasižymi siauru terapiniu diapazonu ir yra labai toksiški. Kitas pavyzdys yra priešnavikiniai vaistai. Jei receptoriai, su kuriais sąveikauja vaistas, yra tik kelių rūšių diferencijuotose ląstelėse, jo poveikis yra selektyvesnis. Šie vaistai gali sukelti mažiau nepageidaujamų reakcijų, tačiau vis dėlto šie vaistai gali būti toksiški, jei jų receptoriai atlieka gyvybiškai svarbią funkciją. Kai kurie biologiniai nuodai (botulino toksinas ir kt.) Veikia panašiai. Be to, net jei tiesioginis farmakologinis poveikis yra selektyvus, jo pasekmės gali būti įvairesnės.
Endogeninių reguliavimo faktorių receptoriai
Terminas receptorius reiškia bet kokį makromolekulinį ląstelės komponentą, su kuriuo jungiasi vaistas. Vienas iš svarbiausių vaistų receptorių yra ląsteliniai baltymai, kurie tarnauja kaip endogeninių reguliavimo veiksnių receptoriai - hormonai, augimo faktoriai, mediatoriai. Jungdamiesi prie endogeninio ligando, receptoriai perduoda signalą iš jo į tikslinę ląstelę.
Iš receptoriaus signalas patenka į ląstelių taikinius (efektoriniai baltymai) tiesiogiai arba per tarpines signalines molekules - baltymų konverterius. Receptorius, baltymų konverteriai ir efektoriniai baltymai sudaro receptoriaus-efektoriaus sistemą. Artimiausias efektoriaus baltymas signalo perdavimo grandinėje dažnai yra ne galinis efektorius (tiesiogiai veikiantis ląstelių funkcijas), bet fermentas arba transportinis baltymas, dalyvaujantis formuojant, pernešant ar inaktyvuojant antrąjį tarpininką - joną ar mažą molekulę. Antrasis tarpininkas savo ruožtu perduoda informaciją į įvairius tarpląstelinius taikinius, užtikrindamas, kad jie tuo pačiu metu reaguoja į vieno receptoriaus signalą.
Receptoriai, konvertuojantys baltymus, ir efektoriniai baltymai ne tik perduoda informaciją. Jie taip pat koordinuoja signalus iš skirtingų ligandų, viena vertus, ir visus šiuos signalus, susijusius su medžiagų apykaitos procesais ląstelėje.
Veikdami kaip katalizatoriai, receptoriai sustiprina biologinį signalą. Dėl šios svarbios savybės jie yra puikūs vaistų tikslai. Tačiau signalo stiprintuvai yra ne tik receptoriai, turintys fermentinį aktyvumą, bet ir visi žinomi receptoriai. Iš tiesų, kai viena ligando molekulė jungiasi prie receptoriaus, konjuguoto su jonų kanalu, daugelis jonų praeina pro pastarąjį. Tas pats pasakytina ir apie steroidinių hormonų receptorius: viena hormono molekulė sukelia daugelio mRNR kopijų, kurių pagrindu susintetinta daugybė baltymų molekulių, transkripciją.
Atsižvelgiant į struktūrą ir veikimo mechanizmą, biologiškai aktyvių medžiagų receptoriai yra suskirstyti į keletą klasių. Šių užsiėmimų skaičius yra nedidelis.
Fermentiniai receptoriai
Didžiausia receptorių grupė, turinti fermentinį aktyvumą, yra membraniniai receptoriai, turintys savo baltymų kinazės aktyvumą. Jie fosforilina įvairius efektorinius baltymus, esančius ląstelės membranos viduje. Dėl to keičiasi šių baltymų funkcija arba jų sąveika su kitais baltymais.
Yra dar viena receptorių, turinčių baltymų kinazės aktyvumą, klasė - tai receptoriai, konjuguoti su baltymų kinazėmis. Jiems trūksta tarpląstelinio katalitinio domeno, tačiau, sąveikaudami su agonistais, jie jungiasi arba aktyvuoja tarpląstelines baltymų kinazes vidiniame membranos paviršiuje. Tai yra neurotrofinių veiksnių receptoriai ir T ir B limfocitų, susidedančių iš kelių subvienetų, antigenus atpažįstantys receptoriai. Pastarieji taip pat sąveikauja su fosfotirozino fosfatais. Kitų receptorių, neturinčių intraląstelinio efektoriaus domeno, funkciją gali tarpininkauti kai kurie kiti efektoriniai baltymai.
Kiti receptoriai, turintys savo fermentinį aktyvumą, turi panašią struktūrą. Tai apima, pavyzdžiui, receptorius, turinčius savo fosfotirozino fosfatazės aktyvumą: jų tarpląstelinis domenas aminorūgščių seka yra panašus į adhezijos molekules. Daugeliui receptorių, turinčių savo fosfotyrosine fosfatazės aktyvumą, endogeniniai ligadai nežinomi. Tačiau, remiantis genetiniais ir biocheminiais tyrimais, atliktais su skirtingų tipų ląstelėmis, svarbų vaidmenį vaidina fermentinis šių receptorių aktyvumas. Prieširdžių natriuretinio hormono receptorių tarpląstelinis domenas, kiti NUP, taip pat guanilino receptoriai, turi savo guanilato ciklazės aktyvumą ir sintezuoja cGMP, kuris veikia kaip antrasis tarpininkas. Galbūt yra ir kitų receptorių, turinčių savo fermentinį aktyvumą.
Jonų kanalais sujungti receptoriai
Kai kurių mediatorių receptoriai yra tiesiogiai susiję su jonų kanalais, sąveikaudami su ligandu, selektyviai praeina tam tikrus jonus per ląstelės membraną (chemiškai jautrūs kanalai, jonotropiniai receptorių kanalai, jonotropiniai receptoriai).
G baltymų jungiami receptoriai
Tai gana didelė receptorių klasė, kuri sąveikauja su efektoriais per G baltymus (baltymai, kuriuose guanino difosfatas (GDF) pakeičia guanino trifosfatą (GTP). Tai apima daugelio biogeninių aminų, lipidus signalizuojančių molekulių (ypač eikosanoidų) ir įvairių peptidų receptorius. fermentai (adenilato ciklazė, fosfolipazė C) ir kalio bei kalcio membranos kanalai veikia kaip efektoriai. Didelis skaičius ir svarbus fiziologinis receptorių, sujungtų su G baltymais, vaidmuo daro juos puikius. mano tikslai dėl narkotikų: maždaug pusė visų gydytojų išrašytų vaistų (išskyrus antibiotikus) veikia šiuos receptorius.
Ląstelė ant savo paviršiaus gali nešti iki 20 receptorių, kurių kiekvienas selektyviai sąveikauja su vienu ar daugiau G-baltymų tipų (jie skiriasi skirtingais α-subvienetų tipais). Α-subvienetas gali sąveikauti su vienu ar daugiau efektorinių baltymų, o tai leidžia koordinuoti signalus iš skirtingų ligandų receptorių, naudojant vieną G-baltymą. Kita vertus, vienas receptorius gali suaktyvinti kelis tarpląstelinio signalo perdavimo mechanizmus, suaktyvindamas kelių tipų G baltymus ir veikdamas skirtingus efektorinius baltymus per tą patį α-subvienetą. Tokia sudėtinga signalų divergencijos ir konvergencijos sistema suteikia galimybę lanksčiai reguliuoti ląstelių funkcijas (Ross, 1992).
Tarpląsteliniai receptoriai
Steroidinių ir skydliaukės hormonų, kalcitriolio ir retinoidų receptoriai yra tirpūs tarpląsteliniai DNR jungiantys baltymai, kurie reguliuoja tam tikrų genų transkripciją (Mangelsdorf ir kt., 1994). Šie receptoriai priklauso ligandui jautrių transkripcijos reguliatorių šeimai. Transkripcijos veiksnių funkciją reguliuoja fosforilinimas, sąveika su ląstelės baltymais, metabolitais ir kitais ląstelės reguliavimo elementais.
Antrosios tarpinės sistemos
cAMP. Antrinės tarpinės sistemos taip pat dalyvauja integruojant išorinius signalus. Nors yra daug daugiau žinomų receptorių ir baltymus signalizuojančių molekulių nei antrieji mediatoriai, pastarieji dalyvauja daugelyje ląstelių signalo perdavimo būdų. Labiausiai ištirti antrieji tarpininkai yra cAMP, cGMP, Ca 2+, IF 3 (inozitolio trifosfatas), DAG (diacilglicerolis), NO. Ši heterogeninių junginių grupė nuolat auga. Antrieji tarpininkai sąveikauja tiesiogiai (keisdami vienas kito metabolizmą) arba netiesiogiai (veikdami tuos pačius tarpląstelinius taikinius). Antrųjų tarpininkų funkcija, taip pat jų formavimo (ar išsiskyrimo), skaidymo ir išskyrimo iš ląstelės reguliavimas, yra patogiai nagrinėjama cAMP pavyzdžiu. Šis antrasis tarpininkas yra sintetinamas veikiant adenilato citazei, suaktyvinus daugelį receptorių, konjuguotų su G baltymais. G s baltymas aktyvina adenilato ciklazę, G i baltymas slopina.
Yra mažiausiai 10 audiniui būdingų adenilato ciklotazės izoformų, kurios skiriasi aktyvumo reguliavimo mechanizmais.
Paprastai cAMP aktyvina baltymų kinazes A (nuo cAMP priklausomas baltymų kinazes), nedidelę susijusių baltymų grupę. Šios baltymų kinazės savo ruožtu fosforilina ne tik galutinius tarpląstelinius taikinius (fermentus, transportinius baltymus), bet ir kitas baltymų kinazes bei kitus reguliuojančius baltymus. Pastarieji apima, pavyzdžiui, transkripcijos veiksnius. Jie yra atsakingi už cAMP tarpininkaujamą genų transkripcijos reguliavimą, užtikrinant uždelstą ląstelės atsaką į signalą. Be baltymų kinazių aktyvavimo, cAMP veikia tiesiogiai katijoninės membranos kanalus, kurie vaidina svarbų vaidmenį, visų pirma, veikiant neuronams. Taigi signalas iš cAMP sukelia biocheminių pokyčių grandinę tikslinėje ląstelėje.
Kalcis Kitas gerai ištirtas antrasis tarpininkas yra tarpląstelinis Ca 2+. Ca 2+ jonai į citoplazmą patenka įvairiais būdais: palei membranos kanalus (priklausomus nuo G baltymų, priklausomus nuo įtampos, reguliuojamus K + arba Ca-Ca 2+), taip pat per kanalus, esančius specialiose endoplazminio retikulumo vietose ir atsiveriančius veikiant. IF 3 ir skeleto raumenyse dėl membranos depoliarizacijos. Kalcis iš citozolinės plazmos pašalinamas dviem būdais: jis absorbuojamas endoplazminio retikulumo būdu arba pašalinamas iš ląstelės. Ca 2+ perduoda signalus daug didesniam skaičiui baltymų nei cAMP - fermentai, dalyvaujantys ląstelių metabolizme, baltymų kinazės, kalcį jungiantys baltymai. Pastarosios sąveikauja su kitais galutiniais ir tarpiniais efektoriais.
Receptorių reguliavimas
Receptoriai ne tik kontroliuoja fiziologines ir biochemines funkcijas, bet ir tarnauja kaip reguliavimo objektai. Šis reguliavimas atliekamas jų makromolekulių sintezės ir skilimo lygmeniu, formuojant kovalentinius ryšius su kitomis molekulėmis, sąveikaujant su reguliuojančiais baltymais ir receptorių judėjimu. Konvertuojantys baltymai ir efektoriniai baltymai taip pat yra reguliuojami. Normatyviniai signalai gali būti gaunami iš tarpląstelinio perdavimo būdų, aktyvuojamų stimuliuojant patį receptorių (per grįžtamojo ryšio mechanizmą), taip pat iš kitų receptorių (tiesiogiai ar netiesiogiai).
Ilgalaikis vaistų receptorių stimuliavimas paprastai lemia reakcijos į jį sumažėjimą - esant tokiai pačiai koncentracijai, vaistas sukelia mažiau ryškų poveikį. Šis reiškinys, vadinamas desensibilizacija, refrakcija ir priklausomybe, vaidina svarbų vaidmenį klinikinėje praktikoje: pavyzdžiui, ilgai gydant β-adrenerginius agonistus pacientams, sergantiems AD, sumažėja reakcijos į šiuos vaistus sunkumas.
Homologinis desensibilizacija taikoma tik stimuliuotiems receptoriams ir būdinga ligandui. Dėl heterologinio desensibilizacijos sumažėja reakcijos į kitus ligandus, kurių receptoriai veikia tuo pačiu tarpląsteliniu signalo perdavimo keliu, sunkumas. Pirmuoju atveju neigiamą grįžtamąjį ryšį teikia poveikis pačiam receptoriui (fosforilinimas, proteolizė, sumažėjusi sintezė), antruoju atveju, be receptoriaus, jis gali paveikti ir kitus baltymus, susijusius su tarpląstelinio signalo perdavimu.
Priešingai, jei receptoriai ilgą laiką nėra stimuliuojami, padidėja jų jautrumas agonistams (pavyzdžiui, ilgą laiką gydant β-adrenoblokatoriaus propronololiu, padidėja β-adrenoblokatorių jautrumas β-adrenostimuliatoriams).
Sutrikimai dėl sutrikusios receptorių funkcijos
Be individualių jautrumo vaistams skirtumų, yra ir ligų, kurias sukelia kai kurių ląstelių signalo perdavimo iš receptorių į efektorių mechanizmo tam tikrų komponentų disfunkcija. Praradus labai specializuotų receptorių funkciją, fenotipinės ligos apraiškos gali būti ribotos (pavyzdžiui, sėklidžių feminizacija susijusi su genetiniu androgenų receptorių nebuvimu ar struktūriniais defektais). Jei pažeidžiamas universalesnis ląstelių signalo perdavimo mechanizmas, ligos simptomai būna įvairesni, pavyzdžiui, sergant myasthenia gravis ir kai kuriomis insulinui atsparaus cukrinio diabeto formomis, kurias atitinkamai sukelia N-cholinerginių receptorių ir insulino receptorių autoimuniniai disfunkcijos. Bet kurio komponento, susijusio su signalo perdavimu iš daugelio receptorių, defektai sukelia daugybinius endokrininius sutrikimus. Pavyzdys yra heterozigotinė G baltymų trūkumo forma, aktyvinanti adenilato ciklazę visose ląstelėse (Spiegel ir Weinstein, 1995). Tikėtina, kad homozigotinė šio baltymo trūkumo forma gali baigtis mirtimi.
Receptorių struktūros ar lokalizacijos sutrikimai gali pasireikšti kaip susilpnėjusi ar sustiprėjusi reakcija į vaistą, taip pat kaip kitas nepageidaujamas poveikis.
Mutacijos, koduojančios genų receptorius, gali pakeisti tiek reakciją į vienkartinį vaisto vartojimą, tiek ilgalaikio gydymo efektyvumą. Pavyzdžiui, β-adrenerginių receptorių, atsakingų už bronchų lygiųjų raumenų atpalaidavimą ir kvėpavimo takų atsparumo reguliavimą, trūkumas padidina šių receptorių jautrumo β-adrenostimuliatoriams sumažėjimą ilgalaikio AD sergančių pacientų gydymo metu. Nustačius mutacijas, sukeliančias sutrikusią receptorių funkciją, ir klonuojant atitinkamus genus, bus įmanoma sukurti tokių ligų gydymo metodus.
Receptorių klasifikacija
Tradiciškai vaistų receptoriai buvo nustatomi ir klasifikuojami remiantis selektyvių agonistų (stimuliatorių) ir antagonistų (blokatorių), kurie veikia šiuos receptorius, poveikiu ir santykiniu aktyvumu. Pavyzdžiui, acetilcholino poveikis, kuris atkuriamas sąveikaujant su cholinerginiais muskarino alkaloido receptoriais ir kurį blokuoja atropinas, yra vadinamas muskarininiu poveikiu, o poveikis, kuris atkuriamas sąveikaujant su cholinerginiais nikotino receptoriais, vadinamas nikotininiu poveikiu. Receptoriai, tarpininkaujantys muskarino ir nikotino poveikiui, vadinami atitinkamai M ir N cholinerginiais receptoriais. Nors tokia klasifikacija paprastai neatspindi narkotikų veikimo mechanizmo, patogu susisteminti jų poveikį. Iš tiesų teiginys, kad vaistas stimuliuoja tam tikro tipo receptorius, tuo pačiu lemia šio narkotiko ir medžiagų, kurios sustiprina arba silpnina šį poveikį, spektrą. Tačiau tokių teiginių galiojimas gali keistis nustačius naujų tipų ir potipių receptorius, atradus papildomus vaistų veikimo mechanizmus ar anksčiau nežinomą šalutinį poveikį.
Receptorių potipiai
Atsiradus vis gausėjančiai labai selektyvių vaistų įvairovei, tapo akivaizdu, kad anksčiau žinomi receptorių tipai yra suskirstyti į daugelį potipių. Molekulinio klonavimo metodai tapo reikšminga pagalba tiriant naujus receptorių potipius, o rekombinantinių receptorių paruošimas palengvino vaistų, selektyviai veikiančių šiuos receptorius, kūrimą. Skirtingi, bet susiję receptorių potipiai dažnai (nors ne visada) sąveikauja su skirtingais agonistais ir antagonistais. Receptoriai, kuriems nenustatyta selektyviųjų agonistų ar antagonistų, paprastai priklauso ne vienam potipiui, o to paties receptoriaus izoformoms.Skiriami potipiai taip pat gali skirtis tarpląstelinio signalo perdavimo mechanizmuose. M 1 ir M 3 cholinerginiai receptoriai, pavyzdžiui, veikia per baltymą G q, kuris aktyvina fosfolipazę C, netiesiogiai sukeldamas Ca 2+ išsiskyrimą iš viduląstelinių saugyklų, o M 2 ir M 4 cholinerginius receptorius per G i baltymą, kuris slopina adenilato ciklazę. Tuo pačiu metu receptorių suskirstymą į tipus ir potipius dažnai lemia ne veikimo mechanizmas, o atsitiktinis pasirinkimas arba jis grindžiamas nusistovėjusiomis idėjomis. Taigi α 1 -, α 2 - ir β-adrenerginiai receptoriai skiriasi pagal reakciją į vaistus ir signalų perdavimą (atitinkamai aktyvina baltymus G i, G q ir G s), nors α ir β adrenerginiai receptoriai yra skirtingų tipų, ir α1 - ir α 2 -adrenoreceptoriai - skirtingiems to paties tipo potipiams. Α 1 -adrenoreceptorių α 1A, α 1B ir α 1D izoformos mažai skiriasi savo biocheminėmis savybėmis; tas pats būdinga β-adrenerginių receptorių izoformrazių potipiams (β 1, β 2 ir β 3).
Skirtumai tarp receptorių potipių naudojami kuriant labai selektyvius vaistus, pavyzdžiui, vaistus, kurie turi skirtingą poveikį tam pačiam audiniui dėl prisijungimo prie receptorių potipių, kurie skiriasi tarpląstelinio signalo perdavimo mechanizmais. Be to, vaistai gali selektyviai nukreipti tam tikras ląsteles ar audinius, išreiškiančius potipio receptorius. Kuo didesnis vaistų selektyvumas (atsižvelgiant į tam tikrą audinį ar į tam tikrą poveikį), tuo palankesnis yra jo naudos ir nepageidaujamo poveikio santykis.
Naudojant molekulinius genetinius metodus, buvo atrastos ne tik skirtingos receptorių izoformos, bet ir genai, koduojantys naujus, anksčiau nežinomus receptorius. Daugelis šių receptorių jau priskiriami vienai ar kitai žinomai klasei, o jų funkcija buvo tiriama naudojant atitinkamus ligandus. Tačiau kai kuriems receptoriams dar nebuvo rasta ligandų.
Daugelio to paties receptoriaus izoformų, užkoduotų skirtingų genų, atradimas (ypač jei izoformos nesiskiria tarpląstelinio signalo perdavimo mechanizmuose ir sąveikauja su tais pačiais endogeniniais ligandais) leidžia receptorių ekspresiją skirtingose \u200b\u200bląstelėse nepriklausomai reguliuoti atsižvelgiant į kūno poreikius skirtinguose. amžiaus laikotarpiai.
Nereceptinių vaistų veikimas
Ne visi vaistai veikia per makromolekulines struktūras - receptorius. Kai kurie vaistai sąveikauja su mažomis molekulėmis ar jonais, esančiais kūne paprastai arba esant vienokiai ar kitokiai patologinei būklei. Taigi, antacidai neutralizuoja druskos rūgštį skrandyje. Mesna (vaistas, kuris greitai išsiskiria pro inkstus ir neutralizuoja laisvuosius radikalus) jungiasi su kai kurių priešnavikinių vaistų aktyviaisiais metabolitais, mažindamas nepageidaujamų reakcijų iš šlapimo takus sunkumą. Daugybė biologiškai neaktyvių medžiagų (pavyzdžiui, manitolio) gali būti įnešta tokiu kiekiu, kad padidėtų biologinių skysčių osmolariškumas ir taip būtų pakeistas tarpląstelinių ir tarpląstelinių skysčių pasiskirstymas. Su šių medžiagų pagalba galima padidinti diurezę, padidinti kraujospūdį, pašalinti smegenų edemą. Be to, jie naudojami kaip vidurius laisvinantys vaistai.
Kai kurie vaistai gali integruotis į ląstelės komponentus ir pakeisti jų funkcijas dėl struktūrinių panašumų su medžiagomis, kurios sudaro šiuos komponentus. Pavyzdžiui, purinų ir pirimidinų analogai įterpiami į nukleorūgštis ir naudojami kaip antivirusiniai ir priešnavikiniai agentai.
A.P. Viktoras "Klinikinė farmakologija"