工業用医薬品製造における点眼剤目次はじめに。
1.眼科用剤形の範囲と構造。
2.グローバル基金XIの要件。 目への投与形態。 彼らの
根拠と実装。
3.点眼薬の工業生産の特徴
4.スポイトチューブの製造技術。
5.目のソリューションの生産のための技術的プロセスとスキーム
チューブドロッパーとバイアル。
6.機械的封入のための点眼液の管理。
7.チューブスポイトで生成される点眼薬の命名法
バイアル8。 目の軟膏、GFソ連XI版の要件の実装、
命名法9。 目の固形剤形。その特徴と
命名法10。 フィルムフォーマーの範囲と特性。
11.アイフィルムの制作12.結論と提案13.参考文献。
はじめに目の品揃えと構造剤形。工業生産では、点眼剤、軟膏、フィルムなどの点眼剤が調製されます。 それらは、視覚器官の構造と機能に起因する特徴と関連して、薬物の目の組織や体液との吸収、分布、相互作用、目のわずかな脆弱性などの特徴に関連して、別のグループで際立っています。多くの目の病気では、透過性が劇的に変化します。 膜およびしばしば涙液中のリゾチーム(酵素ムロミダーゼ)の含有量が減少し、微生物への曝露に対する保護が低下します。 アイソリューション主に洗浄液、ローション、点眼薬、注射用製剤に代表されます。
目薬。 「点眼薬」という用語は、少量の結膜嚢への注入のための水溶液または油性溶液または薬物物質の最も薄い懸濁液である剤形を意味します(GF X、319条)。 医師の指示に従って、これらの物質の作用を延長するために、メチルセルロース、ナトリウムカルボキシメチルセルロースおよびポリビニルアルコールを溶媒に含めることができます。
目の懸濁液薬用物質の粉末の最も薄い懸濁液|水性または油性分散媒中
目の軟膏目の結膜に適用されたときに均一な連続膜を形成することができるソフトコンシステンシーの剤形です
固形剤形へ目のためには、目の丸薬、粉末、鉛筆が含まれます。
目の丸薬。これは、タブレットマシンを押します。
GGLP眼科薬用フィルム)。 生体溶解性であり、その組成に含まれる薬用物質を含む眼ポリマーの組織と適合性があり、ウイルス性、細菌性、アレルギー性およびその他の眼疾患の場合にこれらの物質を結膜腔に導入することを目的としています。 HFRは、9.0X4.5X0.35 mmの楕円形のプレートで、平均重量は0.015 gです。
all-Union Scientific Research Testing Institute of Medical TechnologyおよびMoscow Scientific Institute of Eye Diseasesにちなんで名付けられたソ連の日焼け ヘルムホルツ保健省、ソ連(ソ連著作権証明書No. 387559、1973年)。 この発明は、英国、米国、カナダ、ドイツ、フランスで特許を取得しています。
HLPは、軟膏、ドロップ、懸濁液、乳液、結膜下注射などの従来の点眼剤に比べて多くの重要な利点があります。
GF要件西編 目への投与形態。 それらの理論的根拠と実装。多くの最終剤形の一般的な要件に加えて、無菌性、安定性、等張性、機械的不純物と刺激作用の欠如、投与精度の要件が増加します。 これらの要件を満たすために、眼科用剤形の製造は注射用剤形と同じ方法で行われます。 最も重要な操作は、溶液の準備です。バイアルの充填とキャッピングは、周囲空気との接触を最小限に抑えた自動または半自動ラインの無菌空気の層流で、清浄度クラスAの部屋またはゾーンで実行されます。 これは特に無菌に当てはまります
加熱殺菌の対象ではない製造された製剤。 同様の要件が、出発医薬品および溶剤の品質にも課されています。 工業生産の特徴目薬。
剤形の製剤の分析により、点眼薬の割合は、わが国の薬局で製造されたすべての薬剤の即時製剤の約9〜19%であると結論付けることができます[Gendrolis A. A.、1973]。 このテーマに関する追加情報が蓄積されています。 したがって、E.I。Panchenko(1975)、V.N。Vilinbakova(1982)、I.R。Tashmukhamedova(1984)、R.S。Skulkova(1985)によると、過去10年間にわたる自立型の薬局での点眼薬の即時処方 13.2-18.4%に達し、この期間中に病院の薬局で点眼薬の8.2-8.9%が作られました[Panchenko E.I.、1983; Kuznetsova A.P.、1984]。 病院の眼科では、点眼薬の生産の割合が50-60に達したことを強調することが重要です[N. Bryleva、1984; Kuznetsova A.P.、1984]。
さらに、最も一般的な点眼薬は、スルファシルナトリウム、硫酸アトロピン、ホウ酸を含む硫酸亜鉛、さまざまな濃度の塩酸ピロカルピンなどの溶液であることが判明しました。 ビタミンや他の薬用物質。ただし、このような場合、化学化合物とそれらの非互換性の可能性のある拮抗作用を考慮する必要があります。
点眼薬は、診断、予防、治療のための薬物投与の最も単純な形態です。
目の病気。 点眼剤の水溶液の点滴は簡単で、患者自身が簡単に行うことができます。 しかし、眼、特に点眼剤の局所投与には、患者と医療従事者からの特定の規則を厳守する必要があり、眼液自体に特別な要件が課せられます。
ソ連IX版の州薬局方を含む国内薬局方には、特別な一般的な記事はなく、一般に点眼薬の品質と条件を管理するガイドラインはありませんでした。 このギャップは、ソ連の州薬局方の版でのみ埋められました。
しかし、眼科学と薬学の現代の進歩に照らして、目のソリューションの品質は間違いなくさらに高い要件を満たす必要があり、それは次のように定式化できます。 目の溶液は、無菌、等張、保存中安定、透明で機械的不純物がなく、毒性および刺激性の影響がなく、場合によっては長期の治療効果があり、目の溶液中の薬物は正確な濃度であり、 最大の生物学的活性を示すため、使用に便利なパッケージに眼液を分注する必要があります。
眼科用剤形の製造においては、主に視覚器官に対する薬物の効果の安全性を確保する無菌性および等張性の原則を遵守することに特に注意を払う必要があります。
不妊の原理:通常、涙液には特別な抗生物質が含まれていることが知られています-リゾチーム(現代の酵素分類-KF 3.2.1.17、ムロミダーゼと呼ばれる)は、結膜に入る微生物を溶解する能力があります[Bukharin O. V.、Vasiliev N. V.、 1974]。
主要な成分が大きなポリマーであり、2つの共有結合した成分からなる、厚さが15〜50μmの比較的単純な細胞壁を持つグラム陽性微生物は、リゾチームに最も敏感です。 それらの1つはペプチドグリカン(ムレインまたはムコペプチド)であり、細胞に形状と強度を与え、高い内部浸透圧に耐えることができる剛性の繊維構造を形成します。 別の成分は、細胞表面の強い極性を提供する置換ポリ-(O-リボトール-5-リン酸)であるテイコ酸であり、場合によっては、リゾチームの影響下で、グラム陰性培養物の部分的または完全な溶解が観察されます。 しかし、グラム陰性菌の壁はもっと複雑です。 壁セクションのさまざまなコンポーネントは、外膜と呼ばれる厚さ6〜10 nmの構造を形成します。これは、内部に疎水性セクションがあり、表面が親水性の二重脂質層です。 外膜の主成分は、非常に複雑なリポ多糖、リン脂質(ホスファチジルエタノールアミン、ホスファチジルグリセロール)、脂肪酸、および特殊な機能を持つタンパク質です。 ほとんどの眼疾患では、涙液中のリゾチームの含有量が減少し、その結果、微生物の影響から眼が十分に保護されないため、非滅菌薬の使用は深刻な結果をもたらし、時には視力喪失につながる可能性があります[A. Gendrolis、I. Deltuvene、1976]。
この点で、目の薬の要件は注射液に提供されるものと同様である必要があり、準備措置の性質と技術プロセスの条件に従って、目の薬と注射液は次のように考えることができると考える十分な理由があります 単一の全体。 ただし、この統一は制限されていません。
技術面は1つだけです。 さらなる資料からわかるように、眼の薬物の薬物動態特性も注射液の薬物動態特性とかなり類似しています。
目および注射液の微生物汚染および薬物の腐敗の防止に関連する問題の解決策は、活性物質の含有量と比較してかなりの量の液相を有するシステムであるこれらの薬物において、好ましい条件が作成されるという事実に特に関連している 微生物の繁殖のために。 これらの条件は、溶液中の活性物質の濃度が低いことと、場合によっては微生物の栄養培地である成分が存在することに起因します。
薬物の播種のリスクの程度は、病原性微生物叢の存在、さまざまな反応(酸化、還元、重合など)を開始する発生中の微生物への暴露による薬物の分解生成物の性質など、多くの要因に依存します。 医薬製剤の微生物感染は、製剤、保管、輸送、および使用のすべての段階で発生しますが、ほとんどの場合、栄養微生物相は腐生形態に代表されます。 それにもかかわらず、その存在は、衛生的および衛生的な観点からだけでなく、微生物の播種が細菌酵素の作用下で薬物の分解を促進し、その劣化につながるため、薬物の化学的安定性を維持する観点からも受け入れられません。 したがって、眼科用剤形の調製のための無菌条件が重要になり、これは多くの専門家によって強調されています。 ただし、このような条件は、微生物汚染からの溶液(点眼薬を含む)の完全な保護を保証するものではなく[Besedina I.V. et al。、1981]、および19世紀と20世紀の変わり目に現れた「滅菌」自体の用語です。 と意味
「担保化」もかなり相対的です。 それは、溶液中の(または異なる凝集状態の物質中の)微生物の破壊、または微生物(および他の汚染物質)、特に細菌の重要な産物の滅菌対象からの除去を意味します[Rabinskiy B. Ya。、1981]。 前者の場合、これは物体の熱的、化学的、または放射線処理の方法を使用して達成され、後者の場合は遠心分離、ろ過、凝集、静電気の使用などによって達成されます。
眼科薬の微生物汚染と腐敗を防ぐために、業界ではさまざまな方法が使用されており、厳密な無菌条件下で適切な薬を入手することを可能にし、将来、無菌性の保証を高めるために、安定性を保証する技術を使用してこの薬を滅菌します。 現在、現代の生産には、製造された薬物と微生物による潜在的な汚染源、例えば人の手との接触を完全に排除し、空気のない環境、空気のない空間、または不活性ガス環境での薬物の放出を可能にする技術的能力があります。
厳格な無菌規則の順守は、同様に、殺菌された微生物を含む眼科薬を製造する薬局や製薬会社の仕事の前提条件でもあります。 それらによって分泌される毒素、その多くは高温で安定しています。
熱処理を受けない眼科用医薬品、熱不安定性薬物を含む粉末、乳濁液および懸濁液の製造における無菌剤の役割。加熱すると再結晶のプロセスが急激に増加し、特に増加します。
凝集と合体。 これらの場合、無菌ルールの順守は、製造される医薬品の適切な品質を確保する唯一の方法です。
実際には、これは、無菌条件下で懸濁した熱不安定性物質を滅菌容器内の事前に滅菌した溶媒または軟膏基剤に溶解し、必要に応じて防腐剤と安定剤を添加することで達成されます。 これらの操作は、特別な無菌店、ブロック、箱で行われます。
今日まで、目の薬の滅菌に関連する問題の開発において集中的な研究が行われてきました。 B.V. Nazarov(1972)は、薬局の条件で点眼薬を製造する際に利用可能な経験を要約し、点眼薬の組成物に使用される薬剤を滅菌中の安定性に従って次のように分類しています。
I.薬用物質、その水溶液は、安定剤を添加せずに100℃の温度で30分間の滅菌に耐えます。
点眼薬を組み合わせた溶媒(ホウ酸1.9%とクロラムフェニコール0.2%の水溶液)で調製できる物質のグループ。 この溶媒(pH 5.0)では、酸性反応を起こす物質で点眼剤を準備できます。 100℃の温度で30分間の滅菌に耐えます。 次の点眼薬の製造に使用されます(保管期間は、密封されたパッケージの入手可能性に応じて示されます。
安定したソリューションを作成するには、ほとんどお勧めできません
ソ連保健省の薬理委員会によって承認された方法論。 蒸留水で調製したスルファシルナトリウムの20〜30%溶液1リットルに、0.5%メタ重亜硫酸ナトリウム溶液と18mlの1N水酸化ナトリウム溶液を加えます。 得られた溶液を100℃の温度で30分間滅菌しました 密封包装(ペニシリンバイアル)では、このソリューションは1年間安定です。 保管中に白色の連鎖球菌である結晶性沈殿物の沈殿を防ぐために、水酸化ナトリウム溶液の添加が必要です。
エチルモルヒネ1.2および3%注射用に水で作ることができ、0.1%メタ重亜硫酸ナトリウム溶液が安定剤として加えられ、0.7%塩化ナトリウム溶液が等張性のために加えられます。 溶液は100℃の温度で30分間滅菌されます。
薬局でのオートクレーブによる点眼液の滅菌の可能性に関する研究は、L。V. Polyakova et al。 (1977)。 ベラルーシの眼科診療で使用される以下のソリューションは、研究の対象でした:
滅菌蒸留水を使用した点眼薬の溶液を調製するために、作業は無菌条件下で行われました。 等張性を提供する物質として、塩化ナトリウムまたはホウ酸が使用された。 エチルモルヒネ塩酸塩溶液は、メタ重亜硫酸ナトリウムの添加により安定化されました。 調製した溶液をNS-1ブランドのペニシリンバイアルに包装し、金属キャップを使用して慣らしをするためのゴム栓で栓をし、119〜121°С(0.1〜1.1 atm)の温度でオートクレーブで8分間滅菌しました。
滅菌と保管中に最も安定したのは、アミドピリン、硫酸アトロピン、臭化水素酸ホマトロピン、塩酸エフェドリン、ジフェンヒドラミンの溶液でしたが、これらの製剤では、加齢を加速して研究した後、60°Cの温度で22日間サーモスタットに保管しました(1年間の保管に対応) 通常の状態)副産物の痕跡が見つかりました。 エチルモルヒネ塩酸塩の溶液は、安定性が最も低く、滅菌直後と5〜8日後に少量の分解生成物が現れました。 ストレージソリューションが黄色に変わりました。
現在までのすべての既知の滅菌方法の有効性を評価する主な方法は定量的方法であり、その本質は数の比率を決定することです
滅菌の前後に実行可能な微生物叢。 この評価は、滅菌プロセスに関する長年の研究の結果であり、微生物叢からの解放は微生物の完全な除去または破壊を意味するものではなく、実際には微生物含有量の部分的な減少にすぎないことを示しました。 同時に、その状態は一般的に受け入れられている物体の無菌性の指定として認識され、「14日以内(温度37°C)で滅菌バイオアッセイとして受け入れられる培養物の成長はありません」。
したがって、「無菌性」の概念は非常に相対的であり、一定レベル以下の微生物数の減少のみを示しています。 滅菌方法の効率が向上すると、細菌汚染のレベルは徐々に低下し、国際規格で規制された値になります。
表2.蒸気の作用に対する一部の微生物の耐性耐性度™(最小)。微生物を介して。 80°С1№СWC134-CH 私は . マラリア原虫 1-5優しさアクティブですべん毛 — __ _ _ ウイルス — — — — 議論の余地のないフォーム — — — ~ 酵母 — — — . — かびの生えた — — — — 酵母の胞子と 5-10 1非アクティブ
かびbac菌ポニーのbac菌 ジンジャ-1-60、1ネツィアズネ-ケショイ耐久性 アクティブアクティブ枯草菌の胞子が増加 -60分8から私は日よけの耐久性 最大60時間で_____________________ ^^_^^________ .................................. .............................. __ _^ ^_
海外では、汚染の最大許容値の値は、殺菌剤の影響に対する特定の微生物の耐性に基づいて決定されます。 このように、ドイツおよび他の多くの国では、蒸気に対する耐性に応じた微生物の分類が採用されており、微生物汚染の下限を設定することができます。 実験が示したように、ほとんどの点眼薬は滅菌されておらず、1日目と2日目に調製された溶液で見つかった微生物の数に有意な差は観察されませんでした。 著者
また、最大許容基準を大幅に超える量の微生物が含まれていた製造後1〜2か月で、国内工場で調製されたアルミン0.005%溶液とホスファコール1:7500溶液などの点眼薬もあります。 この点で、工場における点眼剤の製造のための技術的条件には、許容される最大細菌含有量の表示とともに、微生物学的純度を確認する要件を必ず含めることが推奨されます。 点眼薬の無菌性は、特にねじ込み式ピペット付きのボトルを使用する場合は特に、患者の精度にも大きく依存します。 これはP. Ellis(1981)によっても報告されており、熱処理によって提供される点眼薬の無菌性は、患者が使用するまで持続することを示しています。 これに関して、生理的耐性の原理に違反することなく、使用期間全体を通して消毒効果を有する物質を選択し、点眼剤に導入する問題は依然として重要である。
等張性の原理。
眼科医が処方する滴剤は通常、組成、pH、およびその他の特性が涙液と同一ではないため、等張性は点眼剤などの剤形の調製に絶対に必要な条件です。 同時に、高張液と低張液の両方が患者によって許容されにくいことが知られています。 これは、浸透圧の差の結果として大きな浸透圧(7.4気圧以上)の溶液が導入されると、溶液と接触している細胞から水が放出され、しわが発生するためです。 浸透圧の小さな溶液を導入すると、細胞が膨張し、細胞膜が破裂しますが、どちらの場合も、これらの現象には激しい痛みが伴います。 したがって、薬剤師の仕事は、そのような浸透圧が対応する滴を調製することです
涙液の浸透圧になります。 等張濃度を計算する方法の1つは、ヴァンゴフの法則に基づいており、その助けを借りて、希釈された非電解質溶液の等張濃度を決定することが可能です。 この場合の浸透圧、濃度、温度の関係は、クラペイロンの式で表すことができます。これから、非電解質の等張溶液を調製するには、溶液1リットルあたりp、29 g / molのこの物質を摂取する必要があります 電解質の等張濃度を計算するとき、等張係数と呼ばれる補正係数がクラペイロン方程式に導入されます。 完全に解離する電解質の溶液の場合、約0.143で、弱く解離する電解質の溶液の場合、0.2です。 溶液の等張濃度を計算するためのより普遍的で正確な方法は、GF X(p。997)に記載されている、塩化ナトリウムの薬物のいわゆる等張性等価物の使用に基づく方法です。 等張濃度は、血漿と対応する医薬品の溶液[Azhghikhin I. S、1975]。 以下の最も一般的な点眼薬をリストできますが、注射用に水のみで調製されている場合は、等張濃度にする必要があります。
現在、緩衝溶媒で点眼薬を調製する方法は、ますます製薬業務に導入されています。 バッファー溶媒の使用は、化学的安定性の向上とともに、場合によっては点眼薬の薬物成分の治療活性を高め、眼球領域の不快感を軽減するのに役立ちます。ほとんどの場合、ホウ酸塩(1.9%ホウ酸溶液)は点眼薬の溶媒として使用されます。 酸および2.68%四ホウ酸ナトリウム溶液)、ホウ酸-酢酸塩(1.9%ホウ酸溶液および1.5%酢酸ナトリウム溶液)、ホウ酸-プロピオン酸塩(1.9%ホウ酸溶液) sおよびプロピオン酸ナトリウムの2%溶液)およびリン酸(一置換リン酸ナトリウムの2.55%溶液および二置換リン酸ナトリウムの1.85%溶液)緩衝液緩衝溶媒の点眼薬の調製は、そのような緩衝液、組成および 剤形中の原薬の安定性を最大化します。
海外では、特定のpH値を維持するための緩衝能力を有し、涙液と等張性の点眼薬用溶媒の他の処方も提案されています。 適切に選択された溶媒により、水素イオンの濃度を調整して溶液を安定化するだけでなく、薬用物質が最大の治療効果を発揮するpH値を作成することができます。 例として、pH約5.0の1.9%のホウ酸等張液が推奨されます。これは、亜鉛塩、コカイン、ノボカインなどを含む点眼剤の調製に推奨されます。
点眼薬を含む眼液を安定させるために、緩衝液とは別の試薬が使用されます。 近年、点眼薬の等張性と安定性の要件が考慮されています
大多数の研究者。 ポリマー包装における点眼薬の安定した溶液の製造に関連する問題は、研究者の注目を集めています[Gendrolis A. A.、1969、1971、1973、1974、1977; Artemyev A. M.、Kuzmina L. I.、1977、およびその他]。 Yu。I.、Zelikson(1969)によって得られた実験データによると、0.2%レボミセチンを含むホウ酸の1.9%溶液で調製した塩酸ピロカルピンの1%溶液と硫酸アトロピンの1%溶液の点眼薬は、滅菌中安定でした。 およびストレージ。 これらの溶液では、蒸留水で調製した溶液と比較して、pHの小さな変化が観察されました。 そのような溶液の安定性、保存性、等張性を考慮して、著者は、アルカロイド塩、合成窒素塩基、酸性環境で安定な他の薬用物質を含む点眼薬の溶媒としてこの組み合わせを使用することを推奨しました。 同時に、Y。I. Zeliksonにより、ホウ酸およびリン酸緩衝液(pH 6.6〜7.1)で調製された塩酸ピロカルピンと硫酸アトロピンの溶液は、100°Cで30分間の流体蒸気による滅菌後に不安定になることが判明しました。 min:1か月後、薬物の分解が起こり、初期活動の5〜31%のみが保存されます。 したがって、6.6〜7.1のpHを有する緩衝溶媒での点眼剤の調製は、それらに導入される成分の物理化学的特性のみを考慮に入れるべきであり、この溶媒は主に薬局の即時診療でのみ適しています。 場合によっては、緩衝液が点眼薬の調製に積極的な役割を果たすという事実にもかかわらず、この目的のためにそれらを使用する必要性は、多くの研究者によって長い間疑問視されてきました。 そのため、1961年にK. Munzelは、pH値を6.0〜8.0の範囲内に維持する必要がある場合にのみ、目薬の溶液に緩衝剤を導入する必要があると書いています。 点眼薬のpHがこの範囲を超えない場合、
著者によれば、これらの剤形の組成における緩衝液の使用は、この場合の涙液自体が天然の緩衝液の役割を果たすため、実用的ではありません。 A. Poffs(1965)も同じ結論に達しました。A。Poffsは、緩衝液は、pHが生理学的に許容される基準から著しく逸脱する剤形でのみ投与されるべきだと提案しました。 これらの問題の議論の関連性は、眼液の治療活性の水素イオン濃度への依存性に関する不十分な知識に関連しています。 多くの研究者は、一部の溶液の生理活性が7.0以上のpHで増加することを示しています。 これに基づいて、pH値を上げることができる溶媒に点眼薬を準備することが提案されました。 7.0以上。 しかし、R。DynakovskiとR. Figwiski(1972)は、酸性溶液に対するこのような溶液の利点を疑問視していました。 今日まで、これらの質問に対する明確な回答は得られていないため、点眼薬の製造技術とこの剤形の品質を改善するには、この方向でのさらなる研究が必要です。
チューブ製造技術ドロッパー。ポリマー包装の点眼薬の製造分野でのカウナス内分泌薬工場の15年間の運用を通じて、これらの眼科用製剤の大規模生産でかなりの経験が積まれてきました。 しかし、生産方法の継続的な改善にもかかわらず、緊急の解決策を必要とする新しい疑問が生じます。
主な問題は、その解決策が経済的であるだけでなく、薬物の有効期間を延長する可能性の研究である。
価値だけでなく、大部分はこのグループの薬物の質の状態を反映している[Tentsova A.I. et al。、1978; Babayan 3. A. et al。、1984]。現在、0.5±0.1 mmの肉厚のチューブスポイトで製造された点眼剤の有効期間は、溶液からの水分の蒸発により2年を超えません。 目薬が壁厚0.6-0.75 mmのスポイトチューブに詰められ、これらの剤形の有効成分の濃度範囲に対する既存の許容範囲が拡張されている場合、目薬の有効期間を延長できる可能性を示す実験データがあります。 。 1
厚紙製のマイクロパケットの代わりに、ポリ塩化ビニルフィルム(厚さ0.4 mm)とラッカー塗装アルミニウム箔(厚さ0.05 mm)で作られた「Servak」タイプの輪郭パッケージにさまざまな準備をしたチューブドロッパーを保管する研究も行われています[A.Gendrolis。 、ズブカイトG.P.、1977]。 得られたデータにより、点眼薬の有効期間を延長できる可能性が確認されました。さらに「ポリマー包装における点眼薬の生産を改善する別の方向性は、チューブの条件付き無菌チューブの生産方法の提案です
スポイト:現在の技術を使用したスポイトチューブケースの製造では、チューブの表面が汚染されており、洗浄と滅菌が必要でした。 この欠点を解消するために、動作原理が次のようなデバイスが提案されました(図1を参照)。
1)コンベヤーベルトの端およびチューブ付きの運搬ブロック
吹く機械1、ブロックを運ぶコンベヤーを置いて下さい
パンチングスタンプ8;
2)コンベアの最後に、専用のレシーバーを設置します
ブロック7の蓄積;
3)床にセットされたパンチングスタンプ8の下に滅菌Bix
カットアウトチューブドロッパー用の蓋付き9;
4)コンベヤーベルトの表面は容易に取り外し可能に塗られる
フィルムとキャップ付き
環境との接触を排除します。
5)輸送テープの滅菌のために、ローラー3、4、5が取り付けられ、
定期的に消毒剤で保湿します。
6)レシーバー7からのチューブを備えたブロックは、ゲートの端で取られます(
チューブに触れます)、彫刻用のダイカットスタンプ8に置きます
チューブ。
このようにして、表面汚染のないスポイト管の条件付き滅菌ケースが得られます。 記載されている技術プロセスの結果として、その後のチューブの洗浄を中止し、生産の文化を高めることができる条件が作成されます。
スポイトチューブハウジングの半球をトリミングすると、チューブの滅菌開口部が汚れ、その結果、カットオフtKopnycaも洗浄、乾燥、ガス滅菌する必要があります。
チューブドロッパーの無菌カットオフケースを取得する方法が開発されました。これは次のように実装されます。
1)半球トリミング装置は、チューブ供給とカニューレのねじ込み領域の間のアセンブリコンベア上のスポイトチューブを充填および密封する自動アセンブリユニットに配置されます。2)スイベルスプロケットの高さを上げて、
チューブ全体を転送する機能; 3)チューブの半球を切断するためのデバイスは、
ベッド、ガイド、上下のナイフ。 下のナイフは
ライザー、およびトップ-ガイドへ。 上メスを調整するには
編み装置。 ガイド移動
自動設置の中央シャフトのトランスミッションによって提供され、
切り欠きのある円盤が取り付けられます; 4)チューブドロッパーのケースのカットされた半球が押し出されます
全体を接続した後、特別な箱の漏斗を通して機械
換気システム。
提案されたデバイスでは、チューブドロッパーの4つのケースを一度にトリミングすることが可能であり、その後、輸送セルによってカニューレをねじ込んで充填するための領域に輸送されます。
この方法により、洗浄プロセス、チューブドロッパーボディのガス滅菌を放棄し、技術サイクルの時間を大幅に短縮し、複数の人を解放し、材料の節約(エチレンオキシド、二酸化炭素、蒸留水)、電気、さらに複雑な設備を設置する必要もなくなります 容器および最終製品中のエチレンオキシドの残留物を測定するための機器。
技術プロセスとスキームチューブ内の目のためのソリューションの生産ドロッパーとボトル。スポイトチューブのソリューションは、無菌条件下でクラスBの清浄度の部屋で準備されます。 部屋と機器は湿式洗浄され、3-5%フェノール溶液で消毒され、殺菌灯で2時間殺菌されます。溶解は攪拌機付きの反応器で行われ、分析され、溶液から機械的不純物が取り除かれ、滅菌濾過され、滅菌装置で収集され、その後チューブに充填されます ドロッパー。
これと並行して、チューブドロッパーのケースとキャップが作成されます。
1.5±0.15 mlの容量と0.5±0.1 mmの壁厚を備えた本体は、高圧ポリエチレンブランド15803-020または16803-070の顆粒からブロー成形およびスタンピングすることにより、いくつかの段階で機械に形成されます。 穿刺用のピンが付いたキャップは、低圧ポリエチレングレード20906-040または20506-007の溶融顆粒から圧力下で注がれます。 製造後、それらは蒸留水で洗浄され、乾燥され、エチレンオキシドと10%二酸化炭素の混合物で40〜50で2時間ガス滅菌されます。エチレンオキシドは、無菌室で12時間保管することにより製品から除去されます。 次に、無菌条件下で、滅菌空気が過剰な圧力のユニットで、キャップを身体にねじ込み、定量ポンプを使用して薬液の溶液を満たし、ヒートシールで密封します。 印刷機では、薬物の名前の刻印が身体の両側に適用され、その濃度と量が示されます。 充填されたチューブスポイトは、60 Wの電灯で照らされたときに、白黒の背景に機械的な不純物がないかどうかを視覚的にチェックし、各バッチの5%が完全な分析にかけられます。 スポイトチューブは、単一のケース、段ボール箱、またはポリ塩化ビニルフィルムに梱包されています。
GOST 17768–80によると、このパッケージに加えて、安定化されていない低密度ポリエチレン製のストッパーピペットを備えたガラスボトルが目薬に推奨されます。 充填する前に、溶液は濾過により滅菌され、ピペット管は10%の二酸化炭素を含むエチレンオキシドによるガス滅菌により滅菌されます。
上の点眼液の制御機械的介在物。点眼薬は完全に透明で、自由であるべきです機械的損傷を引き起こす可能性のある浮遊粒子はありません目の膜。 点眼薬は、最高の品種でフィルタリングする必要があります。ろ紙、そしてフィルターの下に置く必要があります長い繊維ウールの小さな塊。 重要なのはろ過、溶液の濃度および総質量は減少しませんでした確立された標準で許可されている以上。 すべてが言った少量のソリューションを完全にフィルタリングすることについて(p。396を参照)、主に点眼薬を指します。 レシピによく見られるレシピによると、薬局内ブランクの助けを借りることをお勧めします-少量の液体のろ過を免除する時間通りに準備された濃縮物。
チューブスポイトとバイアルで生成される点眼薬の命名法。
現在利用可能な目の投与形態の品揃え
スポイトチューブの工場時間はまだ短く、確かにさらなる拡張が必要です。 ただし、この問題は単純ではなく、簡単に解決できるものではありません。医薬品の新しい名前ごとの技術標準の開発は、多くの質問の解決に関連しているためです。 まず、膨大な数の眼科薬の処方の中から、全国の眼科診療、または少なくとも大規模な入植地で常に見られるものを選択して分析する必要があります。 次に、薬物物質の最も一般的に使用される濃度を決定する必要があり、これらの値は十分に安定であるか、安定剤の添加により一定レベルに維持される必要があります。 最後に、原薬自体と薬物の他の成分の両方を分析するための適切な方法が利用可能または開発されなければなりません。 これができて初めて、製造、滅菌、保管条件でのポリマー包装材料と医薬品の溶液との相互作用の研究を開始できます。 長期にわたって継続することがあるこれらの研究の最終段階では、否定的な結果が得られる可能性があることに留意する必要があります。 この場合、最初からやり直して、他の最適なオプションを探し続ける必要があります。
医薬品の溶液を洗浄する方法は、無菌性を確保するとともに、新しい包装形態の点眼薬の工業生産における同様に重要な問題は、溶液に機械的不純物がないことです。 それを解決するために、2つの方向で適切な対策を実施することが計画されています。すなわち、薬用物質の溶液の洗浄と、産業施設の産業の清潔さの維持です。
点眼液の凍結プロセスがそれらの物理化学的特性に及ぼす影響に関する研究の結果に基づいて、適切な記録が保管セクションに記載されました。
薬局方の記事:「輸送および保管中の凍結は、その使用の禁忌ではありません。」
同時に、保存期間を延長する可能性を研究するために、凍結した状態でポリマーパッケージに点眼薬を保存する追加の実験が行われました。 実験のために、スルファシルナトリウム(20%)および硫酸亜鉛(0.25%)とホウ酸(2%)の調製物が、幅広い[産業規模]で産業界によって生産されました。 点眼薬は-10±2°Cの温度で保管し、一定の間隔で薬局方の要件に準拠しているかどうかの定性的および定量的な指標を確認しました。
現在、この方向での作業が進行中です。 点眼薬の保存期間を延長し、プラスチック容器の製造技術を改善
ポリマー包装の点眼剤の製造分野でのカウナス内分泌薬工場の15年間の運用を通じて、これらの眼科用製剤の大規模生産でかなりの経験が積まれてきました。 しかし、生産方法vの継続的な改善にもかかわらず、緊急の解決策を必要とする新しい疑問が生じます。
主な問題は、その解決策が経済的に重要であるだけでなく、このグループの薬物の品質状態を大きく反映するため、薬物の有効期間を延ばす可能性の研究である[Tentsova A. I. et al。、1978; Babayan E.A. et al。、1984]、。
眼軟膏、GFソ連の要件の実装西出版物、命名法。
眼軟膏は、目の結膜に適用されたときに均一な連続膜を形成することができるソフトコンシステンシーの剤形です。 古代の剤形である眼軟膏は、最近、その調製技術、および主にその基剤および包装形態の組成の両方に関連する多くの変化を受けています。 有効成分の服用時の投与量の正確性、基剤の安定性および無関心を確保するために、眼軟膏はできるだけ均一に基剤に医薬品を分布させるための一般的な要件に加えて、次の条件を満たす必要があります:
次の条件:1)軟膏基剤に不溶の医薬物質は、最小限の分散度まで粉砕する必要があります。これにより、粘膜が完全に保存され、軟膏を塗布する際の不快感がなくなります。 2)軟膏基剤には異物や不純物が含まれてはならず、無菌、中性、結膜および眼の粘膜上に容易かつ均一に分布している必要があります。 3)眼軟膏は、無菌規則を厳守して準備する必要があります。 4)軟膏のpHは涙液のpHに対応する必要があります。そうしないと、涙液が分泌され、それに関連する薬物が急速に浸出するためです。
眼軟膏は、まぶたの皮膚や縁を滑らかにするために、または結膜嚢に配置するために使用されます。
潤滑は、ガラスまたはプラスチックのスティックを使用して行われ、結膜嚢への敷設は、以前に下眼lidを引っ張ったスパチュラを使用して行われます。 眼に感染を引き起こす可能性があるため、指を使って軟膏を塗ったり、洗浄したりすることは受け入れられません。 軟膏を敷いた後、閉じた状態でまぶたを優しくマッサージして、薬のより良い分布を達成します。 残念ながら、目の軟膏の製造に使用される軟膏基剤の範囲は小さく、ゆっくりと拡大しています。 基礎として、GF Xは「眼軟膏用」ワセリングレード(90部)と根のないラノリン(10部)の混合物を推奨しています。 純粋な石油ゼリーに対するこの混合物の利点は、後者が涙液で十分に濡れず、その結果、結膜全体に不均一に分布することです。
近年、より効果的な組成物が提案されています。 したがって、スルファシルナトリウムを含む軟膏には、ワセリン、水、流動パラフィン、無水ラノリンの混合物(7:5:3:6)が推奨されます。 ウールワックスのアルコールは、眼の軟膏基剤でますます使用されています(GDR VIIの薬局方)。
1968年、ウール、ワックス、セレシン、パラフィンオイル、ワセリンのアルコールを4:24:60:10の割合で含むベースがKHNHFIで開発されました。このタイプのベースは「オイセリン」という名前で知られています。 わが国では、抗生物質の可能なキャリアとして調査され、実施された作業の結果、ジビオマイシンおよびジテトラサイクリン眼軟膏の放出を可能にする肯定的な結果が得られました。
一部の著者は、酸価が低く、刺激作用、感作作用、アレルギー作用がないことを特徴とする加水分解水素化ラノリンの眼軟膏への使用を提案しています[Barura G. S. et al。、1968; アリューシンM.T.、リーV.N.、1971年]。 |ハイドロラインを含むベースの別の成分として、ワセリンが推奨されます(通常、ハイドロリン9部に対してワセリン1部)。 これに基づく軟膏は、抗生物質の担体としてこの基剤を使用する理由である高い安定性によって特徴付けられます。 I. S. Azhgikhikhin V. G. Gandel(1972)、V。M. Gretsky(1975)は、他の剤形では、治療における基剤の役割は軟膏のように決定することではないと強調しています。 著者は、基剤を含む軟膏が、それが適用された皮膚または粘膜のその領域の病理学的プロセス中の状態、特性、応答に大きな影響を与えることを示しています。 同時に、塩基はそこに導入された医薬物質と複雑な相互作用を起こし、その安定性を改善または悪化させ、その送達および吸収に寄与または妨害し、その薬理学的および治療効果を強化または弱体化し、さまざまな副作用の発現にも著しく影響します 原薬の効果。
基剤が特に示されていない場合、眼軟膏の一般的な要件を定めているGP Xの709項によると、眼軟膏の製造では、無水ラノリン10部とワセリン90部の前述の組成が使用されます。 すべての水溶性医薬品(塩
アルカロイド、ノボカイン、銀製剤など)は、注射用の最小量の水に溶解し、その後、ベースの組成物に導入されます。 不溶性または難溶性の物質-黄色の酸化水銀、塩基性硝酸ビスマス、アミド塩化物、および一塩化水銀、ゼロフォーム、酸化亜鉛、クエン酸銅は、少量の液体パラフィン、グリセロール、または水でさらに徹底的に粉砕した後、最高の粉末の形でベースに導入されます 軟膏を作るためにベースが使用される組成。
塩基性物質の不溶性薬物の分布の均一性の確認は、スライドを使用して視覚的にGF Xに従って実行されます。 しかし、軟膏の工業生産で証明されているこの目的のために、スクリーン付きの特別な走査顕微鏡を使用する方がより完璧です。
眼軟膏の包装には、主に内面にニスを塗った金属チューブを使用して、金属が薬物と接触するのを防ぎます。 それでも、金属と相互作用する可能性のある成分を含む軟膏を梱包するときは、金属チューブを使用しないでください。 軟膏の1回限りの包装用のポリマー材料がより広く普及しています。
目のための固体剤形。特徴と命名法。
目の固形剤形には、眼科用錠剤、粉末、鉛筆が含まれます。
目の丸薬。 これは、タブレットマシンでの圧縮によって得られる剤形です。 目の丸薬は二重です。
目的:下まぶたの後ろに置くことで直接使用するか、点眼薬、またはあまり一般的ではないが、目薬を得るためにそれらを事前に溶解するために使用できます。 どちらの場合も、錠剤は適切な溶媒(通常は注射用水)に残留することなく容易に溶解し、刺激性または外傷性の目の成分を含まない必要があります。
このタイプのピルは、アメリカ企業のバローウェルカムとパークデイビスが乳糖と可溶性澱粉をベースにしたアイタブレットの製造を開始した前世紀の終わりに登場しました。 ロシアでは、最初の目薬は1898年に作られ、コカインとアトロピンの混合物が含まれていました。 それらは水に容易に溶解し、下結膜嚢に置かれた場合、眼に弱い、急速に通過する刺激を引き起こしました。 その後、主に海外からの錠剤がロシアで使用されるようになりました。 したがって、1912年に、A。S.ケモロソフは、乳糖に基づいて製造された外国製の目薬の効果をテストしました。 錠剤は無菌条件下で調製されました。当時、眼科で広く使用されていた薬用物質-コカイン、アトロピン、ピロカルピン、ジオニン、硫酸亜鉛などが含まれていました。目での溶解時間はわずか数秒でした。
M. M. Budzko(1910)は、45錠の眼科用錠剤を研究しましたが、結膜嚢に錠剤を置くときの薬物の効果は、眼科の形で同じ物質を使用する場合と比較して、より顕著な程度で、より長期間にわたって現れるという結論に達しました 落ちます。 マイナスの点は、結膜を刺激する賦形剤の錠剤中の存在のみです。
時間が経つにつれて、眼科用錠剤は徐々に時代遅れになり、第二次世界大戦中にのみそれらに戻り、押された錠剤の代わりに、粉砕錠剤が準備され始めました。
湿らせた錠剤塊を小さな形に導入し、続いて乾燥することにより得られる。 そのような錠剤は、圧縮されたものより耐久性が低く、より多孔質であり、その結果、それらは涙液により簡単かつ迅速に溶解します。 1944年、N。N. Solomnikは、重量0.003 g、直径3 mm、高さ0.37 mmの、ピロカルピンを0.00015 gの量で含有する眼用粉砕錠剤の調製方法を提案しました。 ガラス管に詰められた錠剤は、115℃の温度で30分間滅菌されました。 結膜嚢に導入されると、非常に早く溶解します。
パウダー。 無菌のダスティングパウダーは、無菌状態で最高の分散度の医薬品から調製され、非熱不安定性物質は追加の加熱滅菌にかけられます(たとえば、多くのスルファニルアミド製剤は150°Cで15〜30分間乾熱滅菌されます)。
鉛筆。 粘膜を焼uterするために眼科診療で使用される鉛筆(硝酸銀、ミョウバン、硫酸銅などを含む)は、塩を溶かしてから特別な形に注いで固化するか、またはロールアウトすることによって得られます。 後者の場合、薬用物質はペースト状の基剤と混合されます。 乾燥中にスティックを広げた後、水分を失い硬化します。
リストされている剤形は、眼科で薬用物質を使用する可能性に限定されません。 この点で有望なのは、最新の科学的成果とバイオ医薬品の原則の適用に基づいて作成された比較的新しい剤形である医薬品エアロゾルです。 エアロゾル粒子は粘膜によく吸着され、原薬の迅速な吸収を保証します。 エアロゾルの使用は痛みがなく、使用量が大幅に増加する可能性があります
粒子の高分散による薬物の治療効果。
品揃えと特性フィルムフォーマー。目のフィルム(眼科の膜)。 それらは、長さが9.0-6.0 mm、幅が3.0-4.5 mm、厚さが0.35 mm、平均重量が0.015 gの滑らかな端を備えた中実の楕円形プレートです。 組織とポリマーの眼液。 薬用物質は、フィルムの組成に導入されます。
眼科用薬用フィルム(GLP)は、眼軟膏、エマルジョンなどに比べていくつかの利点があります。その助けにより、作用を延長し、眼の組織内の薬物濃度を高め、注射回数を1日5-8回から1-2回に減らすことができます。 結膜嚢に入れ、10〜15秒間、涙液で湿らせて弾力性を与えます。 20〜30分後、フィルムは粘性のあるポリマーの束になり、75〜90分後に完全に溶解し、薄くて均一なフィルムが作成されます。
ポリアクリルアミドまたはアクリル系およびビニル系のモノマーとのコポリマー、ポリビニルアルコール、NaKMUは、フィルム形成剤として使用されます。 全ロシア医療技術研究所は、60部のアクリルアミドコポリマー、20部のビニルピロリドン、20部のアクリル酸エチル、および50部の可塑剤-ポリエチレングリコールスクシネートからなるHFR(VFS-42-439-75)のベースを提案しました。
目のフィルムの生産。SODIの入手方法は次のとおりです。 反応器内で16〜18%のポリマー溶液が得られます。 成分を96%エタノールと混合して緩め、次に水を加え、混合物を50°Cに加熱し、完全に溶解するまで攪拌し、30°Cに冷却し、キャラコ層でろ過します。 それとは別に、薬物溶液を調製し、ポリマー溶液に導入します。
得られた組成物を1時間撹拌して均質化し、2時間遠心分離して気泡を除去する。 特別な設備を使用して得られた溶液は、エタノールで処理され、0.13-0.14 m /分の速度で移動する金属ストリップの表面に2層で(スリットを通して)適用され、40から48°Cの5つの乾燥ゾーンを備えたチャンバーで乾燥され、 38°Cに冷却し、直径30mmのロールの形で金属テープからフィルムを取り外した ひずみ応力を除去し、ストリップに切断し、スタンプを使用して必要なサイズのHFDを取得するために、6〜8時間放置します。 30個のHLPを特別なディスペンサーケースに詰めて、保管および使用中の気密性と無菌状態を確保します。 また、アルミホイルとそれぞれ10 GLPのPVCフィルムの輪郭セルパッケージを使用し、20〜100個の段ボール箱に入れます。 滅菌は、20 kGyの線量でのγ線照射、またはエチレンオキシドと二酸化炭素の混合物での処理によって行われます。 無菌性は一年中持続します。 HFDの品質の評価は、物理化学的特性(表面粗さ、亀裂の存在、裂け目、弾性、強度、光沢)に従って行われます。 医療産業は、塩酸ピロカルピン、ネオマイシン、ジカイン、ピリダジンナトリウム、およびフロレナールで眼用フィルムを製造しています。
有望な剤形は、ゲンタマイシンまたは硫酸カナマイシンとトリメカインを含むコラーゲンに基づいて作られた眼内薬物フィルム(ILP)です。 それらは、計画された外科的介入の間に眼の前房に縁取られ、医薬物質を徐々に放出し、二次感染の発生を排除します。 HLPは10日目に完全に溶解します。
GLPに加えて、ラメルが使用されます-直径3 mmの小さなゼラチン状の楕円形ディスク。 ゼラチン状の塊の組成には、さまざまな薬用物質が注入されます。 治療目的のために、特別なコンタクトレンズが使用されます-ゼラチンまたは薬用物質で満たされたカップの形のポリグリセリルメタクリレートから、使用中にゆっくりと放出され、長時間の作用を提供します。使い捨ての眼用剤形は最小限です-溶液4〜12滴または0 軟膏5 g。 ミニマムの特徴は、それらが簡単に開けられ、粘膜に内容物を絞ることで薬物を投与しやすくすることです。 結論と提案。
剤形が眼科医を完全に満足させるものではないため、眼科、点眼薬および軟膏で広く使用されています。 その理由は次のとおりです。1)比較的短い期間の治療作用。 2)使用された基礎と薬剤の頻繁な投与に関連した刺激; 3)薬物使用時の投与量の不正確さ; 4)繰り返し使用すると、薬物に対するアレルギー反応を起こす可能性。
眼科での薬物の作用の延長は、点眼剤の粘度を上げることで達成できます。 点眼剤の粘度を上げるには、高分子量物質(IUD)を追加する方法と、蒸留水をさまざまな油で置き換える方法の2つがあります。 しかし、すでに述べたように、油膜は視力を損なうため、後者の方法はしばしば患者にとって不快です。
IUDの追加がより受け入れられることが判明しました。 業界では、MCのソリューションを追加して、点眼薬の処方を作成しています。 ただし、眼科医はMCの頻繁な使用を推奨しません。
これは角膜上皮の回復を遅らせる可能性があります。 PVAは、潰瘍、火傷、および角膜の他の疾患の治療に応用されています。 そのプラスの特性には互換性が含まれます。 大多数で目の練習で使用される薬用物質および防腐剤。急速な増粘のため、PVAソリューションは濃度は2%以下です。
参照資料1.Gendrolis Yu.A. 眼科用剤形-M.、1988.-256 p。2.ソ連の州薬局方E-11th ed。-M.、1987、-Vol。 1336秒、M.、1990年。 2 -397秒。
Z.ムラビョフI.A. 薬の技術:2巻の教科書。-M.、1980。-1巻から390秒、2巻から704秒
4.薬剤師ガイド/ Ed。 Tentsovoi A.I.-M、1981.-383p。
5.剤形の技術:2巻の教科書、1巻/編。 T.S. Kondratieva.-M。、1991.-496s、第2巻/ Ed。 L.A. Ivanova.-M。、1991.-554C
内容:
はじめに……………………………………………………………………..page 3
目的
点眼薬……………………………………………………………………5ページ
内服用製剤は製剤を落とす............................................. 11ページ
眼科用懸濁液および乳液……………………………………………………….12ページ
眼科用軟膏……………………………………………………………………..13ページ眼科用剤形の休暇および準備
結論…………………………………………………………………………….. 20ページ
使用文献リスト………………………………………21ページ
はじめに
眼科用剤形は、その使用の詳細およびこの製剤から生じるため、他の薬物の中でも特別な場所を占めています。 目の吸収の領域は角膜であり、厚さ約1 mmの典型的なリポイド障壁です。 脂溶性の薬物をよく浸透します。 脂質バリアの背後に水室があります。 眼科用薬を使用する場合に期待される効果は、薬の眼組織の利用可能性であるため、脂質と水の障壁を克服する必要があります。 眼科用医薬品の調製は、特別な規則を厳守する必要がある薬局業務の重要なセクションです。
眼科診療では、さまざまな薬物が、診断または治療目的の局所効果の作成と、隣接組織での薬理効果の実現の両方に使用されます。
眼科の剤形のうち、ドロップ、軟膏、ローション、アイスプレー、およびアイフィルムが使用されます。 製薬会社での生産量と薬局チェーンでの販売の両方の点で、最大の関心は目薬と軟膏です。
同様に重要なことは、眼科医薬品のシンプルで便利で、審美的で、有益で、経済的に実行可能なパッケージを作成することです。これにより、長期にわたって無菌で化学的に不変の状態に保ち、使用時の投与速度を確保できます。 最近、buffusの実用的なパッケージングが日常生活に含まれています。
目的:最も便利で効果的な剤形としての点眼薬および軟膏の研究。 工業生産ではさまざまな剤形が用意されていますが、眼軟膏と点眼薬は、それらの助けを借りてこれらの剤形の最適な治療効果と使いやすさが生み出されるため、最も重要です。 目の病気の数の増加は、不利な環境条件、技術的影響、視覚器官への負荷など、文明の発展とともに増加する多くの要因によって決定されます。 眼科診療のためのすべての薬は、薬の特別なグループです。 これは、社会的、医学的、薬学的な性質のいくつかの理由によって決定されます。人間の生活のレベルと質を確保する上での視覚器官の排他的な役割。 視覚の解剖学的、生物物理学的および物理光学的メカニズムの特別な複雑さと特異性; 目の前部に対する薬効の可能性と必要性\u200b\u200b; 眼科用剤形の品質と安全性に関する厳しい要件。 組成物および技術の開発における重大な技術的困難。 しかし、常に点眼薬の助けを借りて完全な治療効果が達成されるのではなく、点眼薬と軟膏の組み合わせを使用すると、より大きな効果が達成されます。
眼用剤形
点眼薬-水性または油性の溶液、薬用物質の最も薄い懸濁液またはエマルジョンであり、滴剤で投与される液体剤形。 水溶液。 これらのソリューションは、目などの繊細で敏感な臓器を対象としているため、さらに病気にかかっているため、次の条件下で準備する必要があります。
不妊。 目の結膜を感染から保護する必要があるため、点眼薬は無菌でなければなりません。 通常、感染は涙液に含まれるリゾチームによって防止され、結膜に入る微生物を溶解します。 目の病気の場合、涙液には通常ほとんどリゾチームが含まれておらず、目の結膜は微生物の影響から保護されていません。 滅菌されていない滴を眼に感染させると、重度の原因になる可能性があります(その結果、視力低\u200b\u200b下を引き起こすことがあります)。 無菌条件下で点眼薬、軟膏、ローションを作る必要性は、これらの形態が目の結膜に適用され、感染する可能性があるという事実によって引き起こされます。 通常、涙液には特別な抗生物質であるリゾチームが含まれています。リゾチームは結膜に入る微生物を破壊する能力があります。 多くの病気で、涙液にはリゾチームがほとんど含まれておらず、目は微生物にさらされています。
点眼薬の調製時には、滅菌と無菌操作を使用することで簡単に滅菌できます。 ただし、すでに最初のアプリケーション(ボトルを開く)で、ドロップにミクロフローラを播種しています。 この点で、熱滅菌とともに、保存および繰り返し使用の両方のために無菌性を維持するために、保存剤を点眼薬に追加する必要があります。
点眼液を滅菌する方法:
点眼薬の熱滅菌法の選択は、加熱時の溶液中の薬物の安定性の程度によって決まります。 蒸気滅菌は、圧力下で120°Cで8分間、または110°Cで30分間行われます。 これは、熱安定性物質の溶液に対する最も信頼性が高く効果的な滅菌方法です。 安定性の低い物質は、100°Cの流体蒸気で30分間滅菌されます。 点眼薬の無菌性は、注射用溶液の無菌性と同じ方法-無菌条件下での調製および1つまたは別の滅菌方法を使用して達成されます。 点眼液を滅菌する方法は、温度暴露に対する溶液中の薬剤の耐性に依存します。
微孔性(孔径1〜2ミクロン)滅菌フィルターによる無菌条件下での細菌ろ過は、主に工場で使用されています。
滅菌方法に関係なく、点眼薬は無菌条件下で調製する必要があります。 特に重要なのは、滅菌されていない熱不安定性物質の溶液である点眼液の無菌製造です。
ソビエトの科学者は、点眼薬の防腐剤として多くの物質を研究しました。 次の消毒剤は、病原性ブドウ球菌、干し草および大腸菌、青緑膿菌、酵母、カビおよびキノコの真菌に対して最も効果的です:濃度が最大0.005%のメルチオレート、クロロブタノール水和物が0.5%、塩化ベンザルコニウム-0、 01%、塩化セチルピリジニウム-0.01%、硝酸フェニル水銀(ホウ酸塩、酢酸塩)-最大0.004%、パラヒドロキシ安息香酸のメチル(2部)およびプロピル(1部)エステルの混合物(ニパギンおよびニパゾール)-最大0.15 % "、クロラムフェニコール-ホウ酸-2%と0.2%、その他の防腐剤とその組み合わせ。括弧内の数字 ああ溶液の総量の物質の割合を示します
使用中に点眼液の微生物汚染のリスクがあります。 溶液に落ちた微生物の成長と繁殖を減らすために、慎重に選択された防腐剤がその組成に追加されます。
工業生産では、スポイトチューブの点眼薬は、無菌条件下でIIクラスの清浄度の部屋で準備されます。 部屋と機器はウェットクリーニングされ、3-5%フェノール溶液で消毒され、殺菌灯で2時間殺菌されます。
溶解は攪拌タンク反応器で行われ、その後分析され、順番にろ過されます(最初は機械的不純物からの精製のため、次に滅菌のため)。 得られた溶液を、チューブドロッパーを充填するための滅菌装置に入れる。 スポイトチューブ(本体と貫通ピン付きのキャップで構成されています)は、製造後、蒸留水で洗浄し、乾燥させ、エチレンオキシドと10%二酸化炭素の混合物で2時間40-50°Cでガス滅菌します。 それらからエチレンオキシドを完全に除去するために、12時間無菌室に保管します。
キャップを体にねじ込み、薬液で満たすと、無菌状態で滅菌空気が過剰に圧力がかかった状態で、ユニット内でヒートシールによる密閉が行われます。 次に、薬の名前、濃度、および量を記載した碑文が身体に適用されます。 次に、機械的介在物がないことを60 Wの電気ランプで照らしたときに、黒と白の背景で目視検査が行われます。 GOST 17768-80によると、チューブスポイトに加えて、安定化されていない低密度ポリエチレン製のストッパーピペット付きのガラス瓶が点眼薬の包装に使用されています。 薬液はろ過により滅菌され、ピペットは10%の二酸化炭素を含むエチレンオキシドを用いたガス滅菌により滅菌されます。
等張性。 点眼薬は、涙液に対して等張性が必要です(薬用物質が高濃度で処方され、カラーゴールとプロタルゴールの溶液に加えて処方されている場合を除く)。 非等張液が目に導入されると、痛みが現れます。 残念ながら、点眼薬の義務的な等化の原則は、すべての薬局によって維持されていません。 等張性塩化ナトリウム溶液または他の等張性溶媒で、計算なしで最大3%の濃度の医薬品を含む点眼薬を調製できる場合、彼らの作業は非常に容易になります。 一部の薬局方(米国)ではこれが許可されています。 特別な処方は点眼薬と考えるべきであり、その成分は一緒になって、塩化ナトリウムの1.1%当量濃度を超える滴の浸透圧を増加させる。
点眼薬が医師によって低張濃度で処方される場合、この場合、薬剤師自身が溶液の製造において等張性を達成します。 この場合、州薬局方の規定に従って、塩化ナトリウムの医薬品の等張性等価物が使用されます。
通常、涙液の浸透圧は、血漿および等張性(0.9%)塩化ナトリウム溶液と同じです。 点眼薬はそのような浸透圧を有することが望ましい。 偏差は許容され、目薬は0.7から1.1%の濃度で不快感を引き起こすことが示されています。
安定性 点眼薬では、溶解した医薬品の安定性を確保する必要があります。 熱滅菌(最適な条件下で行われなかった場合)およびガラス容器内の点眼液の長期保管は、加水分解、酸化などによる多くの医薬品(アルカロイド、麻酔薬など)の破壊につながります。
もちろん、要因を安定させるために起因する必要があります。 防腐剤、pHおよび酸化防止剤を調整する物質。 点眼薬の形で使用される医薬物質は、最大の安定性に対応する溶液のpHに応じて3つのグループに分類できます。
最初のグループには、アルカロイドと合成窒素塩基の塩、および酸性環境での加水分解と酸化に耐性がある他の物質が含まれます。 これらの物質は、1.9〜2%の濃度のホウ酸で安定化することをお勧めします。 ホウ酸は、点眼薬に効果のない安定剤です-硫酸アトロピン、塩酸ポリカルピン、臭化水素酸スコポラミン、ジカイン、ノボカインの溶液。
2番目のグループは、中性またはわずかに酸性の環境で安定な薬物で構成されます:ベンジルペニシリン、ストレプトマイシン、クロラムフェニコールなどの塩。このような薬物を安定化するには、さまざまなバッファー混合物、クエン酸ナトリウムなどを使用できます。
3番目のグループには、アルカリ環境で安定な薬物が含まれます。スルファシルナトリウム、ノルスルファゾールナトリウムなど。これらは、苛性ナトリウム、重炭酸ナトリウム、四ホウ酸ナトリウム、およびアルカリ性pH値の緩衝液で安定化できます。
低酸化物質の点眼液を安定させるために、注射液(亜硫酸ナトリウムおよびメタ重亜硫酸塩)の酸化を抑制するために使用される酸化防止剤が使用されます。 例えば、スルファシルナトリウムの30%溶液は、0.5%のメタ重亜硫酸ナトリウム、および同じ抗酸化剤を0.1%の量で含むエチルモルヒネ塩酸塩の1%溶液で効果的に安定化できます。
延長。 点眼薬は、最も長く持続する効果があります。 作用の延長は、水溶液の粘度を上げることで達成できます。 点眼薬に最適な粘度は5〜15 cPと考えられています。 粘度は40〜50 cPを超えないようにしてください。この場合、投与が難しいためです。
ポリビニルアルコール、メギルセルロース、およびカルボキシメチルセルロースナトリウムがこの目的に適していることが証明されました。 これらの物質は視力を曇らせず、その優れた接着特性により、刺激せずに目との必要な接触を提供します。 PVAとNa-KMCの希釈溶液(1.5)とMC(0.5%)は簡単に滅菌でき、冷蔵庫に保管しても透明のままです。
点眼薬の不利な点は、短期間の治療作用です。 これは、頻繁にインストールする必要があり、また目に危険をもたらします。
透明性 点眼薬は完全に透明で、目の膜に機械的損傷を引き起こす可能性のある浮遊粒子を含まないようにする必要があります。 点眼薬は、最高品質のろ紙でろ過し、フィルターの下に長繊維ウールの小さな塊を置きます。 ろ過後、溶液の濃度とその総質量が、確立された標準で許容される以上に減少しないことが重要です。 少量のソリューションを完全にフィルタリングすることについて言われたことはすべて、主に点眼薬に関連しています。 レシピによく見られるレシピによると、薬局内のブランク、濃縮物、時間通りに準備された、少量の液体のろ過を免除する助けを借りることをお勧めします。
内部の薬局ブランクのレシピ。 滴剤は無菌的に調製され、塩化ナトリウムで等張化され、慣らし運転用に密閉され、100°Cの蒸気で30分間滅菌されます。
蒸留水は新たに煮沸する必要があります。 リボフラビンは、目の正常な視覚機能を維持する上で重要な役割を果たします。
Rp:Novocaini 0.1
ジンチスルファチス0.025
Ac。 borici g.s ut ayu sol。 イソトニカ10.0
D.S 2は1日3回ドロップします
製剤では、等張液を得るためにホウ酸の量を計算する必要があります。 上記のレシピは異なる場合があります。 そのため、ノボカインの代わりに、ホウ酸の溶液の代わりにジカインを処方することができます。滴の「ケース」は、シアン酸水銀の溶液1:5000または1%のレゾルシノール溶液として書き出すことができます。 ホウ酸の代わりにミョウバンを添加してもよい。 レシピには、アドレナリン塩酸塩の1:1000溶液が含まれる場合があります。 調剤を加速するために、薬局はしばしば2%ホウ酸溶液中の0.25%硫酸亜鉛溶液の滴の「ケース」を将来使用するために調達します。
Rp。:ソル。 スルファシルナトリ20%10.0
DS。 目薬
スルファシルナトリウム(アルブシド)の滴は、これに必要な事前に洗浄および滅菌された容器(分注ボトルを含む)で注射用に水で調製されます。 2 gのスルファシルナトリウムを5 mlの注射用水に溶解し、得られた溶液を注射用水で事前に洗浄した小さなペーパーフィルターで濾過して、乾燥した滅菌ボトルに入れます。 次に、残りの水を溶液に加え、同じフィルターに通して10 mlの溶液を得ます。
Rp。:リベフラビニ0.001
Ac。 アスコルビニシ0.1
水溶液 プロ注入。 10.0
MDS 目薬
アスコルビン酸は、注射用水に溶解されています。 リボフラビンは1:5000溶液(薬局内ブランク)として投与されます。
目の懸濁液および乳剤
目の懸濁液は、水性または油性分散媒中の薬用物質の粉末の最も細かい懸濁液です。 それらは、懸濁液が最初の不溶物の分散度の漸進的な減少により懸濁液が形成されるとき、すなわち、分散方法によって得られる。 出発物質の分散度の増加の結果として懸濁液の形成が起こる場合、それは以前はイオン、分子またはコロイドの分散度であったが、それを粉砕するか、または凝縮によって。懸濁液の沈降不安定性を克服し、その中の微粒子を保存する場合、得られる製剤は患者に不快な感覚を引き起こさず、点眼薬と同じ効果があります。
医療現場で使用される目の懸濁液は、工場で準備されており、使用前に水で希釈するだけで十分です。
眼科診療で使用するエマルジョンは、原薬の溶液を乳化した滅菌非水性溶媒を使用して調製されます。 エマルジョンの水相のpHは4.5〜7.0であり、最も好ましい値はpH 6.0と考えられています。
作用機序により、乳化剤は界面活性剤に分類され、主に相境界での表面張力の急激な低下によりエマルジョンを安定化します。 界面に強力な吸着膜を形成することにより、エマルジョンを安定化するゲル化剤。 眼科診療で最もよく使用される混合アクション乳化剤。
現在、眼科用の懸濁液の形で、ステロイドホルモン製剤が使用されています。 分散媒による湿潤が不十分な凝集体またはフレークの形成を防ぐために、PEG-400および0.1-0.15%塩化ナトリウム溶液を組成物に導入することをお勧めします。
眼科診療で使用するエマルジョンは、原薬の溶液を乳化した滅菌非水性溶媒を使用して調製されます。 したがって、例えば、緑内障の治療のために、ピロカルピン塩酸塩の0.25〜8.0%水溶液、中性油および乳化剤の10〜80%溶液を含むピロカルピン眼科\u200b\u200b用エマルジョンが提案されている。
目の軟膏
軟膏は、特別なへらの助けを借りてまぶたの下に置くことにより、目の結膜への適用を目的としています。 眼軟膏は、最高品質に基づいて作成し、最高の分散状態の固相を含める必要があります。 眼軟膏の基礎として、「眼軟膏」品種のワセリンと、このワセリンと様々な割合のラノリンとの合金が使用され、多くの場合、少量の水が含まれています。 根拠が示されていない場合、眼軟膏の一般的な要件を定めた州薬局方の記事709によれば、10部の無水ラノリンと90部のワセリンの合金が使用されます。 場合によっては、親水性基剤は眼軟膏の基剤としても使用されます。
時々、新たに調製されたグリセリン軟膏がそのようなベースとして使用されます。 ミクロフローラの作用に対して非常に安定しており、非常に親水性で中性です。 グリセリン軟膏の欠点は、かなり強力な水分摂取効果とそれに関連する刺激効果であり、軟膏に含まれる澱粉の包み込み効果によっていくらか緩和されます。
眼科用軟膏は、無菌条件下で小さなガラス乳鉢で、またはさらに良いことに、平らなガラスの乳棒を使用してつや消しのガラス板の上で調製されます。 後者の場合、透過光中の軟膏の薄い層を調べることにより、均質性を簡単に確認できます。
目の結膜は非常に繊細で脆弱な粘膜であるため、目の軟膏には追加の要件が課されます。
- 目の軟膏には、刺激物質や濃酸だけでなく、結膜を傷つける可能性のある鋭い角を持つ固体粒子を含めないでください。
眼軟膏は、粘膜上に容易かつ自然に分布している必要があります。
- 無菌性(製造は無菌条件下でのみ行われます);
眼懸濁液中の薬物の最小分散度(使用の快適さと安全性のため);
眼軟膏の構造によってもたらされる、結膜および眼の粘膜上の分布の容易さと均一性;
軟膏の組成物(特に酸)に刺激性成分がない;
眼軟膏の必要なpH値は4.5〜9.0の範囲にあります。そうしないと、眼から軟膏が裂けたり浸出したりする可能性があります。
- 不妊
刺激性の欠如;
化学的無関心;
優れた流通能力;
涙液による乳化を提供する親水性;
ベースの融解温度32-33°C
医師が処方の根拠を示していない場合、州薬局方によれば、10部の無水ラノリンと90部の「眼軟膏用」グレードのワセリンの無菌混合物を使用する必要があります。 混合物を融合し、熱濾過用の漏斗で紙で濾過し、高温状態の乾燥滅菌瓶に入れ、羊皮紙で縛り、空気滅菌器で180°Cで30分間または200°Cで15分間滅菌する必要があります。 25℃以下の温度で2日間、または3〜5℃で30日間以下の暗い場所で保管してください。
すべての可溶性医薬物質は、滅菌水への強制溶解後に眼軟膏の組成物に導入されます。 不溶性または難溶性の物質-黄色水銀、塩基性硝酸ビスマス、アミド塩化水銀、一塩化水銀、ゼロフォーム、酸化亜鉛、クエン酸銅などは、少量の補助液体(液体パラフィン、 グリセロールまたは水)、ベースの組成に応じて。 すべての補助材料、軟膏基剤、薬用物質(耐熱性)、缶は、州薬局方の指示に従って滅菌されています。
軟膏の製造では、投与される医薬品は最適な分散度を持たなければなりません。 必要な分散度は、滅菌水に溶解するか、少量の水または関連する基剤で徹底的に粉砕し、その後軟膏基剤と混合することにより達成されます。
眼軟膏の技術を改善することは、新しい軟膏基剤、特にカルボポールゲルの使用の方向付けられた流れに貢献します。 カルボポールゲルに基づいて、抗炎症薬とビタミンを含む軟膏が調製されます。
目の軟膏の製剤は多様です。 これらは主に二価で、より複雑な分散システムです。
黄色の水銀軟膏(目の軟膏)-Unguentura Hydrargyri oxydi flavi。 軟膏は、GFHの規定(第343条)に従って公式であり、2%の黄色酸化物水銀が含まれています。
Rp。:Hydrargyri oxydi flavi 2.0 01。
Vaselini 2.0 Vaselini 80.0 v
Lanol\u200b\u200bini anhydrici 16.0
軟膏の基礎は、ワセリン(5部)とラノリン(1部)の合金です。 黄色い酸化水銀:液体パラフィンで完全に粉砕し、その後、ほぼ冷却された滅菌ベースを部分的に混合します。 軟膏は常に即席で準備されます。 黄色の酸化水銀は金属水銀の放出により光の影響で分解し、また「ラノリン脂肪酸と相互作用して有毒な水銀石鹸を形成するため、日光から保護された場所に保管されます。この軟膏の製造に金属ヘラを使用しないでください。
Rp。:キュプリシトラティス0.3
ウン グリセリーニ10.0
M. f。 うん。
DS。 1日2〜3回永久にポーンする
まず、処方GF1Xに従ってグリセリン軟膏を準備します(軟膏はグリセリン93gと小麦澱粉7gで構成されています)。 これを行うには、磁器カップで小麦澱粉を同量の水と完全に混合し、その後グリセリンを加えます。 攪拌するとき、均一な半透明の塊が得られるまで、混合物をグリッド上で弱火で注意深く加熱します。 作りたての軟膏はそれ自体が無菌です。 硝酸銅を数滴の水で完全に粉砕し、その後、ベースを部分的に混合します。
目の軟膏の処方では、抗生物質を含む軟膏がしばしば見られますが、これは無菌条件下で調製されます。
Rp。:ベンジルペニシリニ-ナトリ1ED
ラノリーニ
Vaselini pro oculis aa 5.0
M. f。 うん。
DS。 1日2〜3回永久にポーンする
まず、乾熱で滅菌されたベースを準備します。 同時に、乳鉢、乳棒、およびテンパージャーが滅菌されます。 滅菌乳鉢では、ベンジルペニシリンナトリウム塩を少量の塩基と完全に混合し、その後、残りを部分的に混合します。
眼科用剤形の休暇および準備
眼科薬は、無菌の密閉容器に入れられた薬局から調剤されます。 点眼薬はペニシリンバイアルで放出され、イスラムグロフマシンを使用してゴム栓とアルミニウムキャップで密閉されています。
眼軟膏は、金属製またはプラスチック製のチューブと同様に、磁器またはガラス瓶(必要に応じてオレンジ色のガラス)で放出されます。 チューブは、シリンジの原理で動作する特別な滅菌装置を使用して充填されます。 金属と相互作用する可能性のある成分を含む軟膏の包装には、金属チューブを使用しないでください。 チューブにはねじ込み式の先端を取り付けることができ、まぶたの軟膏を入れることができます。
ピンク色のラベルは、点眼薬と眼軟膏でパッケージに接着されています。
アイローションとリンスは、しっかりとフィットするストッパーを備えた滅菌ボトルで放出されます。
すべての点眼薬は、「涼しくて暗い場所に保管する」というラベルの付いた、涼しくて暗い場所にある密閉された容器に保管する必要があります
結論
目の病気は最も危険なものの1つです。なぜなら、私たちの周りの世界に関する情報のほとんどは、その使用で受け取るからです。 また、目の病気は、完全または部分的な視力喪失につながる可能性があり、これは社会的および経済的な意味を持ちます。
医薬品の開発は、医薬品の製造の改善、品揃えの拡大、製造された調剤の品質の向上につながり、これは眼科医薬品の開発のダイナミクスによっても確認されています。 これらの剤形を改善するために、重要な科学的および技術的努力がなされてきました。 薬効を強化するための作業が進行中であり、このために新しい活性物質が開発され、それらのさまざまな組み合わせの効果が研究されており、薬物質の作用期間(延長)が増加しています。 また、緑内障を中心とした眼疾患の治療を改善し、患者の治療を改善するために、併用薬も開発されています。 これらの薬物には、降圧作用の異なるメカニズムを持ち、同時に使用すると相加効果が現れる物質が含まれており、それが人口の眼病のレベルの低下に影響を与えます。
参照:
1.薬の産業技術:2巻で。 Chueshov V.I.、Chernov M.Yu.、Khokhlova L.M. X .: MTK- Book; NFAA出版社、2002年。
2.剤形の技術。 ボリューム1、2。 L.A. Ivanova M.、1991
4.ソ連のXI州薬局方。 巻 1、2. M .: Medicine、1987(Issue 1)、1989(Issue 2)
5.Muraviev I.A. 薬の技術。 2巻で。 M.、1980
点眼薬は、水性または油性の溶液、または薬物の最高の懸濁液です。 目のための他の薬のように、それらは無菌で安定していなければならず、肉眼で見える機械的不純物を含んではいけません。
点眼薬の主な要件は、GFHの一般的な記事No. 319に記載されています。
点眼薬の調製プロセスでは、熱滅菌(原薬の安定性が許す場合)および無菌状態の順守により、滅菌が保証されます。 しかし、最初のアプリケーション(ボトルの開封に関連する)ですでに、ドロップにミクロフローラが播種されています。 熱殺菌に加えて、抗菌薬物質は、保管中の無菌性を維持するために、薬局の条件の下で準備さ\u200b\u200bれたほとんどの点眼薬に導入されます。 適用されたとき。 これらには、メルチオレート(0.005% ), エタノール塩化水銀(0.01%)、塩化シチルピリミジン(0.01%)、クロレトン(0.6%)、ニパギン(0.1%)、クロラムフェニコール(0.15%)、ベンジルアルコール(0.9%) 。 最も活発な抗菌効果は、ホウ酸の存在下で提供されます。
点眼剤は、涙液に関して等張性が必要です。 目に注射したとき。 非等張溶液は、涙液と溶液の浸透圧の違いによって引き起こされる痛みのように見えます。 点眼液の等張化は、等張性塩化ナトリウム溶液(0.9±0.2%)または別の等張性溶媒で調製することにより達成されます。 そのような溶液の浸透圧は涙液の浸透圧に近づくので、目薬中の薬物の含有量が4%以上の等濃度の濃度ではもはや必要ではありません。
注射用の水は点眼薬の溶媒として最もよく使用されるため、治療効果の期間は短く、その結果、患者は頻繁に点眼を行う必要があり、その結果、目に悪影響を与える可能性があります:薬物に対するアレルギーがあるため、感染の可能性が高くなります。 これに関して、点眼剤の形で使用される薬物の作用持続時間を増加させることが望ましい。 これは、溶液の粘度を高める物質を導入することで可能になりました。 後者として、ポリビニルアルコール、メチルセルロース(1%溶液の形態)またはカルボキシメチルセルロースナトリウムを使用できる。
点眼薬では、原薬の安定性も確保する必要があります。 ガラス容器内の眼科用溶液の熱滅菌および長期保存は、酸化、アルカリ加水分解などによる多くの医薬物質(アルカロイド、鎮痛剤など)の破壊につながります。薬局での点眼薬の製造では、多くの場合、それらを安定させる必要があります。 。副作用に対する薬物の耐性を高める補助物質の追加。
点眼薬で安定させるために、亜鉛塩、いくつかのアルカロイド、ノボカイン、メサトーンが使用されます。 等張ホウ酸溶液(1.9%)。 アドレナリンとフィゾスチグミンの塩の場合、100 mlの溶液ごとに100 mgの亜硫酸ナトリウムが添加されます。 アトロピン、エフェドリン、ピロカルピンおよびスコポラミンの塩の溶液の安定化は、塩化ナトリウム、一置換および二置換リン酸ナトリウムを使用して行われます。
目の膜に機械的損傷を引き起こす可能性のある浮遊粒子を取り除くために、目薬は最高品質のろ紙でろ過され、長繊維の綿毛の小さな塊がフィルターの下に置かれます。 ろ過後、溶液の濃度とその総量が、確立された標準で許容される以上に減少しないようにすることが重要です。
薬局の処方箋によく見られる処方薬の点眼薬の製造では、指定された時間枠で計算された薬局内ブランク-濃縮液の助けを借りることをお勧めします。 これにより、点眼薬の準備が高速化され、少量の液体をろ過する必要がなくなります。 GFCの指示に従って、点眼薬に使用される濃縮液および点滴自体は、無菌条件下で調製する必要があります。
No.135。Rp。:ソル。 スルファシルナトリ20%10.0 DS。 目薬
スルファシルナトリウム(アルブシド)の滴は、これに必要な事前に洗浄および滅菌された容器(分注ボトルを含む)で注射用に水で調製されます。 2 gのスルファシルナトリウムを5 mlの注射用水に溶解し、得られた溶液を注射用水で事前に洗浄した小さなペーパーフィルターで濾過して、乾燥した滅菌ボトルに入れます。 次に、残りの水を溶液に加え、同じフィルターに通して10 mlの溶液を得ます。
No.136。Rp。:リベフラビニ0.001
Ac。 アスコルビニシ0.1
水溶液 プロ注入。 10.0
MDS 目薬
アスコルビン酸は、注射用水に溶解されています。 リボフラビンは1:5000溶液(薬局内ブランク)として投与されます。
No.137。Rp。:ソル。 ピロカルピニ塩酸塩1%10.0
DS。 1日に3〜4回、各目に1〜2滴
レシピに示されている塩酸ピロカルピンの溶液は非常に低張であり、眼に点滴すると不快感を引き起こすため、塩化ナトリウムで等張化する必要があります。 等張等価物の対応する計算は、pのGFで与えられます。 997.薬局方の表(および現在の教科書の「注射液」のセクション)から、塩化ナトリウムに対するピロカルピン塩酸塩の等張性当量は0.22である、つまり1 gのピロカルピン塩酸塩は0と同じ浸透圧を作り出す 塩化ナトリウム22 g。 したがって、溶液を塩化ナトリウムの等張濃度にするために、次のことを行う必要があります。
重さの量の塩化ナトリウムを注射用水に溶かし、0.1gのピロカルピン塩酸塩をこの溶液の半分(5ml)に溶かし、洗浄したフィルターを通して分注フラスコにろ過し、次に残りの溶液をフィルターを通して溶液に加える。 ピロカルピン塩酸塩はリストAの物質であることを思い出して、フラスコを休暇用に作成します。ラベル「取り扱いに注意」が接着されています。
No. 138. Rp。:ノボカニーニ0.1
ジンチスルファチス0.025
Ac。 ボリチq。 s。 ut f。 sol。 イソトニカ10.0
DS。 1日3回2滴
レシピは、等張溶液を得るために必要なホウ酸の量の計算を提供します。これは上記の例と同様に実行されます。 休日を早めるために、ブランク「ホウ酸の2%溶液中の硫酸亜鉛の0.25%溶液」を使用することもできます。これは10 gを服用し、ノボカイン0.1 gを溶解します。
抗生物質製剤、特に硫酸ストレプトマイシンとクロラムフェニコールは、点眼薬で広く処方されています。 安定性を高めるために、抗生物質を含む点眼液は滅菌緩衝液で調製されます。 したがって、例えば、クロラムフェニコールを含む点眼剤は、次の組成を有するホウ酸塩緩衝液で調製されます。
塩化ナトリウム
四ホウ酸ナトリウムAA 0.2
ホウ酸1.1
蒸留水100.0
指定されたソリューションは、100°Cで30分間滅菌済みです
他の抗生物質の点眼薬は、等張性塩化ナトリウム溶液を使用して調製されます。 ベンジルペニシリン-ナトリウム(カリウム)塩が20,000-100,000 IU / mlの濃度の点眼液で使用される場合、スコポラミン、アトロピン、ジオニン、およびモルヒネも溶媒として使用されます。
最近、Yu。F. Maychukら。 新しい眼科用剤形が提案されています-涙液に溶解し、対応する薬用物質を含むポリマープレートである眼科用剤形フィルム。 眼科用フィルムは、まぶたの上に置き、涙液で湿らせ、弾力性を獲得し、10〜40分以内に徐々に溶解し、そこに含まれる水溶性の薬用物質を放出します。
眼用剤形 -使用方法が異なる特別な投与形態のグループ-目の粘膜への点滴注入。
目の粘膜の特徴は、体のすべての粘膜と比較して最大の感度です。 それは外部刺激に鋭く反応します:機械的封入物、浸透圧に対する眼に導入された薬物の浸透圧とpH値の不一致、および涙液のpH値。
涙液は微生物の保護バリアです。 健康な目では、リゾチームの存在により殺菌性です。 しかし、目の病的状態では、涙液中のリゾチームの含有量は大幅に減少します。
微生物の別の保護バリアは角膜上皮です。 この障壁が損傷すると、一部の微生物が急速に増殖し、失明などの重篤な疾患を引き起こします。
したがって、眼科用剤形の製造のためには、視覚器官の解剖学的、生理学的および生化学的特性、ならびにこの剤形群の治療活性に影響を及ぼす要因を考慮する必要があります。
眼科用剤形の分類
眼科用剤形は4つのタイプに分けられます:
ドロップス;
ソリューション;
軟膏;
映画。
点眼薬は、点眼用の液体剤形です。 それらは、薬用物質の水溶液または油性溶液であり、ほとんどの場合、消毒薬、麻酔薬、眼圧を低下させる物質です。
主な欠点 点眼薬は、吸収の複雑なメカニズム、無効な投与経路(滴)、まばたき中の涙液による薬物のすすぎの結果として、薬物の低いバイオアベイラビリティです。 薬物の投与量の1/10だけが眼に浸透することが確立されています。 そのため、薬局の従業員は、点眼薬を適切に適用する方法を患者に知らせる義務があります。
アプリ
目を掘る方法。 消費者情報
1.手を洗ってください。
2.液滴ボトルが透明な場合は、使用前に溶液を確認します(色が変化した場合、沈殿物がある場合)。
3.頭を後ろに傾け、天井を見てください。
4.下まぶたを指で下に引きます。
5.下まぶたの後ろに形成された空洞に、ピペットまたはバイアルから溶液を1滴落とします。 ミラーを使用するか、誰かに助けを求めることができます。
重要:バイアルのピペットまたはチップは、できるだけ目に近づける必要がありますが、触れないでください。
6.可能であれば、まばたきを30秒間まばたきせずに開いたままにします。
7.インストールの効率を上げるには、目の外側の角を指で押して、1分間のまばたきを防ぎます。
8.バイアルをしっかりと閉じます。
図 30.1。目への適切な点眼
30.1。 アイドロップのGF要件
点眼薬は:
- 無菌条件下で準備さ\u200b\u200bれ、無菌であること。
- 機械的包含試験に耐える;
- 服用時に快適である(等張性、涙液を含む等張性);
- 頻繁に開けられる包装の状態で安定している。 物理化学、微生物を安定させるため
レオロジー特性、添加剤はドロップの組成に導入されます:防腐剤、酸化防止剤、増粘剤、安定剤、延長剤。
ルール1
厚生省の命令? 214が見つかりました:点眼薬に加えられる等張性および安定化物質の濃度と量(または質量)は、パスポートだけでなく、レシピにも示される必要があります。
30.2。 アイドロップ生産技術
薬局での滅菌溶液の製造と品質管理は、現在のグローバル基金の要件、薬局での滅菌溶液の製造に関するガイドライン、規制文書、注文および指示に従って実施されます。
点眼剤の製造技術は、内服用の点滴剤の調製と違いはありませんが、次の特徴があります。
30.2.1。 無菌性保証
グローバル基金によると、無菌性はすべての点眼剤に必要な要件です。 無菌性-実行可能な微生物汚染がない。 シードフリーの薬物は、目の感染症を引き起こす可能性があり、視力低下につながる可能性があります。
ルール2
眼科用剤形は、注射液と同様に無菌条件下で調製されます。
ルール3
滅菌溶媒は、点眼薬の調製に使用されます。精製水、等張緩衝液、油など。滅菌溶液は滅菌バイアルにパッケージされています。
ルール4
点眼薬は無菌でなければなりません。
点眼液を滅菌する方法は、溶液中の薬物の温度暴露に対する耐性に依存し、MOHの順序によって決まりますか? 1997年7月16日付けの214(注射と同様)。
保健省の命令によって確立された滅菌レジメンによると? 214、目薬は3つのグループに分けることができます:
1.安定剤を添加せずに、1.1 atmの圧力で120°Cの蒸気を8〜12分間、または流体の蒸気を30分間滅菌したドロップ。
この方法で、溶液は滅菌されます:硫酸アトロピン、ホウ酸、ジカイン、ヨウ化カリウム、塩化カルシウム、塩化ナトリウム、ニコチン酸、塩酸ピロカルピン、プロセリン、リボフラビン、スルホピリダジンナトリウム、フラシリン、硫酸亜鉛、塩酸エフェドリン、および点眼液 アスコルビン酸およびグルコースなどと組み合わせたリボフラビン
2.圧力下の蒸気または液体蒸気で滅菌できる安定剤を添加した滴剤(ロシア連邦保健省の命令の付録をご覧ください?214)。
3.熱的方法では滅菌できない熱不安定性物質を含む滴。 滅菌ろ過は、0.22μmの膜を通して行われます。 この技術により、ベンジルペニシリン、硫酸ストレプトマイシン、カラーゴール、プロタルゴール、レゾルシノール、塩酸アドレナリン、シトラールなどのソリューションが作成されます。
薬局で製造された点眼薬の無菌性のチェックは、衛生および疫学的サーベイランス(TsGSEN)の地区センターに割り当てられています。
ルール5
点眼薬は、頻繁に開けられる包装の条件下で無菌状態を維持する必要があります。
点眼薬は、滅菌条件に関係なく、使用中に微生物で汚染される可能性があります(1本のボトルから繰り返し使用)。 塗布中の点眼液の微生物汚染を防ぐために、次の防腐剤を導入することをお勧めします:クロロブタノール水和物(0.5%)、ベンジルアルコール(0.9%)、およびパラオキシ安息香酸エステル
あなた(ニパギンとニパゾール、0.2%)、第四アンモニウム塩(塩化ベンザルコニウム、0.01%)、ソルビン酸(0.05-0.2%)など(表30.1)。
表30.1点眼液中の保存料の最大濃度
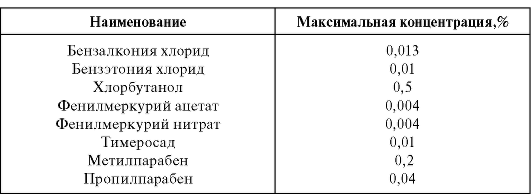
ルール6
防腐剤は殺菌効果を生み出しません。 防腐剤の導入は無菌性を保証するものではありませんが、頻繁に開封される包装内の微生物汚染の一定レベルを維持します。
防腐剤の存在に関係なく、患者は使用後にバイアルを密封し、ピペットを沸騰させるように助言されるべきです。
30.2.2。 機械的不純物がないことを確認する
薬局内ブランクの製造では、注射液をろ過するための機器が使用されます。
少量(10〜30 ml)を製造する場合は、あらかじめ湿らせて洗浄したペーパーフィルターを使用します。 ろ過は、ろ過水ですすいだボトルで行われます。
製造プロセスでは、ソリューションは、ロシア連邦保健省の命令に従って、機械的不純物のない一次および二次制御を受けますか? 214。
ソリューションをフィルタリングしてパッケージ化した後、初期制御が実行されます。 この場合、ソリューションのある各ボトルが表示されます。 機械的な不純物が見つかった場合、溶液は再ろ過、再検査、コルク、ラベル付け、滅菌されます。
また、二次管理は、設計とパッケージングの前に滅菌段階を過ぎた溶液を含むボトルの100%の影響を受けます。
医薬品内調達の品質管理は、機械的不純物がないことを30本のボトルで確認することによって実行されます。 制御時間は、それぞれ、5〜50 ml〜8〜10秒の容量を持つ2〜5本のボトルです。
30.2.3. 薬の投与量の正確性を確保する
点眼薬中の薬物の濃度の精度は、特にその量が0.05 g未満の場合、物質の計量の精度に影響されます。この状況から抜け出す方法は、濃縮溶液の使用です。 濃縮溶液の製造、包装、閉鎖、保管の要件は、点眼薬の要件と同様です。 使用する点眼薬の製造:リボフラビンの0.02%溶液、ホウ酸の4%溶液、硫酸亜鉛の2%溶液、2、アスコルビン酸の10%溶液、または2種類の薬物からなる混合溶液。 濃縮物のリストとその保管期間は、保健省の順序で示されていますか? 214。
30.2.4. 快適さ
点眼薬を使用することの快適さは、薬物の点滴中に不快感がないことを決定するバイオ医薬品の要因の1つです。 これは、点眼液を等張化するか、pHを涙液のpHに調整することにより達成されます。
等張化は、計算された量の塩化ナトリウムを溶液に導入することで実行されます(輸液を参照)。
点眼薬は、浸透圧が濃度0.7〜1.1%の塩化ナトリウムの浸透圧に相当する場合、不快感を引き起こさないことが示されました。 浸透圧値のソリューションの使用
これらの限界を超えて、それは目の粘膜の燃焼と刺激につながります(表30.2)。
表30.2。等張性、高張性、低張性点眼液の組成

30.2.5。 PH規制
点眼薬の快適性は、pH値に大き\u200b\u200bく影響されます。 涙液の平均pHは7.4です。 pHが4.5の比較的使いやすいドロップ
9.0まで(表30.3)。
点眼薬のpHを調整するには、重炭酸ナトリウムとホウ酸を使用します。 緩衝液をホウ素溶媒として使用することをお勧めします:酢酸ホウ酸およびリン酸(表30.4)。 塩酸またはアルカリの使用は実用的ではありませんが、頻繁に使用されます。
表30.3。点眼薬の推奨pH値

注:ロシア連邦保健省の命令によると? 214
表30.4。リン酸緩衝液の組成
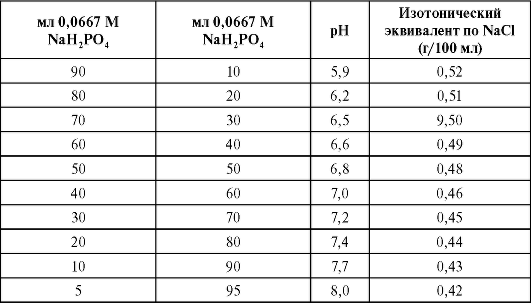
ご注意USP XXIによると、p。 1338。
30.2.6。 化学的安定性
実施者:
PH規制;
酸化防止剤の導入。
pHレベルは、薬物の溶解度に影響します(ソリューションを参照)。 加水分解と塩の塩基への転移を防ぐために、点眼液のpHを調整する必要があります。 一部の薬物は酸化分解を受ける場合があります。 これを防ぐために、抗酸化剤と抗触媒が点眼液の組成に導入されます(表30.5、30.6)。 低原子価の硫黄誘導体の導入は、特に子供たちにアレルギー反応を引き起こす可能性があることに留意してください。
表30.5。許可された抗酸化剤濃度
ご注意USP XXIによると、p。 1338。
30.2.7。 行動の延長のための規定
点眼薬の不利な点は、短期間の治療作用です。 このため、頻繁に設置する必要があり、患者や医療関係者にとって不便であり、目に危険をもたらします。 たとえば、緑内障患者における塩酸ピロカルピンの水溶液の最大降圧効果は2時間しか観察されないため、点眼薬の取り付けは1日に6回まで行う必要があります。 この場合、眼圧の急激な変動があります。 水溶液を頻繁に設置すると、リゾチームを含む涙液が洗い流され、それによって感染プロセスの発生条件が作り出されます。
延長により、点眼薬の設置頻度を減らし、同時に眼組織との接触時間を長くすることができます。 延長は、ニレを増やすことによって達成されます。
骨溶解。 粘度は、目の粘膜に沿った薬液の流出速度を決定します。 溶液の粘度が高いほど、溶液が長く保持され、バイオアベイラビリティが高くなります。
延長の最初の方法は、点眼液の組成に粘性溶媒を含めることで、結膜嚢からの薬物の急速な浸出を遅くします。 そのような点眼液の成分として、油が使用されます(精製ひまわり、桃またはアプリコット、魚油)。
点眼薬の作用を長引かせる2番目の方法は、合成増粘剤を導入して溶液の粘度を上げることです(表30.6を参照)。 天然の増粘剤は薬物の微生物学的安定性を低下させるため、使用されていません。
例1
pHの調整と抗酸化剤の導入によるスルファシルナトリウム溶液の安定化
工場製造用の30%処方スルファシルナトリウム溶液 | 10; 20; 薬局の処方箋によると、スルファシルナトリウムの30%溶液、新生児用10および20%を含む |
スルファシルナトリウム-300 gメタ重亜硫酸ナトリウム-5 g水酸化ナトリウム溶液-1 gからpH 7,7-8,0 注射用水-最大1リットルパッキング:慣らし運転用のボトル滅菌条件:温度100°C-30分賞味期限-26か月 | スルファシルナトリウム-100 g、200 g、 300グラム チオ硫酸ナトリウム-1.5 g、1.5 g、1.5 g 1M塩酸溶液:3.5 ml; 3.5 ml; 3.5 mlの精製水-最大1 l。溶液のpHは7.5〜8.5です。包装:流し込み用ボトル。滅菌条件:温度 120?C-8分 賞味期限-1ヶ月特徴:目の粘膜に対するアルカリおよびメタ重亜硫酸ナトリウムの刺激効果の低減 |
ご注意厚生省の命令によると? 308。
表30.6点眼薬の作用を長引かせる
ご注意OTC眼科用医薬品に関するFDA諮問審査パネル、最終報告書、12月 1979年。
30.3。 眼科用溶液の包装のための風袋と包装
点眼液には、ドロッパーボトル(図30.2)とガラスチューブボトルが使用されます。これらはゴム製の栓で閉じられ、アルミニウムキャップで密封されています。 ボトルは、ガラス管(droot)ブランドのNSで作られています。 ボトルは医薬品の包装と保管を目的としています。 バイアルはTU 9461-010-00480514-99に対応します(図30.2)。
ラバーストッパーABは、ドローンの薬瓶をコルキングするためのものです。 ゴム製ストッパーはTU 38.006108-95に準拠しています。
アルミニウムK-1キャップ(TU 9467-004-39798422-99)。 それらは、厚さ0.2 mmのアルミ箔で作られています(図30.3)。

図 30.2。ポリエチレンおよびガラス点滴ボトル

図 30.3。ガラス管(droot)ブランドNSのボトル; ゴムグレードAB製のプラグ; キャップアルミニウムK-l
生産プロセスでは、エンジンオイルを洗浄するために、スタンピングおよび化学処理後に脱脂を実行することが不可欠です。
30.4。 アイドロップ機器
アルミニウムキャップPOK-1を圧着するためのツール
(図30.4)。 代用血液と輸液溶液が入ったコーキングボトル、および直径20 mmの無人機のバイアル用に設計されています。
動作原理:デバイスは手動駆動を使用して動作します。 キャップの圧着は、圧着ノズルを垂直面内で下に移動することにより実行されます。 ノズルはボトルの首(ボトル)を捕捉し、トロイダルスプリングを圧縮することで圧着します。
主な機能と利点:
コンパクトでポータブルなデスクトップタイプ。
軽量(5 kg以下);
圧着ヘッドとサポートの迅速な交換の可能性;
さまざまな種類のボトルやボトルに簡単に再構成できます。
半自動シーミングマシンPZR-M。 薬局および医薬品製造用の10〜500 mlのアルミニウムキャップK-1、K-2、K-3、K-4、K-5の容量を持つ滑らかでネジの付いたネックを備えたあらゆるタイプのバイアルおよびボトルの栓抜き用に設計されています。 GMP製薬機器の要件を満たしています。 生産性-最大1300 fl./h
(図30.5)。
薬物のポンピングおよび分割充填のための設置。 Kontur-P4の設置は、5 mlの倍数の用量の薬液のろ過、ポンピング、および部分充填を目的としています。 シリコーンゴムとの長期接触を可能にするあらゆる液体に使用されます。 その助けを借りて、薬、生物学的および他の液体は10から400mlの容量を持つ容器に注がれます。 その流路は簡単に洗浄および滅菌されます。
動作原理:ディスペンスされる液体物質はist動計量ポンプの入口でろ過され、per動シリコーンホースと携帯用注入ヘッドを介して、5 mlの液体を充填ボトルに供給します。
30.5。 アイドロップとソリューションを生産するための技術スキーム
水道水で外側と内側から新しい皿を洗い、50-60°Cに加熱された洗浄液に20-25分浸します マスタード1:20の懸濁液、Desmolの0.25%溶液、Progress、Lotus、Astraの0.5%溶液、SPMSの1%溶液(スルファノールとトリポリリン酸ナトリウム1:10の混合物)も使用します。 ひどい汚染の場合は、特別な指示に従って、皿をマスタードの5%懸濁液または洗剤の溶液に2〜3時間浸します。
洗浄した皿は、260°Cの熱風で60分間滅菌されます。 使用されていた料理は1%の溶液で消毒されます

図 30.4。POK-1デバイス
活性化クロラミン-30分; 0.5%の洗剤を加えた3%の新たに調製した過酸化水素溶液-80分または0.5%のデスモル溶液-80分。
精製水は、新たに調製され、適切なモードで滅菌されて使用されます。
コルキングボトルには、IR-21(シリコン)、IR-119、IR-119A(ブチルゴム)の特殊なゴムのチューブを使用します。 新しいゴム栓は、指示に従って硫黄、亜鉛、その他の物質を表面から除去するように処理されています。 使用済みの栓を純水で洗浄し、20分間2回煮沸し、121 + 2℃で45分間滅菌します。
ゴム栓で栓をした溶液を含むバイアルは、機械的不純物がないように制御します。 溶液の初期制御中に機械的不純物を検出すると、ろ過されます。
製造後、溶液は化学分析にかけられます。これは、真正性(定性分析)および剤形を構成する医薬品の定量的内容(定量分析)を決定することから成ります。 結果が正の場合、金属キャップで巻き込まれています。
巻かれた溶液ボトルには、名前、バッチ番号を示すアルミニウムのキャップが付いています。
ラベルの付いたバイアルをオートクレーブに入れ、容器内の溶液の量を考慮して、グローバル基金の指示に従って滅菌します。 滅菌後、ソリューションは機械的介在物の含有量について分析されますか? 308.拒否されたバイアルはリサイクルできません。
拒否されたバイアルは、グローバル基金または連邦議会の要件に従って完全な分析のために送信されます。
無菌分析のためにサンプルが採取されます。 良好な結果が得られた場合は、マークが付けられ、段ボール箱に梱包されます。 眼科用溶液を得るための典型的なスキームはスキーム30.1に示されています。
したがって、点眼液が少量であるため、薬局方の要件により禁止されているリストAおよびBの重量が0.05 g未満のサンプルを計量する必要がある場合を除き、点眼液を製造する技術は、実際には注射液を製造する技術と変わりません。 この障害を克服するには、それが推奨されます
スキーム30.1点眼薬および点眼液の製造技術

濃縮溶液を使用し、その組成と技術はロシア連邦保健省の順序で提示されていますか? 214。
30.6目薬の製造例
例1
薬用物質の溶解による点眼薬の調製Rp .: Solutionis Atropini sulfatis 1%-10 ml
D.S. 左目で1日2回2滴。 保健省の順番ですか? 214が示されています。
-溶液の組成:硫酸アトロピン0.1 g、塩化ナトリウム0.08 g、純水10 ml
-滅菌条件:温度100 "C-30分。
-ストレージ:リストAによる。
-有効期限:温度3-5 "C-30日。
無菌条件下で、0.1 gの硫酸アトロピンと0.08 gの塩化ナトリウムを、10 mlの精製水を含むシリンダーからの約5 mlの精製水に滅菌スタンドで溶解します。 この溶液を、事前に洗浄したろ紙と医療用脱脂綿(または孔径10-16μmの滅菌ガラスフィルター)で滅菌中性ガラスボトルにろ過し、残りの水を同じフィルターでろ過します。
溶液は、硫酸アトロピンと塩化ナトリウムの定性的および定量的含有量、および機械的不純物がないことを監視します。
ボトルはコルク栓をされ、アルミキャップで包まれ、マーキングされ、蒸気滅菌器で流れる蒸気で滅菌されます。 滅菌後、点眼薬には機械的な不純物がないかどうかがチェックされ、ピンクのラベルと追加のラベル「取り扱いに注意」が飾られています。 ボトルは密封され、レシピのコピーが作成されます。
例2
Rpの濃縮溶液からの点眼剤の調製:Riboflavini 0.001 Acidi ascorbinici 0.02 Kalii iodidi 0.3
Solutionis acidi borici 2%-10 ml
M.D.S. 両目で1日2回2滴。
このレシピにはNDはありません。 計算では、規定量のヨウ化カリウムと酸のため、ホウ酸溶液が高張であることが示されています。 すべての成分は、滅菌濃縮溶液の形です。
3.3 mlの精製水、4%のホウ酸溶液と組み合わせた5 mlの0.02%リボフラビン溶液、0.2 mlの10%アスコルビン酸溶液、1.5 mlの20%ヨウ化カリウム溶液を滅菌バイアルで測定します。
機械的不純物がないかどうか、溶液を監視します。 ボトルはコルク栓をされ、ラベルで満たされています。
例3
点眼薬の内部調剤の準備Rp .: Riboflavini 0.002 Solutionis Citrali 0.01%-10 ml
保健省の命令で指定された言葉に従って、10本のボトルの溶液を次のように調製します。リボフラビン0.02 gと塩化ナトリウム0.9 gを精製熱水99 mlに溶解します。 溶液をろ過して滅菌します。 溶液を冷却した後、無菌条件下で1mlの1%アルコールシトラール溶液をそれに加えます。
ルール7
シトラールは滅菌に耐えられず、ゴム栓材料に吸収されます。 したがって、そのアルコール溶液は無菌条件下で滅菌点眼液の栓の下に注入されます。
賞味期限-25°C以下の温度で2日間または5日間-3-5°Cの温度で 滴の貯蔵寿命が短い理由は、ゴム栓での収着によるシトラールの濃度の低下です。
ボトルをプラスチックキャップで覆うと、涼しい暗い場所に保管した場合に、ドロップの保存期間を最大1か月まで延長できます。
30.7。 アイソリューション
眼科用液剤は、ローション、灌注液(眼科手術の灌漑用)、ソフトコンタクトレンズの洗浄、消毒、保管用の形態で使用されます。
点眼薬の品質を確保する方法は、基本的に点眼薬と同じです。滅菌され、安定しており、機械的不純物を含んでいない必要があります。 ローションと灌漑ソリューションは等張である必要があり、これは滴の製造よりも重要です。 ほとんどの場合、アイローションは処方液です:フラシリナ、重炭酸ナトリウム、ホウ酸、乳酸エタクリジン。
例4
Rp .: Solutionis Furacilini 1:5000 100 ml D.S. アイローション。
厚生省の命令? 214塩化ナトリウムで等張化された0.02%フラシリナ溶液(0.85%)。 溶液は100°Cで30分間、または120 + 2℃で8分間滅菌されます。
溶液の保存期間は、暗い場所で25°Cを超えない温度で30日間です。
無菌条件下で、フラシリナ0.02 gおよび塩化ナトリウム0.85 gを、100 mlの精製熱水に入れた滅菌スタンドに溶解します。 溶液をろ過して中性ガラスの滅菌ボトルに入れ、機械的不純物がないことを確認します。 溶液ボトルは、ゴム栓で栓をし、アルミキャップで包み、印を付けて滅菌します。 滅菌後、機械的不純物がないかどうか溶液を再チェックし、ラベルを記入します。
30.8。 アイオイル
溶液および薄い懸濁液に加えて、軟膏は眼科用剤形の形で使用され、それはまぶたの上に置くことによって使用されます。 軟膏の組成は多様です。 多くの場合、抗生物質、スルホンアミドなどの眼軟膏があります。
適用の目的は異なる場合があります(消毒、麻酔、瞳孔の拡大または縮小、眼圧の低下など)。
ルール8
眼軟膏には、懸濁液や溶液よりも眼の結膜の薬剤を遅らせる性質があります。 軟膏は粘性があり、涙液で洗い流されないため、投与後のほとんどの軟膏は一時的に視力を損ないます。 したがって、夜間の使用には目の軟膏をお勧めします。
眼軟膏の場合、一般的な要件(薬物の均一な分布、無関心および基剤の持続性)に加えて、いくつかの追加要件が作成されます。
1.軟膏基剤は不純物を含んではならず、中性で、無菌で、目の粘膜に均一に分布している必要があります。
2.眼軟膏は、無菌状態に従って準備する必要があります。
3.目への刺激を防ぐため、薬物の粒子サイズは最小限に抑える必要があります。
30.8.1. 軟膏基金
ワセリンは、刺激性、持続性、化学的無関心がないため、眼軟膏の軟膏として広く使用されています。 しかし、疎水性に起因するワセリンは、角膜を洗浄する涙液とうまく混合せず、目の軟膏の基礎としては不快です。
GFは、10部の無水ラノリンと90部のワセリン(眼軟膏のグレード)からなる混合物を基本として提供します。 この種のワセリンが存在しない場合、通常のワセリンは次のように精製されます。ワセリンはエナメル容器で溶かされ、1〜2%の活性炭が加えられます。 混合物の温度を150℃に上げ、1〜2時間加熱を続け、熱いワセリンをペーパーフィルターでろ過し、滅菌瓶に注ぎました。 有機不純物の不在および中和の化学分析の後、ワセリンがベースとして使用されます。
30.8.2. 眼軟膏の製造技術
眼軟膏は、皮膚軟膏のように準備されますが、無菌状態になります。 すべての補助材料、軟膏基剤、高温の作用に耐えることができる薬物、缶は、世界基金で指定された方法に従って滅菌されます。 眼軟膏の製造における重要な要素は、投与された医薬品の最適な分散度の達成です。 物質の必要な分散は、関連する基礎を少量の液体で事前に溶解するか、徹底的にこすることによって達成されます。 アルカロイドの塩、ノボカイン、プロタルゴールなどの水に溶ける物質は、最小限の量の滅菌水に溶かしてから、軟膏基剤と混合します。
ルール2
不溶性または難溶性の物質(ゼロフォーム、酸化亜鉛)は、少量の滅菌流動パラフィン、グリセリンまたは水で注意深く分散させた後、微粉末の形で眼軟膏の組成物に導入されます。
ルール10
火傷を引き起こす可能性のある物質(硫酸亜鉛、プロタルゴール)などを含む軟膏の製造には特に注意が払われ、眼の軟膏に導入されます。
例5
Rp。:Unguenti Zinci sulfatis 0.5%-10.0 D.S. 目の軟膏。 右目のまぶたに1日2回。 無菌条件下で、0.05 gの硫酸亜鉛を数滴の滅菌精製水(同じ皮膚科用軟膏とは異なり、同じ医薬物質を含む)の滅菌乳鉢に溶解し、眼軟膏用の滅菌基剤10 gを加え、完全に混合します。 軟膏を滅菌ガラス瓶に移します。滅菌ガラス瓶には、ピンクの目軟膏ラベルで装飾された、滅菌ガスケット付きのねじ込み式プラスチック蓋が付いています。
点眼薬と同様に、眼軟膏の製造において、最新版の世界基金および外国の薬局方に示されているように、防腐剤を追加することが推奨されます。 この目的のために、塩化ベンザルコニウム1:1000、ニパギン0.12%とニパゾール0.02%の比率のニパギンとニパゾールの混合物、ソルビン酸(0.1-0.2%)、および医療用途に承認された他の防腐剤が提案されています。
パッキング
目の軟膏は、しっかりとフィットする蓋付きの滅菌ガラスまたは磁器の瓶で放出されます。 使用中に軟膏が汚染されないように、患者がまぶたの後ろに軟膏を置く必要がある滅菌スパチュラで軟膏を放出することをお勧めします。 アイチューブの使用をお勧めします。
まぶたの軟膏を入れることができる細い先端を持ち、低容量(最大3.5 gの軟膏)。
品質管理
品質管理は薬局方の要件と保健省の命令に従って実施されていますか? 305および214。
アプリ
目の軟膏を適用する方法。 患者情報 (図30.7)
1.手を洗ってください。
2.軟膏を付けたチューブを数分間手で持ち、ベースを溶かします。
3.鏡の前に立って、上を見上げ、下まぶたを少し下に引きます。
4.まぶたの縁(約0.5〜1.0 cm)に少量の軟膏を慎重に置きます。
重要:軟膏を塗るときは十分に注意してください。 チューブの先端がまぶた、眼球、指、またはその他の表面に触れないようにしてください。
5.目を閉じて、眼球をゆっくりと回転させて、軟膏を塗ります。 軟膏が均等に分布するように、数回点滅させることができます。
7.チューブカバーを閉じます。 軟膏を塗ると、視力が一時的に悪化します。 心配しないでください-それは合格します。

図 30.7。 目の軟膏の適切な適用
セキュリティの質問
1.点眼後の二次的な眼感染の考えられる原因は何ですか? そのような場合を除外するための目薬の技術はどうあるべきですか?
2.点眼薬と注射液の品質指標を比較します。 この比較からどのような結論を導き出すことができますか?
3.点眼薬の無菌性は、使用中にどのように確保できますか?
4.点眼液の組成-アナプリリン溶液には、賦形剤:チオ尿素、塩化セチルピリジニウム、クエン酸-リン酸緩衝溶媒が含まれます。 これらの物質の機能的な目的は何ですか?
5.点眼薬の点滴後に生じる不快な感覚の考えられる原因は何ですか?また、これらの現象を排除する方法は何ですか?
6.点眼液の品質指標を比較します(長期にわたる作用と安定性)。 これらの指標を確保する例を挙げてください。
7.皮膚および眼軟膏の製造技術の類似点は何ですか? 彼らの技術の違いを説明するには?
8.眼科用剤形の品質と製造技術を改善するための主な方向は何ですか?
テスト
1. 厚生省の命令? 214確立-点眼液に追加される等張性および安定化物質の濃度と体積(または質量)を示す必要があります。
1.パスポートだけでなく、レシピにも。
2.パスポート。
3.レシピで。
4.要件については、登録簿に適切な碑文を添付してください。
2. 眼用剤形は、以下の場合、注射液と同様に無菌条件下で調製されます:
1.無菌。
2.非滅菌。
3.滅菌のモードおよび条件に関係なく。
3. 間違った答えを選択してください:点眼薬の調製には:
1.滅菌溶媒-精製水、等張緩衝液、オイル。
2.滅菌バイアルとプラグ。
3.滅菌補助材料(フィルター、漏斗、ピペット)。
4.無菌薬。
4. 間違った答えを選択してください:少量(最大30 ml)を製造する場合:
1.あらかじめ湿らせて洗浄したペーパーフィルターを使用します。
2.ディスペンス用に精製ボトルで滅菌水をすすぐ。
3.溶解は溶媒の半分の容量で行われます。
4.溶液の量は公称値に等しくなければなりません。
5. 眼科用剤形の濃縮溶液の製造および1ヶ月未満の子供向けの混合物の製造は、ビュレット設置用の濃縮物の製造と段階によって異なります。
1.無菌製造条件を作成します。
2.補助材料および器具の滅菌。
3. NDに従った製造後の溶液の滅菌。
4.フィルタリング。
5.標準化。
6. 硫酸マグネシウムの等張液30 ml(塩化ナトリウムの等張性当量は0.14)を作るには、薬を服用する必要があります:
1.4 g
2.6 g
3. 1.92 g。
4. 0.04 g。
5.27 g
7. ピロカルピン塩酸塩の1%溶液10 mlを製造するには、塩化ナトリウムを摂取する必要があります(塩化ナトリウムの等張性当量は0.22です)。
1.0.022 g
2.0.090 g
3.2.220 g
4.0.068 g
5.680 g
6. 0.000 g。
7. 0.900 g。
8. 10 mlの精製水に0.2ピロカルピン塩酸塩(塩化ナトリウムの等張性当量は0.22)を含む点眼液、涙液:
1.等張性。
2.低張。
3.高張。
9. 点眼剤-10%四ホウ酸ナトリウム溶液10 ml(塩化ナトリウムの等張性当量は0.34)、涙液:
1.等張性。
2.低張。
3.高張。
10.点眼薬組成物を作成する必要があります。
リボフラビニ0 02%-10 ml Acidi Borici 0.2。
どの製造オプションを最適として選択しますか:
1.固体の溶解。
2. 1成分濃縮溶液の使用。
3.組み合わせた濃縮溶液の使用。
11. 点眼剤の製造に安定剤を追加します。
1.リボフラビン。
2.ピロカルピン塩酸塩。
3.スルファシルナトリウム。
4.コラルゴル。
12. 以下を含む熱殺菌点眼液:
1.ベンジルペニシリン。
2.レゾルシノール。
3.コラルゴル。
4.クロラムフェニコール。
点眼薬は、水性の油性溶液です。 目への点滴注入を目的とした最も薄い懸濁液と乳剤。
これは公式の剤形です。 グローバル基金には共通のグループ記事があります。 目薬に加えて、目の軟膏、目のフィルム、ローション、目の電気泳動用の溶液は、目の治療に使用されます。
点眼薬の要件:
1.不妊。
健康な目の涙液は無菌です。 天然の抗生物質であるリゾチームが含まれています。 炎症性眼疾患では、リゾチームの量が減少し、非滅菌液の投与により、視力低下を含む眼感染症を引き起こす可能性があります。
したがって、薬局で準備された点眼薬は、医師の助言なしで無菌でなければなりません。 注文番号308に従って、点眼薬は無菌条件下で作成されます。
点眼薬の命名法と滅菌レジメンは、注文番号214(付録10)に記載されています。
滅菌には、2つのモードが使用されます:圧力下の飽和蒸気120 0〜8分、または流体蒸気100〜30分。 滅菌方法の選択は、加熱時の薬物の特性に依存し、214番で示されています。
LHC分析のために、1四半期に2回目薬の無菌性をチェックします。
点眼薬を使用すると、無菌性が損なわれます。 工場や薬局の条件での微生物の播種を防ぐため、点眼薬の量は5〜15 mlを超えません。 工場では、TUに従って防腐剤が追加されています。ニパギン、ニパゾール、クロロブタノール水和物などです。
薬局の状況では、医師の指示に従って防腐剤が追加されます。
防腐剤の特性は次のとおりです。薬理作用に関連して、ホウ酸の2%溶液、クロラムフェニコールの0.2%溶液。
2.清潔さ。
目の粘膜をさらに刺激し、それを傷つける機械的不純物の存在は許可されません。 点眼薬は、長繊維の綿棒で湿らせたSSBFでろ過します。 清潔さを2回確認してください:滅菌の前後。
3.等張性。
点眼は、点滴中の不快感(かゆみ、火傷、痛み、流涙、粘膜の発赤)を避けるために、等張でなければなりません。
点眼薬は、医師の指示に関係なく、等張性です。
等張化剤:塩化ナトリウム、硝酸ナトリウム、硫酸ナトリウム。
硫酸ナトリウムまたは硝酸ナトリウムは、ナトリウムの場合に使用されます
塩化物は薬物と化学反応を起こします:
硝酸銀溶液は、硝酸ナトリウムで等張化されます。
硫酸亜鉛溶液は、硫酸ナトリウムで等張化されます。
・10 mlあたりの計算
・5mlの計算
0,045-(薬物のサンプル*等張性等価物)
・等張性塩化ナトリウム溶液について
クロラムフェニコール、シトラール、リボフラビン、フラシリンのドロップが準備されています。
この場合、サンプルの重量はわずかであり、浸透圧は発生しません。
・アイソトーンしないでください:
1.薬物の濃度が3%以上の場合
2.カラーゴル、プロタルゴルのソリューション。 塩化ナトリウムは電解質であり、コロイド溶液を破壊します。
4.集中の正確さ。
準備は、質量によって行われます-体積法で体積を増やします。
PHC-滅菌の1回前:
必須:点眼薬および軟膏、PKUの対象
(麻薬、強力、スケジュールA)
新生児の目薬
点眼薬の集中ソリューション
残り:選択的に、まず第一に。 子供向けのLFへの特別な注意、ただしシフトごとに少なくとも3つの剤形。
5.安定性(抵抗)。
安定剤は、注文番号214に従って、または医師の指示に従って追加されます。 安定剤の量は、PPCとレシピの裏に示されています。
6.アクションの延長。
生理的な理由から、点眼薬は粘膜に長時間置くことはできません。 これは、1日数回目薬の使用につながります。 溶液の粘度を上げると効果が長くなります。 粘度を上げるために、医師の指示に従ってカルボキシメチルセルロースとポリビニルアルコールを投与してもよい。 延長は、主にTUに従って工場で行われます。
点眼薬の準備に関する規則:
1.医師は、注文番号110に従って点眼薬を処方します。
2.複雑な処方の成分の適合性を確認する必要があります
3.集中に注意してください。
4.溶剤を使用する場合:
・注射用水。 点眼薬は、通常注射用の蒸留水が入った箱で作られます。
・二酸化炭素、アンモニウム塩、還元物質を含まない精製水。
・オイルは無菌です。
・塩化ナトリウム溶液は等張です。
5.点眼薬は無菌条件下で調製されるため、ラベルは「設計のための統一規則」に従って事前に処方されています。 要件とレシピがボックスに入力されていないため、構成はラベルに配置されます。
6.調理方法を選択し、コントロールパネルの背面で計算を実行します。
7.等張化剤の量は、AUCおよびレシピの裏に示されています。
8. PPCの調理時間は、パイロジェンフリーの要件がないことを示していません。
9.慣らし運転下でコルク栓をし、同時に注射液と同様に滅菌のマーキングを行います。
10.点眼薬は分析のために選択的に与えられます。
11.滅菌後、清潔さ、色、バイアルの完全性、コルクの堅さのために結婚が必須です。
点眼薬を準備する方法(方法)。
・「2つのシリンダー」の方法
・濃縮溶液を使用した2シリンダー法
・倍額方式。
調製方法の選択は、調製した溶液の量と薬物のサンプルを正確に計量する能力に依存します。
「2シリンダー」方式。
溶液の量が10 mlを超えず、薬物のサンプルを計量の規則に従って手動スケールで計量できる場合に使用されます。
この場合、濃度と体積の精度が達成されます。
ペニシリンバイアルの規定量の半分の水の中で、薬用物質、等張化剤を溶解し、PTDVで湿らせたSBPを通して溶液をメスシリンダーにろ過します。 同じフィルターを通して、水を所定の量にします。 休暇のためにペニシリン瓶に注いだ。
タスク。
慢性患者の処方に従って、塩酸ピロカルピン1%-10 ml点眼液の溶液を調製します。
応答アルゴリズム。
Rp:ソル。 ピロカルピニ塩酸塩1%-10 ml 0.1ピロカルピン
D.S. 目薬。 0.068(0.07)NaCl
入水用に最大10 mlの水
機能:
特徴
1.塩酸ピロカルピンは、スケジュールAの薬ですが、PKUの対象ではありません。 処方箋フォーム107-Uには、「慢性患者へ。 1年間、10日ごとに2つのバイアルをリリースします。 追加の碑文は、医師の印章と署名、および「レシピ用」の印で封印されています。レシピは1年間有効です。
2.注文番号214(1%、2%、4%、6%)で濃度を確認し、赤鉛筆(注文番号330)で下線を引きます。
6.点眼薬は等張でなければなりません。
0.09-(薬物のサンプル*等張性等価物)
= 0,09 –(0,1*0,22)=0,068=0,07
等張化剤の量は、PPCおよび裏面に示されています。
ピロカルピンの計算された量は、手持ち式スケールで計量することができ、溶液の量は10 mlなので、「2シリンダー」法を使用して調製します。
8.薬物はリストAであるため、次のとおりです。
・レシピの裏に記入して薬剤師技術者から受け取ります
・パスポート-「A」
・PHC-滅菌の1回前に必須
・追加ラベル「取り扱いに注意」
・慣らし運転中のコルクとして、密封されていません。
10.点眼薬は無菌でなければなりません。 120 0-8分 追加のラベル「滅菌」は必要ありません。
11. 30日間の有効期限。
12.患者は帰るまで安全な場所に保管されます。
13.緑内障の治療に使用されます。
料理。
ペニシリンバイアルに約5 mlの水を注ぎます。薬剤師から入手します-技術者は0.1ピロカルピン塩酸塩を溶解します。 0.07塩化ナトリウムを計量して溶解します。 フィルターを準備します。 溶液をシリンダーにろ過し、同じフィルターを通して体積を10 mlにし、分析のために1 mlを注ぎます。 PPCに入力します。
溶液は、分注のためにペニシリン瓶に注がれ、清浄度がチェックされ、事前にマークされた慣らし運転のためにコルク栓がされています。
ソル Pilocarp。 1%
09.09.09署名。
120〜8分間オートクレーブで滅菌します。 私たちは結婚をします。 休暇に出かけます。
タスク。
処方に従って、スルファシルナトリウム10%10 mlの点眼液を調製するには
応答アルゴリズム。
Rp:ソル。 スルファシル-ナトリイ10%-10 ml 1、0スルファシルナトリウム
D.S. 目薬。 0.015(0.02)チオ硫酸ナトリウム
0.1 M HCl -0.35 ml
入水用に最大10 mlの水
機能: この剤形は、点眼用の複雑な液体水溶液です。
特徴
2.注文番号214(10%、20%、30%)で濃度を確認します。
3.「登録の統一規則...」の構成でラベルを書きます。
5.点眼薬は等張でなければなりません。 この場合、濃度は大きく、滴は高張です。 滴を分配するとき、患者は不快感を警告されなければなりません。
6.点眼薬は安定している必要があります。 スルファシルナトリウムは酸化されやすい物質です。 注文番号214に従った安定化。
濃度に関係なく、10 mlあたりの安定剤の組成
0.015チオ硫酸ナトリウム
0.1 M HCl -0.35 ml
HCl + Na 2 S 2 O 3 NaCl + H 2 O + SO 2 + S
SO 2-酸化防止剤として機能します。
安定剤の量は、PPCとレシピの裏に示されています。
7.溶液の濃度は正確でなければなりません。
計算された薬物の量は、手持ち式スケールで計量することができ、溶液の量は10 mlなので、「2シリンダー」法を使用して調製します。
8.滴の例外として、0.1 M HClを分析ピペットで加えます。
9.溶解順序:チオ硫酸ナトリウム、スルファシルナトリウム、0.1 M HCl。
10.点眼薬はきれいでなければなりません。 湿ったSSFをPTDVでろ過します。 清潔さを2回確認します。
11. PHC-主に滅菌の1回前に選択的に。
12.点眼薬は無菌でなければなりません。 120 0-8分で滅菌します。 追加のラベル「滅菌」は必要ありません。
13. 30日間の有効期限。
14.結膜炎の治療、新生児のgo病の予防に使用されます。
タスク。
処方グリセリンで点眼薬を準備します。
応答アルゴリズム。
Rp:ソル。 グリセリン40%-10 ml 4.44グリセリン90%
D.S. 目薬。 入水用に最大10 mlの水
機能: この剤形は、点眼用の複雑な液体水溶液です。
特徴
1.処方箋を確認します。 処方フォームフォーム107-U。
2.治療効果に応じて濃度を確認します。
3.「登録の統一規則」の構成でラベルを書きます。
4.注文番号308および309で無菌条件下で調理します。
5.コントロールパネルの裏側で計算を実行します。
6.無水物に関するグリセリン数
7.点眼薬は等張でなければなりません。 この場合、濃度は大きく、滴は高張です。 滴を調剤するとき、患者に不快感を警告する必要があります。
この場合、グリセリンは粘性液体であるため、質量-体積法で調製します。
9.点眼薬はきれいでなければなりません。 湿ったSSFをPTDVでろ過します。 清潔さを2回確認します。
12.賞味期限は30日間です。
13.脱水剤として使用されます。
タスク。
キニーネ塩酸塩で処方点眼薬を準備します。
応答アルゴリズム。
Rp:ソル。 チニーニ塩酸塩1%-10 ml 0、1キニーネ塩酸塩
D.S. 目薬。 0.08 NaCl
入水用に最大10 mlの水。
機能: この剤形は、点眼用の複雑な液体水溶液です。
特徴
1.処方箋を確認します。 処方フォームフォーム107-U。 リストB.薬物
2.注文番号214(1%)で濃度を確認します。
3.「登録の統一規則...」の構成でラベルを書きます。
4.注文番号308および309により、無菌条件下で調理します。
5.塩酸キニーネMP 1:30、お湯に溶かします。
6.点眼薬は等張でなければなりません。
0.09-(薬物のサンプル*等張性等価物)
= 0,09 –(0,1*0,14)=0,076=0,08
等張化剤の量は、AUCおよびレシピの裏に示されています。
7.点眼薬は安定している必要があります。 キニーネ塩酸塩はアルカロイド塩です;同じ名前のイオンの存在下では、塩基が沈殿する場合があります。 したがって、キニーネ塩酸塩は7〜8 mlの熱水に溶解します。 完全に冷却した後、塩化ナトリウムを加えます。
8.溶液の濃度は正確でなければなりません。
計算された薬物の量は手動スケールで計量することができ、溶液の量は10 mlなので、調製には「2シリンダー」法を使用します。
9.点眼薬はきれいでなければなりません。 湿ったSSFをPTDVでろ過します。 清潔さを2回確認します。
10. PHC-選択的に主に滅菌の1回前。
11.点眼薬は無菌でなければなりません。 120 0-8分で滅菌します。 追加のラベル「滅菌」は必要ありません。
12. 120日の賞味期限。
13.単純な微生物によって引き起こされる病気の治療に使用されます。