Farmakodinamika
Farmakodinamika je odjeljak opće farmakologije koji proučava značajke djelovanja lijekova na organizam. Naime, farmakodinamika proučava:
mehanizmi djelovanja lijekova;
konačni farmakološki efekti;
ovisnost djelovanja lijekova od različitih stanja;
efekti lijekova nakon opetovane primjene;
kombinirano djelovanje lijekova;
nespojivost lijekova;
nuspojave ljekovite tvari.
Mehanizmi djelovanja lijekova su načini na koje tvari uzrokuju farmakološke učinke. Glavni mehanizmi djelovanja lijekova uključuju:
Fizički.
Mehanizam direktne hemijske interakcije.
Membrana (fizikalno-hemijska).
Enzimski (biohemijski).
Receptor.
Direktna hemijska interakcija. Ovo je prilično rijedak mehanizam djelovanja lijekova, čija je suština u tome da lijekovi direktno stupaju u interakciju sa molekulima ili ionima u tijelu. Takav mehanizam djelovanja ima, na primjer, unitiolni lijek koji pripada grupi protuotrova. U slučaju trovanja tiolnim otrovima, uključujući soli teških metala, unitiol ulazi u izravnu hemijsku reakciju s njima, što rezultira stvaranjem netoksičnih kompleksa koji se izlučuju mokraćom. Tako djeluju i antacidi koji ulaze u izravnu kemijsku interakciju sa solnom kiselinom, snižavajući kiselost želučanog soka.
Membrana (fizikalno-hemijske) mehanizam. Povezana je s učinkom lijekova na jonske struje (Na +, K +, Cl - i druge), koje određuju transmembranski električni potencijal. Prema ovom mehanizmu javljaju se anestetici, antiaritmički lekovi, lokalni anestetici itd.
Enzymatic (biohemijska) mehanizam. Taj mehanizam određuje sposobnost nekih lekova da aktiviraju ili inhibirajuće na enzime. Arsenal lijekova s \u200b\u200btakvim mehanizmom djelovanja je vrlo širok. Na primjer, antiholinesterazni lijekovi, inhibitori monoamin oksidaze, blokatori protonske pumpe itd.
Receptorni mehanizam. U ljudskom telu postoje visoko specifične biološki aktivne supstance (posrednici) koji stupaju u interakciju sa receptorima i menjaju funkcije različitih organa ili tkiva u telu.
Receptori su makromolekularne strukture sa selektivnom osjetljivošću na određena hemijska jedinjenja. Uz interakciju lijekova s \u200b\u200breceptorima, događaju se biokemijske i fiziološke promjene u tijelu, praćene jednim ili drugim kliničkim učinkom.
Pozvani su posrednici i lijekovi koji aktiviraju receptore i uzrokuju biološki učinak agonisti. Ljekovite tvari koje se vezuju za receptore, ali ne uzrokuju njihovu aktivaciju i biološki učinak, smanjuju ili uklanjaju učinke agonista, nazivaju se antagonisti. Dodijelite također agonisti antagonista - tvari koje djeluju različito na podtipove istih receptora: stimulišu neke podvrste receptora, a blokiraju druge. Na primjer, narkotički analgetik nalbufin stimulira receptore opioidne kappe (dakle smanjuje osjetljivost na bol) i blokira opioidne mu receptore (dakle, manje je opasan u pogledu ovisnosti o lijekovima).
Sposobnost tvari da se vezuju za receptore naziva se terminom "afinitet". U odnosu na iste receptore, afinitet različitih tvari može biti različit.
Razlikuju se sledeće vrste receptora:
Recepti za membranu plazme:
tip kanala: kolinergički receptori N-tipa, H-holinergički receptori mišićnog tipa, GABA receptori;
g-proteinski receptori: α- i β-adrenergički receptori, M3 -holinoreceptori;
receptori integrativnog tipa: NO receptor.
Citosolna.
Mitohondrijalni.
Nuklearna
Receptori tipa kanala
N n holinergički receptor nervnog tipa (CNS, autonomne ganglije, sinokarotidna zona, hromafin tkivo nadbubrežne žlijezde). Nakon vezanja acetilholina (AX) s H n -holinergičkim receptorima, Na + kanali se otvaraju i Na se odvodi u ćeliju noseći pozitivan naboj. Postinaptička membrana je depolarizirana. Postoji akcijski potencijal koji se pomiče duž membrane neurona, otvarajući električno ovisne Na + kanale. U postganglionskom vlaknu nastaje nervni impuls (Sl. 6).
Sl. 6. N n -holinergički receptor
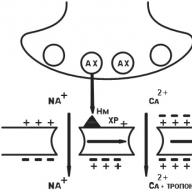
N m mišićni tip holinergički receptor (membrane skeletnih mišićnih stanica). Početni procesi su slični, ali otvaraju se Ca ++ kanali o električnom razvoju. Ioni Ca ++ ulaze u mišićna vlakna, Ca ++ se oslobađa iz sarkoplazmatskog retikuluma. Razina Ca ++ raste, što inducira kontrakciju mišića (Sl. 7).

Sl. 7. N m-holinergički receptor
GABA receptori. Ovo su receptori za γ-aminobuternu kiselinu (GABA). GABA djeluje u interakciji s GABA receptorima, u čijoj strukturi postoje kloridni kanali. Kao rezultat stimulacije receptora, kanali se otvaraju i kloni ioni (Cl -) slobodno ulaze u ćeliju. Povećanje koncentracije jona hlora unutar ćelije dovodi do hiperpolarizacije membrane i smanjenja aktivnosti neurona. Teže je pobuđivati \u200b\u200btakvu ćeliju (sl. 8).
 Sl. 8. GABA receptor:
Sl. 8. GABA receptor:
GABA-R - GABA receptor, BD-R - benzodiazepinski receptor, BR - barbituratni receptor
Receptori povezani sa G protein
G-proteini, tj. Proteini koji se vežu za GTP (guanozin trifosfat), lokalizirani su u staničnoj membrani i sastoje se od α-, β- i γ-podjedinica. Oni (G-proteini) regulišu aktivnost određenih efektora (trenutni glasnici, sekundarni posrednici). Ovi glasnici mogu biti enzma (adenilat ciklaza, fosfolipaza); kanali za kalijum, kalcijum, natrijum; neke transportne proteine. Svaka ćelija može imati mnogo G-proteina, a svaka od njih reguliše aktivnost različitih glasnika, istovremeno mijenjajući funkciju stanice.
M 3 holinergički receptor (membrane glatkih mišića (MMC) i ćelije egzokrinih žlezda). Acetilholin stimulira M3 -XR vezan na G protein. Aktivira se fosfolipaza-C (FLS), koja katalizira cepanje PIDP (fosfatidilinozitol-difosfat) u ITP (inozitol trifosfat) i DAG (diacilglicerol). ITF koji ulazi u citoplazmu MMC oslobađa Ca ++ iz kavela .

Sl. 9. M3 -holinergički receptor
Ca ++ se veže na kalmodulin, aktivira miozin-kinazu (MK), koja katalizira fosforilaciju lakih lanaca miozina, što dovodi do kontrakcije ćelije (slika 9). Slično tome, impuls se prenosi u sinapsama sekretornih žlezda.
Norepinefrin stimulira α 1 adrenoreceptorPokretanjem sljedećeg lanca događaja:
Norepinefrin (HA) → α 1 -adrenoreceptor → aktivacija α-podjedinice G s-proteina → aktivacija PLL → cijepanje FIDF-a → porast ITF koncentracije → porast koncentracije Ca 2+ u stanici → Ca 2+ veže se na kalmodulin → aktivira se miozin-kinaza → lagani lanci fosforilat → laki lanac miozin → miozin u interakciji s aktinom → razvija se smanjenje MMC-a (Sl. 10).

Sl. 10. α 1 -adrenoreceptor
1 receptor(sl. 11). Norepinefrin → aktivira 1 -AP → aktiviranje α-podjedinice G-proteina → aktivacija AC → povećanje stvaranja cAMP iz ATP → porast koncentracije cAMP u kardiomiocitima → aktiviranje protein kinaza → fosforilacija proteina kalcijumovih kanala → povećanje ulaska Ca 2+ kroz kanale i povećanje koncentracije Ca 2+ u ćeliji → porast sile kontrakcija srca.

Sl. 11 1 receptor
2 receptor(sl. 12). ON → 2 -AR → aktiviranje α-podjedinice G-proteina → aktivacija AC-a → povećana tvorba cAMP → stimulirana protein-kinaza → kinaza koja katalizira fosforilaciju miozin-kinaze se cijepa, a aktivnost posljednjeg se gubi → fosforilacija miozina ne dolazi → MMC opuštanje.
Regulaciju oslobađanja HA iz nervnih završetaka vrši sam neurotransmiter nakon pobuđivanja presinaptičke membrane α 2 -AP. Emisija HA smanjuje se.

Sl. 12 Recept 2 receptora
Receptori integrativnog tipa
To su receptori koji su proteini koji prodiru kroz membranu. U tom slučaju vanjski dio proteina igra receptorsku ulogu, dok unutarnji dio igra katalitičku ulogu (Sl. 13).

Sl. 13 Integrirani receptor
Citosolni receptori
U fiziološkim uslovima, takvi receptori služe za vezanje steroidnih hormona (polni hormoni, glukokortikoidi). Ove tvari ulaze u stanicu i vezuju se za citosolne receptore. Ovaj kompleks prodire u jezgro i tamo mijenja rad genoma. Kao rezultat toga, mijenja se sinteza proteina u stanici (Sl. 14).

Sl. 14 Citosolni receptor
Mitohondrijski receptori
U mitohondrijama se nalaze i receptori s kojima ljekovite tvari djeluju, poput trijodtironin hidroklorida, koji su analogi prirodnog hormona T3. Kao rezultat ove interakcije, sinteza ATP se povećava.
Nuklearni receptori
T3 prodire u jezgro i tamo stupa u interakciju sa receptorima ove vrste. Kao rezultat toga, rad genoma se mijenja i sintetiziraju se novi proteini.
Konačni farmakološki efekti (prema Veršininu)
Uprkos obilju lijekova, promjene koje uzrokuju u tijelu su iste vrste (sl. 15). Učinak bilo kojeg lijeka na organe može se smanjiti na pet glavnih farmakoloških učinaka (prema N. V. Vershinin):
Umirujuće - smanjenje na normalno pojačano funkcionisanje organa (upotreba sedativa).
Ugnjetavanja - pad ispod norme funkcije tijela (upotreba lijekova za anesteziju)
Paraliza - prestanak smanjene funkcije organa (respiratorna depresija u slučaju predoziranja opojnih analgetika).
Toniranje - jačanje smanjene funkcije na normalno (upotreba β -adrenomimetika).
Uzbuđenje - Povećanje funkcije organa iznad norme (uporaba diuretika u slučaju trovanja, lijekovi za iskašljavanje).

Sl. 15. Konačni farmakološki efekti
Vrste djelovanja lijekova
Glavna stvar je sekundarna.
Reverzibilni, nepovratni.
U rijetkim slučajevima terapeutski cilj iziskuje nepovratna isključivanje strukture iz svoje funkcije. To se odnosi, na primjer, na većinu antimikrobnih, antitumorskih agenasa koji su u stanju formirati snažne (kovalentne) veze s elementima DNK spiralnih ćelija („umrežavanje“) ili bakterijskim enzimima, uslijed čega ćelije gube sposobnost reprodukcije.
Direktno, indirektno (indirektno).
Poseban je slučaj indirektne akcije refleks radnja. Na primjer, vazodilatacija i poboljšanje trofičnog tkiva kao posljedica iritacije krajeva senzornih živaca kože.
Selektivno, neselektivno.
Lokalna, resorptivna.
Resorptive (sistemsko) delovanje razvija se nakon apsorpcije lijeka u krv. Ogromna većina lijekova ima ovaj efekat.
Čimbenici koji utječu na farmakokinetiku
i farmakodinamika
I. Vanjski faktori
Okoliš:
sezona (ljeti nakon uzimanja tetraciklina moguća je opeklina od sunca (lijek povećava osjetljivost kože na ultraljubičastu svjetlost));
temperatura okoline (po vrućem vremenu očituje se jači efekat lijekova koji pritiskuju centralni nervni sistem);
parcijalni pritisak O2 (uzrokovan epinefrinom (adrenalinska) tahikardija bolje se podnosi pri visokom parcijalnom tlaku O2).
Svojstva lijekova:
rastvorljivost (rastvorljivi Ba2CO3 je toksičan, a netopljivi Ba2S04 nije toksičan);
radikali (supstitucija CH3 - grupe na atomu dušika u molekuli morfija sa -CH2-CH \u003d CH2 - skupinom (nalokson) dovodi do pojave svojstava antagonističkih morfijumu u supstanci);
izomerizam (levorotatorni izomer propranolola (anaprilin) \u200b\u200bje 40-60 puta jači od dekstrorotatornog);
polaritet (polarni molekuli su obično slabo topljivi u lipidnim membranama, stoga se slabo apsorbiraju i slabo prodiru kroz stanične membrane).
Unos lijekova u organizam:
oblik doziranja (lijek u tečni oblik ima veću bioraspoloživost, efekat počinje brže i izraženiji je);
put administracije (sa intravenska primena Lijek djeluje brže i jače nego kad se uzima oralno, trajanje njegovog djelovanja je kraće);
doza (s povećanjem doze (do određene granice), jačina djelovanja lijekova se povećava);
kombinacija lijekova (moguće slabljenje, sumiranje, pojačavanje efekata kombiniranih lijekova, a ponekad jačanje nekih i slabljenje drugih učinaka lijekova);
trajanje davanja (sa dugotrajna upotreba barbiturati se njihovo djelovanje smanjuje, jer se ubrzava njihov metabolizam u jetri).
II. Unutrašnji faktori
Biološki objekt:
karakteristike vrsta (zečevi lako podnose smrtonosne doze atropina za ljude);
etničke karakteristike (kod ljudi mongoloidne rase manjak alkohol-dehidrogenaze je češći i, rezultat toga, njihova osjetljivost na etanol je veća nego kod Europljana);
dob (u novorođenčadi i male djece sposobnost jetre da metabolizira lijekove je niska, bubrezi ne funkcioniraju u potpunosti, a sadržaj tekućine u tijelu je veći nego kod odraslih; u starijih ljudi metabolizam lijekova je smanjen, a funkcija bubrega opada s godinama);
spol (uklanjanje mnogih lijekova kod muškaraca je brže nego kod žena jer se vjeruje da muški spolni hormoni aktiviraju jetrene enzime);
genotip (kod osoba s oštećenom (neaktivnom) pseudoholinesinesom, zaustavljanje disanja nakon primjene mišićno relaksirajućih suksametonija (ditilin) \u200b\u200bne traje 2-3 minute, kao kod većine bolesnika, već 2-3 sata ili više zbog oštrog smanjenja brzine razaranja suksamethonijuma (idiosinkrazija) );
fenotip (kod pretilih ljudi, lipofilni lijekovi (fenobarbital itd.) kumuliraju se u većoj mjeri nego u tankih).
Fiziologija tijela:
prehrana (hrana može imati značajan utjecaj na farmakokinetiku lijeka; najčešće usporava i smanjuje apsorpciju lijekova);
trudnoća (mnogi lijekovi koji prelaze placentarnu barijeru mogu utjecati na razvoj fetusa);
dojenje (antibiotici koje koristi majka i dijete primaju mlijeko, što ga može na primjer uzrokovati disbiozom);
stres (uzbuđeni ljudi su najosjetljiviji na supstance podsticajnog djelovanja);
cirkadijanski ritmi (sulfonamidi se sporije izlučuju bubrezima noću kada pH urina opada).
Patološka stanja:
bolesti (kod bolesnika sa cirozom jetre lijekovi kao što su barbiturati i klorpromazin mogu izazvati neuobičajeno dugo djelovanje);
alkoholizam (etilni alkohol pojačava učinak na anksiolitike centralnog nervnog sistema, antikonvulzive i antidepresive);
pušenje (biotransformacija mnogih lijekova u tijelu pušača je brža (smanjena efikasnost kombiniranih oralnih kontraceptiva kod žena pušača)).
Doza je količina lijekova unesenih u tijelo i uzrokuje ih farmakološki učinak.
Obično se doze izražavaju u jedinicama mase, zapremine (gram, mililitri). U jedinicama djelovanja (ED) doziraju se određeni lijekovi biološkog porijekla s isprekidanim djelovanjem (hormoni, antibiotici, heparin, itd.).
Klasifikacija doze
Do trenutka administracije:
jednokratno;
dnevnica;
naravno.
Na silu:
medicinski ili terapeutski (minimalan, srednji, viši);
otrovno (minimalno, srednje, smrtonosno).
Doza zasićenja je doza kojom je moguće stvoriti potrebne koncentracije lijekova u tkivima (na primjer, u liječenju srčanih glikozida).
Doza održavanja - doza kojom možete održavati koncentraciju lijekova u plazmi i tkivu, nadoknađujući gubitak lijeka tijekom eliminacije (na primjer, digitalizaciju).
Šokna doza je doza koja vam omogućava da stvorite optimalnu koncentraciju lijeka koja je potrebna za njegovu konkurenciju s određenim endogenim supstratom (na primjer, udarna doza sulfanilamida potrebna za natjecanje s para-aminobenzojevom kiselinom (PABA) za mjesto u strukturi molekule folne kiseline u fazi njegove sinteze). , lijekovi se propisuju u srednjim terapijskim dozama, koji kod većine bolesnika imaju optimalni terapeutski učinak bez toksičnih efekata. Tipično je takva doza 1/2 ili 1/3 maksimalne terapijske.
Naziva se raspon doza između minimalne terapijske i minimalne toksičnosti širina terapijskog efekta(SHTD) . Što je veća širina terapijskog djelovanja, sigurniji su lijekovi (slika 16).
SHTD

Sl. 16. Širina terapijskog djelovanja
1 - minimalna terapijska doza, 2 - prosječna terapijska doza,
3 - maksimalna terapijska doza, 4 - minimalna toksična doza
Terapijski indeks (TI) je odnos toksične doze sa prosječnom terapijskom dozom određenom formulom:
gdje je TD 50 doza koja uzrokuje trovanje kod 50% pacijenata;
ED 50 - prosječna terapijska doza, tj. Doza koja izaziva terapeutski učinak kod 50% pacijenata.
Što je više TI, sigurniji su lijekovi. Da bi lijek bio siguran, njegova TI bi trebala biti veća od 3.
U djece i starijih osoba doziranje lijekova ima svoje karakteristike, koje su povezane s fiziološkim razlikama tih skupina.
Značajke dječijeg tijela:
neuspjeh metabolizirajuće funkcije jetre (zbog toga su lijekovi toksičniji);
koža i sluznice obilno vaskulariziraju (zbog toga se lijekovi apsorbiraju bolje nego kod odraslih);
BBB je propusniji (to stvara relativno veliku koncentraciju lijekova u mozgu);
visok sadržaj vode u tkivima;
manje masnog tkiva
Lijekovi se u manjoj mjeri vežu na proteine \u200b\u200bplazme (to može dovesti do toksičnih reakcija, jer se povećava slobodna (aktivna) frakcija);
izlučna funkcija bubrega je smanjena (to dovodi do dužeg djelovanja lijekova).
S obzirom na prisutnost dovoljno značajnih razlika u farmakodinamikama i farmakokinetikama lijekova kod djece i odraslih, jednostavno izračunavanje proporcionalne dozi doze za odrasle osobe neprihvatljivo je prilikom izračuna doze lijeka za dijete, jer može dovesti do nepredvidivih posljedica.
Doza se kod djece izračunava na 1 kilogram tjelesne težine, po godini života, po površini tijela. Na primjer:
Doza djeteta \u003d Doza za odrasle × težina djeteta / 70 kg
Fiziološke karakteristike senilnih ljudi:
kršenje metabolizma lijekova u jetri kao rezultat atrofičnih i distrofičnih promjena;
nizak sadržaj vode u tijelu i veći sadržaj masnog tkiva;
smanjenje proteina u plazmi (to dovodi do povećanja slobodne frakcije lijekova);
progresivno smanjenje funkcije izlučivanja bubrega;
Centralni nervni i kardiovaskularni sistem su osjetljiviji na djelovanje lijekova.
Nuspojave (neželjeni) efekti lijekova
Neželjeni efekti znače bilo kakve reakcije na lijekove štetne za tijelo koje nastaju kada se koriste za liječenje, dijagnosticiranje ili sprečavanje bolesti. Nuspojave se javljaju od 1 do 30% slučajeva upotrebe lijekova u kliničkoj praksi. Postoje lijekovi, čija upotreba vrlo često izaziva neželjene reakcije. Uključuju antibiotike, glukokortikoide, nesteroidne protuupalne lijekove, antiepileptike, antitumorske i druge lijekove. Neželjeni efekti lijekova mogu se podijeliti u nekoliko grupa.
Neželjeni efekti povezani s terapijskom koncentracijom lijekova u krvi:
alergijske reakcije;
pseudo-alergijske reakcije;
genetski određene reakcije (idiosinkrazija);
sindrom mentalne i fizičke zavisnosti.
Pseudoalergijske reakcije (anafilaktoidni) karakterizira direktan učinak lijeka na mastociti, bez sinteze IgE. Za razliku od alergijske reakcije, ovise o dozi. Pacijent u pravilu nema opterećenu alergijsku anamnezu. Pseudoalergijske reakcije mogu biti uzrokovane ampicilinom, radioaktivnim supstancama koje sadrže jod, lokalnim anesteticima itd.
Idiosinkrazija - genetski određena netolerancija na lijekove. Genetske reakcije se ne mogu predvidjeti. Povezani su s nasljednim oštećenjima enzimskih sustava ili sa nasljednim metaboličkim bolestima.
Na primjer, nedostatak pseudoholinesinesa prati i suzbijanje razaranja ditilina (što dovodi do produljenog opuštanja mišića). Manjak glukoza-6-fosfat dehidrogenaze praćen je smanjenjem aktivnosti niza reducirajućih enzima (glutation-reduktaza itd.). Ulazak oksidirajućih lijekova (sulfonamida, nitrofurana, antimalarijskih lijekova - kinina, chingamina, primakvina itd.) U organizam dovodi do stvaranja hemolize crvenih krvnih zrnaca i stvaranja methemoglobina. Nasljedna abnormalnost sarkoplazmatskog retikuluma popraćena je kršenjem fiksacije kalcija na aktomiozin i općenito kiselinsko bazno stanje kada se koriste halotan, barbiturati i drugi lijekovi, koji se uglavnom primjenjuju u anestetskoj praksi. Pojavljuje se maligna hipertermija, koja može dovesti do smrti pacijenta.
Mentalna i fizička ovisnost (ovisnost). Droga je uzrokovana drogama kao što su opijum i njegovi alkaloidi (morfij, kodein, heroin), promedol, kokain, amfetamin, etanol, neki barbiturati, itd.
Euforija je osnovni uzrok nekontrolirane upotrebe ili razvoja droga mentalna ovisnost. Euforiju karakteriše nestanak ili prigušenost neugodnih emocija, osjećaja straha, anksioznosti. Želja za ponovnim iskustvom euforije uzrok je psihičke ovisnosti.
Fizička ovisnost povezan s pojavom sindroma povlačenja (sindroma povlačenja ili deprivacije): zimica, hipertermija, oštra kolebanja krvnog tlaka, bolovi u mišićima i zglobovima, povraćanje, anksioznost, neprijateljstvo, nesanica. Štoviše, broj i intenzitet simptoma povezani su sa stupnjem fizičke ovisnosti.
Možda je mehanizam za razvoj fizičke ovisnosti nastao zbog činjenice da opojni analgetici, aktivirajući opijatne receptore po principu povratne sprege, inhibiraju oslobađanje endogenih opijatnih peptida, postepeno zamjenjujući njihovu aktivnost. Kao rezultat ukidanja analgetika dolazi do neuspjeha prethodno unesenog analgetskog i endogenog peptida. Razvija se sindrom otkazivanja.
Neželjeni efekti povezani s toksičnom koncentracijom lijekova u krvi (uglavnom karakteristični za lijekove uske širine terapijskog učinka):
nefrotoksičnost (aminoglikozidi);
ototoksičnost (produljena upotreba aminoglikozida može dovesti do gubitka sluha, do razvoja nepovratne gluhoće);
hematotoksičnost (antibiotik levomicetin ima depresivan učinak na hematopoetski sistem);
neurotoksičnost (antimikrobni lijek iz skupine fluorokinolona lomefloksacin uzrokuje nesanicu, glavobolju);
gastrotoksičnost (salicilati uz produženu upotrebu mogu dovesti do peptičke čirne bolesti);
hepatotoksičnost (antibiotici-linkozamidi uzrokuju žuticu s povećanjem nivoa jetrenih transaminaza u plazmi, što ukazuje na oštećenje jetrenog tkiva);
kardiotoksičnost (antitumorski antibiotici).
Neželjeni efekti koji ne ovise o koncentraciji lijekova u krvi:
disbioza;
superinfekcija;
hipovitaminoza;
imunodeficijencija.
Superinfekcija razvija se primjenom visoko aktivnih antibiotika i drugih antimikrobnih sredstava. Njegova pojava nastaje činjenicom da antibiotici suzbijaju mikrofloru koja je osjetljiva na njih, a mikroflora rezistentna na antibiotike (apatogena ili uvjetno patogena) počinje se intenzivno razmnožavati i pod određenim uvjetima može uzrokovati novu bolest - superinfekciju.
Negativan učinak lijekova na embrion i plod
Poseban značaj u modernim uvjetima predstavlja problem učinka lijekova u terapijskim i toksičnim koncentracijama na ljudski plod. Propisivanje lijekova trudnicama zahtijeva veliku opreznost jer lijekovi mogu prodrijeti kroz placentnu barijeru, pojaviti se u krvi fetusa i imati negativan utjecaj na njega.
Takvi uticaji uključuju:
Embriotoksični efekat.
Teratogeni efekat.
Fetotoksični efekat.
Teratogeni efekat nastaje uglavnom kao rezultat uzimanja lijekova od 3. do 10. sedmice trudnoće (I tromjesečje). U ovom periodu dolazi do histo- i organogeneze. Teratogeni učinak predstavlja kršenje diferencijacije fetalnog tkiva zbog čega se može roditi dijete s malformacijama ekstremiteta, glave i unutrašnjih organa. Ovisno o karakteristikama oštećenja, dijete može biti neživo i umrijeti ubrzo nakon rođenja ili može ostati onemogućeno cijeli život.
Primjer teratogenih efekata je nerazvijenost ekstremiteta (focomelia) uslijed upotrebe talidomida. Upotreba androgena tokom trudnoće dovodi do maskulinizacije ženskog ploda. Upotreba velikih doza tetraciklina praćena je nakupljanjem lijeka u kostima fetusa i kršenjem njihovog razvoja.
Fetotoksični efekat - To je rezultat reakcije zrelog ili već zrelog ploda na lijekove, što može uzrokovati promjenu vitalnih funkcija. Na primjer, indometacin i neki drugi NSAID uzrokuju zatvaranje ili sužavanje arteriosusa duktusa. Aminoglikozidni antibiotici izazivaju ototoksičnost. Antikoagulansi mogu izazvati krvarenje u novorođenčadi. Upotreba antitiroidnih lijekova prati razvoj guša. Te toksične reakcije mogu uzrokovati tešku patologiju ploda i novorođenčadi i povećati perinatalnu smrtnost kod djece.
Pojave koje se razvijaju kod opetovanog unošenja droga
U kliničkim uvjetima nema mnogo slučajeva kada se lijekovi koriste jednom. Ovo se susreće pri prikazivanju hitna pomoć. Najčešće se lijekovi ponovo propisuju. U tom slučaju mogu se primijetiti sljedeće vrste reakcija.
Kumulacija je nagomilavanje neke tvari u tijelu ( kumulacija materijala) ili njegovi efekti ( funkcionalna kumulacija) Verovatnoća materijala kumulacija je veća, sporije se lijek inaktivira u tijelu i što se jače veže na biosubstrat u tkivima. Kumulacija je uvijek opasna zbog brzog porasta broja i težine različitih komplikacija i toksičnih reakcija. Barbiturati, srčani glikozidi itd. Najviše su skloni kumulaciji. Funkcionalnom kumulacijom porast terapeutskog efekta, koji postaje intoksikacija, nadilazi fizičko nakupljanje lijeka u vremenu (možda i nije). Dakle, s alkoholizmom, povećane promjene u funkciji središnjeg živčanog sustava mogu dovesti do razvoja delirium tremensa. U tom se slučaju tvar (etilni alkohol) brzo oksidira i ne zadržava se u tkivima. Ukratko su prikazani samo njegovi neurotropni efekti.
Tolerancija (ovisnost) - ovo je postepeno slabljenje (do potpunog gubitka) terapijsko djelovanje lijek s produljenom uporabom. Tolerancija može imati različite uzroke i obično se razvija paralelno sa svim predstavnicima ove farmakološke grupe. Može biti posljedica sljedećih reakcija:
povećanje ili smanjenje broja receptora;
poboljšavanje funkcioniranja homeostatskih regulatornih mehanizama koji nadoknađuju pomak uzrokovan lijekom (na primjer, porast vazodilatatora krvnih žila snizan krvnim tlakom kao posljedica zadržavanja tekućine, povećanog rada srca, uključivanja drugih mehanizama za povećanje vaskularnog tonusa);
ubrzana inaktivacija lijeka kao rezultat indukcije njega ili drugog hemijskog faktora mikrosomalnih enzima.
Pokušaji prevladavanja ovisnosti jednostavnim povećanjem doze istog lijeka su neučinkoviti i preplavljuju se komplikacijama liječenja lijekovima.
Tahifilaksa - opcija brze tolerancije, kada se ovisnost brzo pojavi, u roku od nekoliko sati ili dana. Na primjer, tolerancija na efedrin razvija se već prilikom druge primjene lijeka.
Sindrom povlačenja nastaje kada se lijek naglo prekine u sljedećim slučajevima:
nakon prestanka uobičajene patogenetske farmakoterapije (na primjer, pogoršanje IHD - nitrati, β-blokatori);
s ukidanjem lijekova koji mogu izazvati simptome povlačenja (opojni analgetici, sredstva za smirenje, psihostimulansi);
nakon završetka terapije, lijekovi čiji se analozi proizvode u tijelu (glukokortikoidi, hormoni štitnjače); uzimanje ovih lijekova može inhibirati proizvodnju endogenih hormona što je praćeno ovisnošću o lijekovima.
Ricochet sindrom (pojava odvikavanja) - je vrsta sindroma povlačenja. Suština fenomena je dezinhibicija regulatornog postupka ili zasebna reakcija, prethodno suzbijena ljekovitom supstancom. Kao rezultat, dolazi do svojevrsne superkompenzacije procesa s oštrim pogoršanjem bolesti u usporedbi s čak razinom prije liječenja.
Najbolji način za prevenciju je i postepeno povlačenje lijeka.
Ovisnost o drogama (vidi temu „ Nuspojave ljekovite tvari ").
Interakcije lijekova
Istovremena primjena nekoliko lijekovi koristi se kada postoji više problema istovremeno. Međutim, u liječenju jedne bolesti često se propisuje nekoliko lijekova za povećanje terapeutskog efekta i (ili) za smanjenje nuspojave.
Na primjer, za povećanje analgetskog efekta fentanila, kombinira se s droperidolom.
Da bi se smanjila hipokalemija izazvana hidrohlorotiazidom, propisan je panangin (sadrži kalijev asparaginat).
Da bi se povećao terapeutski efekat i smanjili nuspojave, levodopa se kombinira s karbidopom.
Naziva se vrsta terapije, kada se veliki broj lijekova naučno nerazumno koristi za liječenje bolesti polifarmacija.
Ako jedan lijek uđe u tijelo, tada se o njegovoj sudbini (farmakokinetika) i njegovim učincima (farmakodinamika) može zaključiti u oko 90-95% slučajeva; ako dva lijeka - samo u 50% slučajeva, a ako u tijelo uđu više od tri - do 10%. Ovome treba dodati da se povećava i rizik od nuspojava pri kombiniranoj upotrebi lijekova: za 5% ako se koristi do 5 lijekova, za 20% - do 8 lijekova i za 40% - do 15 lijekova.
Interakcija lijekova može biti nepoželjna, štetna. Moguće slabljenje terapeutskih svojstava lijekova, povećanje njihovih nuspojava ili pojava toksičnih efekata. U takvim slučajevima razgovaraju inkompatibilnosti lijekova.
Na primjer, penicilini imaju baktericidni učinak na rastuće mikroorganizme, a tetraciklini narušavaju sintezu proteina i inhibiraju rast bakterija. S tim u vezi, tetraciklini slabe učinak penicilina.
Interakcije lijekova mogu biti:
Farmaceutski
Farmakološki.
Na primjer, nemoguće je kombinirati otopine aminofilina s otopinama pipolfena ili askorbinske kiseline u istoj špricu, jer u kiselom mediju dolazi do taloženja aktivnog principa aminofilina - teufilina.
Farmakološki interakcija je podijeljena na:
farmakokinetika;
farmakodinamička.
Farmakokinetička interakcija lijekova može se pojaviti na različitim nivoima:
Usisavanje.
utjecaj lijekova na pH u gastrointestinalnom traktu - primjena antacida dovodi do povećanja pH u želucu, uslijed čega se smanjuje apsorpcija lijekova slabe kiseline, a samim tim i učinak tih tvari.
učinak lijekova na gastrointestinalnu pokretljivost - M-antikolinergici i narkotički analgetici usporavaju pokretljivost gastrointestinalnog trakta, što uzrokuje duži kontakt lijeka sa sluznicom i može dovesti do iritacije (na primjer, kada koristite aspirin).
Distribucija.
Metabolizam.
Izlučivanje.
Farmakodinamička interakcija - ovo je interakcija lijekova, kada jedan od njih mijenja proces proizvodnje i provođenja farmakoloških učinaka drugog. Farmakodinamička interakcija može se dogoditi na dva načina:
Sinergizam.
Antagonizam.
sažeto - jednostavan dodavanje učinaka dva ili više lijekova (na primjer, istodobna primjena dva diuretika etakrilne kiseline i furosemida dovodi do zbrajanja njihovog diuretskog djelovanja), ova vrsta interakcije izražena je formulom 1 + 1 \u003d 2;
potencirana - vrsta interakcije u kojoj je farmakološki učinak kombinacije lijekova veći od matematičkog zbroja farmakoloških učinaka svakog od posebno propisanih lijekova (na primjer, antipsihotičkim antipsihoticima droperidol značajno pojačava analgetski učinak uzrokovan opioidnim analgetičkim fentanilom); ova vrsta interakcije lijekova izražena je formulom 1 + 1 \u003d 3.
Antagonizam - ovo je suprotan učinak lijekova koji se koriste istovremeno, kada je njihov ukupni farmakološki učinak na organizam manji od zbroja učinaka pojedinih lijekova. Sledeće vrste antagonizma su:
fizička, zasnovana na fizičkoj interakciji tvari (na primjer, aktivni ugljen adsorbira toksine);
hemijska, koja se temelji na kemijskoj interakciji lijekova (na primjer, s povećanom kiselošću, neutralizacijom klorovodične kiseline u želucu antacidnim lijekovima);
primjećuje se kompetitivni antagonizam kada su tvari slične strukture i natječu se za isti receptor (na primjer, M-holin blokator atropin i M-holinomimetski pilokarpin natječu se za vezanje za M-holinergičke receptore);
uočava se nekonkurentski antagonizam sa suprotnim učincima tvari pri djelovanju na različite receptore; nekonkurentski antagonizam može biti funkcionalnikada tvari djeluju na različite receptore istog organa (na primjer, pobudni učinak adrenalina i inhibitorni učinak acetilholina na rad srca) i fiziološkakada tvari djeluju na različite receptore različitih organa (npr. aldosteron povećava krvni tlak djelujući na bubrege, a klonidin snižava krvni tlak djelujući na središnji živčani sustav).
Farmakologija, njeni odsjeci, zadaci i mjesto među medicinskim, biološkim i specijaliziranim disciplinama. Postignuća domaće farmakologije.
Farmakologija - biomedicinska nauka o lekovitim supstancama i njihovom uticaju na organizam; u širem smislu, nauka o fiziološki aktivnim tvarima uopšte i njihovom uticaju na biološke sisteme.
Odjeljci: Opći i privatni. Općenito: 1) principi proizvodnje lijekova, njihov sastav i svojstva 2) metabolizam - farmakokinetika i farmakodinamika, 3) toksikologija, 4) farmakogenetika 5) farmakogenomija.
Definicija i struktura recepta. Obrasci na recept Opća pravila propisivanja. Značajke propisivanja otrovnih, opojnih, moćnih lijekova.
Recept- Ovo je apel ljekara farmaceutu oko puštanja lijekova pacijentu, ukazuje na oblik doze, dozu i način upotrebe. To je medicinski, pravni i novčani dokument u slučaju besplatnog ili preferencijalnog izdavanja lijekova. Dozaizraženo u jedinicama mase ili volumena decimalnog sustava i označeno je arapskim brojevima. Broj cijelih grama odvojen je zarezom (1,0). Češće se koriste: 0,1 - jedan decigram; 0,01 - jedan centigram; 1.001 jedan miligram. Kapi koje čine lijek označene su rimskim brojem, ispred kojeg je napisano gtts. Biološke jedinice djelovanja u receptu tako pokazuju 500.000 jedinica. Tečne supstance u receptima su naznačene u ml (0,1 ml). Recept je ovjeren potpisom i ličnim pečatom. Recept mora navesti: pacijentovu starost, datum propisivanja, prezime i inicijale pacijenta; prezime i inicijali liječnika, nalog za plaćanje lijeka. Štaviše, preferencijalni recepti se ispisuju na posebnim obrascima koji imaju pečat i pečat. Na posebnim oblicima drugog uzorka propisuju se i lijekovi s liste opojnih supstanci, tablete za spavanje, anorexigenic lijekovi. Štoviše, liječnik propisuje recept, stavlja svoj potpis i ovjerava ga osobnim pečatom. Uz to, potpisuje ga glavni ljekar ili njegov zamjenik, na receptu se nalazi okrugli pečat i medicinski pečat
institucije. Isti postupak propisivanja definiran je i za anaboličke steroide, kao i za fenobarbital, ciklodol, efedrin hidroklorid, klonidin ( kapi za oči, ampule), sunoref masti. Na ostalim oblicima recepta predviđaju se antipsihotici, sredstva za smirenje, antidepresivi, lijekovi koji sadrže etilni alkohol i dr. Za ambulantne bolesnike zabranjeno je propisivanje etera za anesteziju, kloretil, fentanil, sombrevin, ketamin. Recept počinje riječju Recept (Rp. - u skraćenom obliku), što znači "uzeti", tada su navedena imena i količine ispisanih
ljekovite tvari u genitivu. Prvo se zove primarna, a zatim pomoćna. Zatim je naveden potreban oblik doziranja. Na primjer Misce ut fiat pulvis(M. f. pulvis) - "miješati da se napravi prah." Za dozirano napisati: " Da priče su doze numerisane10 "-" izdajte takve doze s brojem 10 ". Na kraju recepta nakon riječi Signa(S) - "odrediti" na ruskom (ili nacionalnom) jeziku ukazuju na način upotrebe lijeka.
Opšta farmakologija, njeni odsjeci. Primjeri zajednički mehanizmi efekti lijekova. Koncept medicine i otrova.
1) principi proizvodnje lijekova, njihov sastav i svojstva 2) metabolizam - farmakokinetika (doktrina apsorpcije, raspodjele i biotransformacije istih u tijelu) i farmakodinamika (doktrina djelovanja lijekova na organizam) 3) toksikologija, 4) farmakogenetika (medicinski dio genetike i farmakologije, proučavajući prirodu reakcija tijela na lijekovi ovisno o nasljednim faktorima). 5) farmakogenomija (grana farmaceutskih proizvoda i farmakologije koja proučava učinak genetske varijacije svake osobe na njegov odgovor na lijek)
Kada koristi lijekove u tijelu, potonji mogu djelovati na specifične receptore, enzime, ćelijske membrane ili direktno komunicirati sa staničnim supstancama. Učinak na specifične receptore zasniva se prvenstveno na činjenici da su makromolekularne strukture selektivno osjetljive na određena hemijska jedinjenja. Interakcija hemijskih tvari s receptorom popraćena je fiziološkim, biohemijskim promjenama u tijelu, koje na kraju određuju klinički učinak. Lijekovi - farmakološka sredstva (tvari ili smjese tvari) koja su prošla klinička ispitivanja i odobrena su za uporabu za prevenciju, dijagnostiku i liječenje bolesti od strane ovlaštenog tijela zemlje na propisan način, dobivena iz krvi, krvne plazme, kao i iz organa, ljudskog ili životinjskog tkiva, biljke, minerali, sintezom ili upotrebom biotehnologije. Dakle, lijekovi uključuju tvari biljnog, životinjskog ili sintetskog podrijetla koje imaju farmakološko djelovanje i namijenjene su proizvodnji i proizvodnji dozni oblici. Otrov - tvar koja u dozama, čak i malim u odnosu na tjelesnu težinu, dovodi do poremećaja u organizmu: trovanja, intoksikacija, bolesti i patološka stanja.
Farmakodinamika
Proučava se mehanizam djelovanja lijekova, kao i njihovi biohemijski i fiziološki učinci. Njeni zadaci uključuju opis kemijskih i fizičkih interakcija između lijeka i ciljane ćelije, kao i puni spektar i ozbiljnost njegovih farmakoloških učinaka. Poznavanje farmakodinamičkih obrazaca omogućava vam odabir pravih lijekova. Farmakodinamičke studije pružaju dublje razumijevanje regulacije biokemijskih i fizioloških procesa u tijelu (Katzung B.G., 1998; Lawrence D.R. et al., 2002).
Djelovanje većine lijekova posreduje njihovim vezanjem na makromolekule u tijelu. Promjena funkcionalnog stanja ovih makromolekula, zauzvrat, pokreće lanac biohemijskih i fizioloških reakcija koje se pretvaraju u farmakološki učinak. Makromolekule s kojima kemikalije stupaju u interakciju nazivaju se receptori. Dakle, sve funkcionalno aktivne makromolekule mogu poslužiti kao receptori za lijekove. Iz ove izjave proizlazi nekoliko važnih posljedica. Prvo, uz pomoć lijekova možete promijeniti brzinu bilo kojeg fiziološkog procesa u tijelu. Drugo, lijekovi mijenjaju samo prirodne fiziološke funkcije ćelije, ne dajući joj nova svojstva.
Receptori
Većina receptora su proteini. Riječ je o receptorima hormona, faktorima rasta, posrednicima, proteinima koji su uključeni u najvažnije metaboličke i regulatorne reakcije (dihidrofolat reduktaza, acetilholinesteraza), transportnih proteina (Na +, K + -ATPase), strukturnih proteina (tubulin). Stanične ćelije različitog hemijskog karaktera, kao što su nukleinske kiseline, sa kojima antitumorska sredstva međusobno djeluju, takođe mogu djelovati kao receptori.
Receptori endogenih regulatornih faktora - hormona, posrednika itd., Imaju farmakološki značaj. Ovi receptori služe kao meta mnogih lijekova, obično djeluju selektivno zbog visoke specifičnosti receptora za endogene ligande. Lijekovi koji, nakon vezivanja na receptor, reproduciraju fiziološki učinak endogenog liganda, nazivaju se aganisti ili stimulansi. Lijekovi koji ne uzrokuju taj učinak, ali interferiraju s vezanjem endogenih liganda, nazivaju se antagonisti ili blokatori. Supstance čiji je efekat manje izražen od efekta agonista nazivaju se djelomičnim agonistima. Pripravci koji stabiliziraju receptor u neaktiviranoj konformaciji klasificirani su kao inverzni agonisti.
Strukturna i funkcionalna ovisnost
Hemijska struktura lijeka prilično čvrsto određuje njegov afinitet prema receptorima i unutrašnju aktivnost. Neznatna promjena u kemijskoj strukturi može značajno utjecati na farmakološka svojstva.
Na tome se u velikoj mjeri temelji sinteza novih lijekova. Budući da kemijska modifikacija ne mora nužno utjecati na sva farmakološka svojstva jednako, moguće je poboljšati učinkovitost i sigurnost lijeka, povećati njegovu selektivnost i poboljšati farmakokinetičke karakteristike. Na primjer, mnogi antagonisti hormona i posrednika koji se koriste u klinici sintetišu se hemijskim modifikacijama endogenih supstanci.
Bodovi za prijavu lijekova
Budući da učinak lijekova posreduju receptori, točka primjene lijeka određuje se ne samo karakteristikama njegove raspodjele, već i lokalizacijom receptora, a farmakološki učinci ovise o funkcionalnom značaju tih receptora. Farmakološki učinci lijekova čiji su receptori zajednički u mnogim organima i tkivima su različiti. Ako ovi receptori obavljaju funkciju koja je vitalna za stanice, nije samo teško koristiti lijek u terapeutske svrhe, već je i nesiguran. Bez obzira na to, takvi lijekovi mogu biti od velike kliničke važnosti. Dakle, srčani glikozidi, koji se široko koriste kod zatajenja srca, mijenjaju transport jona kroz staničnu membranu, o čemu ovisi vitalna aktivnost ćelije. Imaju uzak terapeutski raspon i vrlo su toksični. Drugi primjer su antitumorska sredstva. Ako su receptori s kojima lijek djeluje prisutni na samo nekoliko vrsta diferenciranih ćelija, njegov učinak je selektivniji. Ovi lijekovi mogu imati manje nuspojava, ali ipak, ti \u200b\u200blijekovi mogu biti toksični ako njihovi receptori obavljaju vitalnu funkciju. Neki biološki otrovi (botulinum toksin, itd.) Djeluju na sličan način. Pored toga, čak i ako je izravni farmakološki učinak selektivan, njegove posljedice mogu biti raznovrsnije.
Endogeni receptorski faktorski receptori
Izraz receptor odnosi se na bilo koju makromolekularnu komponentu stanice s kojom se lijek veže. Jedan od najvažnijih receptora za lijekove su ćelijski proteini, koji služe kao receptori za endogene regulatorne faktore - hormone, faktore rasta, posrednike. Vezivanjem na endogeni ligand, receptori prenose signal iz njega u ciljanu ćeliju.
Iz receptora signal stiže do ćelijskih ciljeva (efektorskih proteina) direktno ili posredstvom signalnih molekula - protein-pretvarača. Receptori, proteinski pretvarači i efektorski proteini tvore sistem receptora i efektora. Najbliži efektorski protein u lancu prijenosa signala često nije terminalni efektor (koji direktno utječe na stanične funkcije), već enzim ili transportni protein uključen u stvaranje, transport ili inaktivaciju drugog posrednika - iona ili malog molekula. Drugi posrednik, pak, prenosi informacije na različite unutarćelijske ciljeve, osiguravajući njihov istovremeno reagiranje na signal s jednog receptora.
Receptori, pretvaranje proteina i efektorski proteini ne prenose samo informacije. Oni koordiniraju i signale iz različitih liganda, s jedne strane, i svi ti signali s metaboličkim procesima u stanici, s druge.
Djelujući kao katalizatori, receptori pojačavaju biološki signal. Zbog ovog važnog svojstva služe kao odlične mete za lijekove. Međutim, pojačivači signala nisu samo receptori s enzimskom aktivnošću, već su svi poznati receptori. U stvari, kad se jedan molekul liganda veže na receptor konjugiran na ionski kanal, mnogi ioni prolaze kroz zadnji. Isto vrijedi i za receptore za steroidne hormone: jedna molekula hormona pokreće transkripciju mnogih kopija mRNA, na temelju kojih se sintetišu brojne proteinske molekule.
Ovisno o strukturi i mehanizmu djelovanja, receptore biološki aktivnih tvari dijele se u nekoliko klasa. Broj ovih časova je mali.
Enzimski receptori
Najveća grupa receptora s enzimatskom aktivnošću su membranski receptori sa vlastitom aktivnošću protein kinaze. Fosforiliraju različite efektorske proteine \u200b\u200bkoji se nalaze na unutrašnjoj strani ćelijske membrane. Kao rezultat toga, funkcija ovih proteina ili njihova interakcija sa drugim proteinima se menja.
Postoji još jedna klasa receptora sa aktivnošću proteinske kinaze - to su receptori konjugirani s protein kinazama. Nedostaje im intracelularni katalitički domen, ali prilikom interakcije sa agonistom, vežu se ili aktiviraju unutarćelijske proteinske kinaze na unutrašnjoj površini membrane. Riječ je o receptorima za neurotrofične faktore i receptorima koji prepoznaju antigene za T i B limfocite, a sastoje se od nekoliko podjedinica. Potonji takođe međusobno djeluju sa fosfotirozin fosfatima. Funkcija drugih receptora koji nemaju intracelularnu efektorsku domenu može biti posredovana nekim drugim efektorskim proteinima.
I drugi receptori sa vlastitim enzimatskim djelovanjem imaju sličnu strukturu. Tu spadaju, na primjer, receptori sa vlastitom aktivnošću fosfotirozin fosfataze: njihova izvanstanična domena slična je u slijedu aminokiselina kao adhezijski molekuli. Za mnoge receptore s vlastitom aktivnošću fosfotirozin fosfataze endogeni ligandi nisu poznati. Međutim, prema genetičkim i biohemijskim istraživanjima koja se vrše na različitim tipovima ćelija, enzimska aktivnost ovih receptora igra važnu ulogu. Intraćelijska domena atrijskih receptora natriuretskog hormona, ostali NUP-ovi, kao i gvaninilski receptori imaju vlastitu aktivnost gvanilat ciklaze i sintetizira cGMP, koji djeluje kao drugi posrednik. Možda postoje i drugi receptori sa vlastitom enzimskom aktivnošću.
Receptori vezani za jonski kanal
Receptori nekih medijatora direktno su povezani sa ionskim kanalima, pri interakciji s ligandom selektivno prolaze određene ione kroz staničnu membranu (hemosenzitivni kanali, jonotropni receptorski kanali, ionotropni receptori).
G-proteinski povezani receptori
Ovo je prilično velika klasa receptora koji stupaju u interakciju s efektorima preko G-proteina (proteina koji koriste zamjenu ganin-difosfata (GDF)) gvanin-trifosfatom (GTP). Tu spadaju receptori za mnoge biogene amine, molekule lipidnog signala (posebno eikosanoidi) i razne peptide bjelančevine i proteini. Enzimi (adenilat ciklaza, fosfolipaza C) i kalijum i kalcijevi membranski kanali djeluju kao efektori. Veliki broj i važna fiziološka uloga receptora spojenih sa G-proteinima čini ih izvrsnim. moji ciljevi za lijekove: otprilike polovina svih lijekova koje su propisali ljekari (osim antibiotika) djeluju na ove receptore.
Stanica može nositi do 20 receptora na svojoj površini od kojih svaki selektivno djeluje s jednom ili više vrsta G-proteina (razlikuju se u različitim vrstama α-podjedinica). Α-podjedinica je u mogućnosti komunicirati s jednim ili više efektorskih proteina, što vam omogućava koordiniranje signala iz receptora različitih liganda pomoću jednog G-proteina. S druge strane, jedan receptor može pokrenuti nekoliko mehanizama prenosa unutarćelijskog signala, aktivirajući nekoliko vrsta G-proteina i djelovati na različite efektorske proteine \u200b\u200bkroz istu α-podjedinicu. Tako složen sistem divergencije i konvergencije signala omogućuje fleksibilnu regulaciju staničnih funkcija (Ross, 1992).
Intraćelijski receptori
Receptori steroidnih i štitnih hormona, kalcitriol i retinoidi su topljivi unutarćelijski proteini koji se vežu za DNK koji reguliraju transkripciju određenih gena (Mangelsdorf et al., 1994). Ti receptori pripadaju super-porodici regulatora transkripcije osjetljivih na ligande. Funkcija faktora transkripcije reguliše se fosforilacijom, interakcijom sa ćelijskim proteinima, metabolitima i drugim regulatornim komponentama stanice.
Drugi posrednički sistemi
cAMP. Sekundarni posrednički sustavi također su uključeni u integraciju vanjskih signala. Iako ima mnogo više poznatih receptora i proteinskih signalnih molekula od drugih medijatora, potonji su uključeni u mnoge putove unutar ćelijskog prenosa signala. Najviše proučavani drugi posrednici uključuju cAMP, cGMP, Ca 2+, IF3 (inozitol trifosfat), DAG (diacilglicerol), NO. Ova grupa heterogenih spojeva konstantno raste. Drugi posrednici stupaju u interakciju direktno (mijenjajući međusobni metabolizam) ili indirektno (djelujući na iste unutarćelijske ciljeve). Funkcija drugog medijatora, kao i regulacija njihovog formiranja (ili oslobađanja), cijepanja i izlučivanja iz stanice, prikladno se razmatra na primjeru cAMP. Ovaj drugi medijator sintetizira se pod utjecajem adenilat citaze aktiviranjem mnogih receptora konjugiranih s G-proteinima. G s protein aktivira adenylat ciklazu, G i protein inhibira.
Postoji najmanje 10 izoformnih adenilata ciklotaza, specifičnih za tkivo, koji se razlikuju u mehanizmima regulacije aktivnosti.
U pravilu, cAMP aktivira protein kinaze A (cAMP-ovisne proteinske kinaze), malu grupu srodnih proteina. Ove proteinske kinaze, zauzvrat, fosforiliraju ne samo konačne unutarćelijske mete (enzimi, transportni proteini), već i druge proteinske kinaze i druge regulatorne proteine. Potonje uključuje, na primjer, faktore transkripcije. Oni su odgovorni za cAMP-posredovanu regulaciju transkripcije gena, pružajući odgođeni stanični odgovor na signal. Uz aktiviranje protein kinaza, cAMP djeluje izravno na kanale kationskih membrana, koji imaju važnu ulogu, posebno, u funkcioniranju neurona. Stoga signal iz cAMP-a uzrokuje lanac biohemijskih promjena u ciljanoj ćeliji.
Kalcijum Drugi dobro proučeni drugi posrednik je unutarćelijski Ca 2+. Ioni Ca 2+ ulaze u citoplazmu na različite načine: duž membranskih kanala (ovisno o G-proteinima, o naponu ovisnih, reguliranih K + ili Ca-Ca 2+), kao i preko kanala smještenih u posebnim područjima endoplazmatskog retikuluma i otvaranja pod djelovanjem AKO 3 i u skeletnim mišićima kao rezultat depolarizacije membrane. Uklanjanje kalcijuma iz citosolne plazme događa se na dva načina: apsorbuje ga endoplazmatski retikulum ili se izlučuje iz ćelije. Ca 2+ odašilje signale mnogo većem broju proteina nego cAMP - enzimi koji su uključeni u stanični metabolizam, protein kinaze, proteini koji vezuju kalcijum. Potonji interaktivno djeluju s ostalim završnim i intermedijarnim učincima.
Regulacija receptora
Receptori ne samo da kontroliraju fiziološke i biohemijske funkcije, već i služe kao objekti regulacije. Ova regulacija provodi se na nivou sinteze i razgradnje njihovih makromolekula, stvaranjem kovalentnih veza s drugim molekulama, interakcijom sa regulatornim proteinima i kretanjem receptora. Pretvorba proteina i efektorskih proteina je takođe podložna regulaciji. Regulatorni signali mogu poticati iz intracelularnih putova prenosa aktiviranih stimulacijom samog receptora (preko povratnog mehanizma), kao i iz drugih receptora (direktno ili indirektno).
Dugotrajna stimulacija receptora za lijekove obično dovodi do smanjenja reakcije na njega - pri istoj koncentraciji lijek izaziva manje izražen efekat. Taj fenomen, nazvan desenzibilizacija, vatrostalnost i ovisnost, igra važnu ulogu u kliničkoj praksi: na primjer, s produljenom primjenom β-adrenergičkih agonista za liječenje bolesnika s AD-om, ozbiljnost reakcije na ove lijekove opada.
Homološka desenzibilizacija odnosi se samo na stimulirane receptore i specifična je za ligand. S heterološkom desenzibilizacijom, smanjuje se ozbiljnost reakcije na druge ligande, čiji receptori djeluju istim putem prenosa signala unutar staničnog signala. U prvom slučaju negativne povratne informacije daju se učinkom na sam receptor (fosforilacija, proteoliza, smanjena sinteza), u drugom slučaju osim receptora može utjecati i na ostale proteine \u200b\u200bkoji su uključeni u prijenos unutarćelijskog signala.
Naprotiv, ako se receptori dugo ne stimulišu, njihova osjetljivost na agoniste se povećava (na primjer, kod dugotrajnog liječenja β-adrenoblokatorom propronololom povećava se osjetljivost β-adrenergičkih receptora na β-adrenostimulanse).
Poremećaji zbog oslabljene funkcije receptora
Pored individualnih razlika u osjetljivosti na lijekove, postoje i bolesti uzrokovane disfunkcijom određenih komponenti mehanizma prijenosa unutarćelijskog signala s receptora na efektor. S gubitkom funkcije visoko specijaliziranih receptora, fenotipske manifestacije bolesti mogu biti ograničene (na primjer, feminizacija testisa povezana s genetskom odsutnosti ili strukturnim oštećenjima androgenih receptora). Ako se krši univerzalniji mehanizam unutar prijenosa staničnog signala, simptomi bolesti su raznolikiji, kao što su, na primjer, miastenija gravis i neki oblici dijabetesa melitusa otpornog na inzulin, uzrokovani autoimunim disfunkcijama N-holinergičkih receptora i inzulinskih receptora. Defekti u bilo kojoj komponenti koja je uključena u prijenos signala s mnogih receptora dovode do više endokrinih poremećaja. Primjer je heterozigotni oblik nedostatka proteina G, koji aktivira adenilat ciklazu u svim stanicama (Spiegel i Weinstein, 1995). Homozigotni oblik nedostatka ovog proteina vjerovatno će rezultirati smrću.
Poremećaji u strukturi ili lokalizaciji receptora mogu se pokazati kao oslabljena ili pojačana reakcija na lijek, kao i drugi neželjeni efekti.
Mutacije koje kodiraju genske receptore mogu mijenjati i odgovor na jednokratnu upotrebu lijeka i efikasnost dugotrajnog liječenja. Na primjer, nedostatak β-adrenergičkih receptora odgovornih za opuštanje glatkih mišića bronha i reguliranje otpornosti dišnih puteva pogoršava smanjenje osjetljivosti ovih receptora na β-adrenostimulanse tijekom dugotrajnog liječenja pacijenata s AD. Kad se utvrde mutacije odgovorne za oslabljenu funkciju receptora i kloniraju odgovarajući geni, bit će moguće razviti metode liječenja takvih bolesti.
Klasifikacija receptora
Tradicionalno su receptori za lijekove identificirani i klasificirani na temelju učinaka i relativne aktivnosti selektivnih agonista (stimulansa) i antagonista (blokatora) koji djeluju na te receptore. Na primjer, efekti acetilkolina koji se reproduciraju pri interakciji s holinergičkim receptorima muskarin alkaloida i blokirani su atropinom nazivaju se muskarinima, a učinci koji se reproduciraju u interakciji s holinergičkim receptorima nikotina nazivaju se nikotinskim učincima. Receptori koji posreduju učinke muskarina i nikotina nazivaju se M i N holinergičkim receptorima. Iako takva klasifikacija obično ne odražava mehanizam djelovanja lijekova, prikladno je za sistematizaciju njihovih učinaka. Zapravo, tvrdnja da lijek stimulira receptore određene vrste, istodobno određuje spektar djelovanja ovog lijeka i tvari koje te efekte pojačavaju ili slabe. Međutim, valjanost takvih tvrdnji može se promijeniti identifikacijom novih tipova i podvrsta receptora, otkrivanjem dodatnih mehanizama djelovanja lijekova ili prethodno nepoznatih nuspojava.
Podtipovi receptora
Sa pojavom sve većeg broja vrlo selektivnih lijekova postalo je jasno da se prethodno poznate vrste receptora dijele na brojne podvrste. Metode molekularnog kloniranja postale su značajna pomoć u proučavanju novih podtipova receptora, a priprema rekombinantnih receptora olakšala je stvaranje lijekova koji selektivno djeluju na te receptore. Različite ali povezane podtipove receptora često (iako ne uvijek) komuniciraju s različitim agonistima i antagonistima. Receptori za koje nisu identificirani selektivni agonisti ili antagonisti, obično ne pripadaju jednoj podtipi, već izoformama istog receptora. Odvojeni podtipovi mogu se razlikovati u mehanizmima prijenosa unutarćelijskog signala. M1 i M3 holinergički receptori, na primjer, djeluju putem proteina q q, koji aktivira fosfolipazu C, neizravno uzrokujući oslobađanje Ca2+ iz unutarćelijskih depoa, i M2 i M4 holinergičke receptore preko proteina G i koji inhibira adilatnu ciklazu. Istodobno, podjela receptora na vrste i podvrste često se određuje ne mehanizmom djelovanja, već slučajnim odabirom ili se temelji na ustaljenim idejama. Dakle, α 1 -, α 2 - i β-adrenergički receptori se razlikuju u odgovoru na lijekove i u prenosu signala (aktiviraju proteine \u200b\u200bG i, G q i G s, respektivno), iako su α i β-adrenergički receptori različitih vrsta, i α1 - i α2-adrenoreceptori - za različite podvrste unutar iste vrste. Izoforme α 1 -adrenoreceptora α 1A, α 1B i α 1D malo se razlikuju u svojim biohemijskim svojstvima; isto je karakteristično za podtipove izoformraze β-adrenergičkih receptora (β 1, β 2 i β 3).
Razlike između receptorskih podtipova koriste se za stvaranje visoko selektivnih lijekova, na primjer, lijekovi koji imaju različito djelovanje na isto tkivo zbog vezanja na receptore podtipa koji se razlikuju u mehanizmima prijenosa unutarćelijskih signala. Osim toga, lijekovi mogu selektivno ciljati određene stanice ili tkiva koja eksprimiraju receptore podtipa. Što je veća selektivnost lijekova (u odnosu na određeno tkivo ili u odnosu na određeni učinak), povoljniji je omjer njegovih koristi i neželjenih efekata.
Korištenjem molekularno-genetskih metoda otkriveni su ne samo različiti izoformi receptora, već i geni koji kodiraju nove, do tada nepoznate receptore. Mnogi od tih receptora su već dodijeljeni jednoj ili drugoj poznatoj klasi, a njihova funkcija je proučavana pomoću odgovarajućih liganda. Međutim, ligandi još uvijek nisu pronađeni za neke receptore.
Otkrivanje mnogih izoforma istog receptora kodiranih različitim genima (posebno ako se izoformi ne razlikuju u mehanizmima intracelularnog prijenosa signala i interakciju s istim endogenim ligandima) omogućava da se ekspresija receptora u različitim stanicama neovisno regulira u skladu s potrebama tijela u različitim starosnim periodima.
Djelovanje lijekova bez receptora
Nisu svi lijekovi djeluju kroz makromolekularne strukture - receptore. Neki lijekovi djeluju u interakciji s malim molekulima ili ionima koji su normalno prisutni u tijelu ili u jednom ili drugom patološkom stanju. Dakle, antacidi neutraliziraju solnu kiselinu u stomaku. Mesna (lijek koji se bubrezima brzo izlučuje i neutralizira slobodne radikale) veže se na aktivne metabolite nekih lijekova protiv raka, smanjujući ozbiljnost neželjenih reakcija iz mokraćovoda. Broj biološki neaktivnih tvari (na primjer manitol) može se unijeti u količinama dovoljnim da se poveća osmolarnost bioloških tekućina i na taj način promijeni raspodjela izvanstanične i unutarćelijske tekućine. Uz pomoć ovih tvari moguće je povećati diurezu, povećati bcc, ukloniti moždani edem. Pored toga, upotrebljavaju se kao laksativi.
Neki lijekovi se mogu integrirati u komponente ćelije i mijenjati njihove funkcije zbog strukturnih sličnosti s tvarima koje čine ove komponente. Na primjer, analozi purina i pirimidina ubačeni su u nukleinske kiseline i koriste se kao antivirusna i antitumorska sredstva.
A.P. Viktorov "Klinička farmakologija"