Mehanizmi delovanja ljekovite tvari - ovo su načini na koje tvari izazivaju farmakološke učinke. Glavni mehanizmi djelovanja lijekova uključuju:
Fizički.
Mehanizam direktne hemijske interakcije.
Membrana (fizikalno-hemijska).
Enzimski (biohemijski).
Receptor.
Fizički mehanizam djelovanja. Djelovanje ljekovite tvari povezano je s njegovim fizičkim svojstvima. Na primjer, aktivni ugljen se posebno obrađuje, te stoga ima visoku površinsku aktivnost. To mu omogućava da apsorbuje plinove, alkaloide, toksine itd.
Direktna hemijska interakcija. Ovo je prilično rijedak mehanizam djelovanja lijekova, čija je suština u tome da lijekovi direktno stupaju u interakciju sa molekulima ili ionima u tijelu. Takav mehanizam djelovanja ima, na primjer, unitiolni lijek koji pripada grupi protuotrova. U slučaju trovanja tiolnim otrovima, uključujući soli teških metala, unitiol ulazi u izravnu hemijsku reakciju s njima, što rezultira stvaranjem netoksičnih kompleksa koji se izlučuju mokraćom. Tako djeluju i antacidi koji ulaze u izravnu kemijsku interakciju sa solnom kiselinom, snižavajući kiselost želučanog soka.
Membrana (fizikalno-hemijske) mehanizam. Povezana je s učinkom lijekova na jonske struje (Na +, K +, Cl - i druge), koje određuju transmembranski električni potencijal. Prema ovom mehanizmu javljaju se anestetici, antiaritmički lekovi, lokalni anestetici itd.
Enzymatic (biohemijska) mehanizam. Taj mehanizam određuje sposobnost nekih lekova da aktiviraju ili inhibirajuće na enzime. Arsenal lijekova s \u200b\u200btakvim mehanizmom djelovanja je vrlo širok. Na primjer, antiholinesterazni lijekovi, inhibitori monoamin oksidaze, blokatori protonske pumpe itd.
Receptorni mehanizam. U ljudskom telu postoje visoko specifične biološki aktivne supstance (posrednici) koji stupaju u interakciju sa receptorima i menjaju funkcije različitih organa ili tkiva u telu.
Receptori su makromolekularne strukture sa selektivnom osjetljivošću na određena hemijska jedinjenja. Uz interakciju lijekova s \u200b\u200breceptorima, događaju se biokemijske i fiziološke promjene u tijelu, praćene jednim ili drugim kliničkim učinkom.
Pozvani su posrednici i lijekovi koji aktiviraju receptore i uzrokuju biološki učinak agonisti. Ljekovite tvari koje se vezuju za receptore, ali ne uzrokuju njihovu aktivaciju i biološki učinak, smanjuju ili uklanjaju učinke agonista, nazivaju se antagonisti. Dodijelite također agonisti antagonista - tvari koje djeluju različito na podtipove istih receptora: stimulišu neke podvrste receptora, a blokiraju druge. Na primjer, narkotički analgetik nalbufin stimulira receptore opioidne kappe (dakle smanjuje osjetljivost na bol) i blokira opioidne mu receptore (dakle, manje je opasan u pogledu ovisnosti o lijekovima).
Sposobnost tvari da se vezuju za receptore naziva se terminom "afinitet". U odnosu na iste receptore, afinitet različitih tvari može biti različit.
Razlikuju se sledeće vrste receptora:
Recepti za membranu plazme:
tip kanala: kolinergički receptori N-tipa, H-holinergički receptori mišićnog tipa, GABA receptori;
g-proteinski receptori: α- i β-adrenergički receptori, M3 -holinoreceptori;
receptori integrativnog tipa: NO receptor.
Citosolna.
Mitohondrijalni.
Farmakodinamika je odjeljak opšta farmakologijaproučavaju značajke djelovanja lijekova na tijelo. Naime, farmakodinamika proučava:
- mehanizmi djelovanja lijekova;
- kraj farmakološki efekti;
- ovisnost djelovanja lijekova od različitih stanja;
- efekti lijekova nakon opetovane primjene;
- kombinirano djelovanje lijekova;
- nespojivost lijekova;
- nuspojave lijekova.
Mehanizmi delovanja lijekovi
Mehanizmi djelovanja lijekova su načini na koje tvari uzrokuju farmakološke učinke. Glavni mehanizmi djelovanja lijekova uključuju:
- Fizički.
- Mehanizam direktne hemijske interakcije.
- Membrana (fizikalno-hemijska).
- Enzimski (biohemijski).
- Receptor.
Fizički mehanizam djelovanja. Djelovanje ljekovite tvari povezano je s njegovim fizičkim svojstvima. Na primjer, aktivni ugljen se posebno obrađuje, te stoga ima visoku površinsku aktivnost. To mu omogućava da apsorbuje plinove, alkaloide, toksine itd.
Direktna hemijska interakcija. Ovo je prilično rijedak mehanizam djelovanja lijekova, čija je suština u tome da lijekovi direktno stupaju u interakciju sa molekulima ili ionima u tijelu. Takav mehanizam djelovanja ima, na primjer, unitiolni lijek koji pripada grupi protuotrova. U slučaju trovanja tiolnim otrovima, uključujući soli teških metala, unitiol ulazi u izravnu hemijsku reakciju s njima, što rezultira stvaranjem netoksičnih kompleksa koji se izlučuju mokraćom. Tako djeluju i antacidi koji ulaze u izravnu kemijsku interakciju sa solnom kiselinom, snižavajući kiselost želučanog soka.
Membrana (fizikalno-hemijske) mehanizam. Povezana je s učinkom lijekova na jonske struje (Na +, K +, Cl - i druge), koje određuju transmembranski električni potencijal. Prema ovom mehanizmu javljaju se anestetici, antiaritmički lekovi, lokalni anestetici itd.
Enzymatic (biohemijska) mehanizam. Taj mehanizam određuje sposobnost nekih lekova da aktiviraju ili inhibirajuće na enzime. Arsenal lijekova s \u200b\u200btakvim mehanizmom djelovanja je vrlo širok. Na primjer, antiholinesterazni lijekovi, inhibitori monoamin oksidaze, blokatori protonske pumpe itd.
Receptorni mehanizam. U ljudskom telu postoje visoko specifične biološki aktivne supstance (posrednici) koji stupaju u interakciju sa receptorima i menjaju funkcije različitih organa ili tkiva u telu.
Receptori su makromolekularne strukture sa selektivnom osjetljivošću na određena hemijska jedinjenja. Uz interakciju lijekova s \u200b\u200breceptorima, događaju se biokemijske i fiziološke promjene u tijelu, praćene jednim ili drugim kliničkim učinkom.
Pozvani su posrednici i lijekovi koji aktiviraju receptore i uzrokuju biološki učinak agonisti. Ljekovite tvari koje se vezuju za receptore, ali ne uzrokuju njihovu aktivaciju i biološki učinak, smanjuju ili uklanjaju učinke agonista, nazivaju se antagonisti. Dodijelite također agonisti antagonista - tvari koje djeluju različito na podtipove istih receptora: stimulišu neke podvrste receptora, a blokiraju druge. Na primjer, narkotički analgetik nalbufin stimulira receptore opioidne kappe (dakle smanjuje osjetljivost na bol) i blokira opioidne mu receptore (dakle, manje je opasan u pogledu ovisnosti o lijekovima).
Sposobnost tvari da se vezuju za receptore naziva se terminom "afinitet". U odnosu na iste receptore, afinitet različitih tvari može biti različit.
Razlikuju se sledeće vrste receptora:
- Recepti za membranu plazme:
- tip kanala: kolinergički receptori N-tipa, H-holinergički receptori mišićnog tipa, GABA receptori;
- g-proteinski receptori: α- i β-adrenergički receptori, M3 -holinoreceptori;
- receptori integrativnog tipa: NO receptor.
- Citosolna.
- Mitohondrijalni.
- Nuklearna
Recepti za membranu plazme.
Receptori tipa kanala
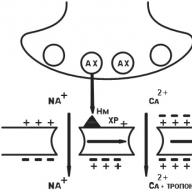
N n -holinergički receptori nervnog tipa (CNS, autonomne ganglije, sinokarotidna zona, hromafin tkivo nadbubrežne žlijezde). Nakon vezanja acetilholina (AX) s H n -holinergičkim receptorima, Na + kanali se otvaraju i Na se odvodi u ćeliju noseći pozitivan naboj. Postinaptička membrana je depolarizirana. Postoji akcijski potencijal koji se pomiče duž membrane neurona, otvarajući električno ovisne Na + kanale. U postganglionskom vlaknu nastaje nervni impuls (Sl. 6).
Sl. 6. N n -holinergički receptor
N m - holinergički receptor mišićnog tipa (membrane skeletnih mišićnih stanica). Početni procesi su slični, ali otvaraju se Ca ++ kanali o električnom razvoju. Ioni Ca ++ ulaze u mišićna vlakna, Ca ++ se oslobađa iz sarkoplazmatskog retikuluma. Razina Ca ++ raste, što inducira kontrakciju mišića (Sl. 7).

Sl. 7. N m-holinergički receptor
GABA receptori. Ovo su receptori za γ-aminobuternu kiselinu (GABA). GABA djeluje u interakciji s GABA receptorima, u čijoj strukturi postoje kloridni kanali. Kao rezultat stimulacije receptora, kanali se otvaraju i kloni ioni (Cl -) slobodno ulaze u ćeliju. Povećanje koncentracije jona hlora unutar ćelije dovodi do hiperpolarizacije membrane i smanjenja aktivnosti neurona. Teže je pobuđivati \u200b\u200btakvu ćeliju (sl. 8).

Sl. 8. GABA receptor:
GABA-R - GABA receptor, BD-R - benzodiazepinski receptor, BR - barbituratni receptor
Receptori povezani sa G proteina
G-proteini, tj. Proteini koji se vežu za GTP (guanozin trifosfat), lokalizirani su u staničnoj membrani i sastoje se od α-, β- i γ-podjedinica. Oni (G-proteini) regulišu aktivnost određenih efektora (trenutni glasnici, sekundarni posrednici). Ovi glasnici mogu biti enzma (adenilat ciklaza, fosfolipaza); kanali za kalijum, kalcijum, natrijum; neke transportne proteine. Svaka ćelija može imati mnogo G-proteina, a svaka od njih reguliše aktivnost različitih glasnika, istovremeno mijenjajući funkciju stanice.
M3 -holinergički receptor (membrane glatkih mišića (MMC) i ćelije egzokrinih žlezda). Acetilholin stimulira M3 -XR vezan na G protein. Aktivira se fosfolipaza-C (FLS), koja katalizira cepanje PIDP (fosfatidilinozitol-difosfat) u ITP (inozitol trifosfat) i DAG (diacilglicerol). ITF koji ulazi u citoplazmu MMC oslobađa Ca ++ iz kavela .

Sl. 9. M3-holinergički receptor
Ca ++ se veže na kalmodulin, aktivira miozin-kinazu (MK), koja katalizira fosforilaciju lakih lanaca miozina, što dovodi do kontrakcije ćelije (Sl. 9). Slično tome, impuls se prenosi u sinapsama sekretornih žlijezda.
Norepinefrin stimulira α 1 -adrenoreceptorPokretanjem sljedećeg lanca događaja:
Norepinefrin (HA) → α 1 -adrenoreceptor → aktivacija α-podjedinice G s-proteina → aktivacija PLL → cijepanje FIDF-a → porast ITF koncentracije → porast koncentracije Ca 2+ u stanici → Ca 2+ veže se na kalmodulin → aktivira se miozin-kinaza → lagani lanci fosforilat → laki lanac miozin → miozin u interakciji s aktinom → razvija se smanjenje MMC-a (Sl. 10).

Sl. 10. α 1 -adrenoreceptor
b 1 receptor(sl. 11). Norepinefrin → aktivira b 1 -AP → aktivacija α-podjedinice G-proteina → aktivacija AC → povećanje proizvodnje cAMP iz ATP → porast koncentracije cAMP u kardiomiocitu → aktiviranje protein kinaza → fosforilacija proteina kalcijumovih kanala → povećanje ulaza Ca 2+ kroz kanale i povećanje koncentracije Ca 2+ u ćeliji → povećajte snagu kontrakcija srca.

Sl. 11 b 1 receptor
b 2 receptor(sl. 12). ON → b 2 -AP → aktiviranje α-podjedinice G-proteina → aktivacija AC → povećana formacija cAMP → stimulirana proteinska kinaza → kinaza koja katalizira fosforilaciju miozin-kinaze, cijepa se, a aktivnost posljednjeg se gubi → fosforilacija miozina ne dolazi → MMC opuštanje.
Regulaciju oslobađanja HA iz nervnih završetaka vrši sam neurotransmiter nakon pobuđivanja presinaptičke membrane α 2 -AP. Emisija HA smanjuje se.

Sl. 12 b 2 receptor
Receptori integrativnog tipa
To su receptori koji su proteini koji prodiru kroz membranu. U tom slučaju vanjski dio proteina igra receptorsku ulogu, dok unutarnji dio igra katalitičku ulogu (Sl. 13).

Sl. 13 Integrirani receptor
Citosolni receptori
U fiziološkim uslovima, takvi receptori služe za vezanje steroidnih hormona (polni hormoni, glukokortikoidi). Ove tvari ulaze u stanicu i vezuju se za citosolne receptore. Ovaj kompleks prodire u jezgro i tamo mijenja rad genoma. Kao rezultat toga, mijenja se sinteza proteina u stanici (Sl. 14).
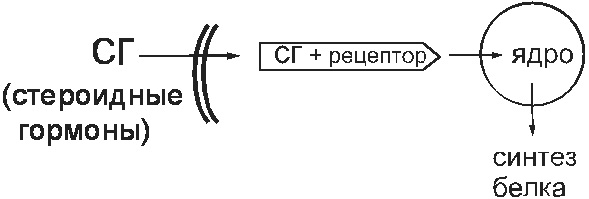
Sl. 14 Citosolni receptor
Mitohondrijski receptori
U mitohondrijama se nalaze i receptori s kojima ljekovite tvari djeluju, poput trijodtironin hidroklorida, koji su analogi prirodnog hormona T3. Kao rezultat ove interakcije, sinteza ATP se povećava.
Nuklearni receptori
T3 prodire u jezgro i tamo stupa u interakciju sa receptorima ove vrste. Kao rezultat toga, rad genoma se mijenja i sintetiziraju se novi proteini.
Konačni farmakološki efekti (prema Veršininu)
Uprkos obilju lijekova, promjene koje uzrokuju u tijelu su iste vrste (sl. 15). Učinak bilo kojeg lijeka na organe može se smanjiti na pet glavnih farmakoloških učinaka (prema N. V. Vershinin):
- Umirujuće - smanjenje na normalno pojačano funkcionisanje organa (upotreba sedativa).
- Ugnjetavanja - pad ispod norme funkcije tijela (upotreba lijekova za anesteziju)
- Paraliza - prestanak smanjene funkcije organa (respiratorna depresija u slučaju predoziranja opojnih analgetika).
- Toniranje - jačanje smanjene funkcije na normalno (upotreba β -adrenomimetika).
- Uzbuđenje - Povećanje funkcije organa iznad norme (uporaba diuretika u slučaju trovanja, lijekovi za iskašljavanje).
Sl. 15. Konačni farmakološki efekti

Vrste djelovanja lijekova
- Glavna stvar je sekundarna.
Glavna stvar radnja je ona koja je u osnovi terapijskog ili profilaktičkog davanja leka. Kolateralna - nepoželjno, opasno za pacijenta djelovanje lijekova.
- Reverzibilni, nepovratni.
Jednom u tijelu, ljekovite supstance stupaju u interakciju sa onim ćelijama koje imaju biološki supstrat koji je sposoban reagirati s ovom supstancom. Ta interakcija ovisi o kemijskoj strukturi lijeka. Vezivanje lekovite supstance na odgovarajući supstrat je reverzibilni ako se oni (supstrat i lijek) na neko vrijeme vežu.
U rijetkim slučajevima terapeutski cilj iziskuje nepovratna isključivanje strukture iz svoje funkcije. To se odnosi, na primjer, na većinu antimikrobnih, antitumorskih agenasa koji su u stanju formirati snažne (kovalentne) veze s elementima DNK spiralnih ćelija („umrežavanje“) ili bakterijskim enzimima, uslijed čega ćelije gube sposobnost reprodukcije.
- Direktno, indirektno (indirektno).
Direktno djelovanje podrazumijeva da je terapeutski učinak posljedica izravne interakcije lijeka s biosubstrom oboljelog organa i izravno dovodi do određenih pomaka. Ako se funkcija organa (sistema) po drugi put promijeni direktan uticaj droga na drugi organ, drugi sistem, ova akcija se naziva indirektna (indirektna). Srčani glikozidi poboljšavaju kontraktilnost miokarda ( direktna akcija) i, kao rezultat, poboljšavaju cirkulaciju krvi u tijelu, što je popraćeno poboljšanjem diureze (indirektni efekat).
Poseban je slučaj indirektne akcije refleks radnja. Na primjer, vazodilatacija i poboljšanje trofičnog tkiva kao posljedica iritacije krajeva senzornih živaca kože.
- Selektivno, neselektivno.
Selektivna radnja je učinak terapijskih doza lijekova na specifične receptore. Na primjer, učinak salbutamola na β2-adrenoreceptore. Treba imati na umu da je selektivnost lijekova relativna, s povećanjem doza nestaje.
- Lokalna, resorptivna.
Lokalno učinak lijeka vrši se prije nego što ga se apsorbira u krv (na primjer, mast).
Resorptive (sistemsko) delovanje razvija se nakon apsorpcije lijeka u krv. Ogromna većina lijekova ima ovaj efekat.
U velikoj većini slučajeva da bi lijek (ligand) mogao pokazati svoje djelovanje mora se zadovoljiti specifičnim komponentama u tijelu - receptorskim ciljevima, molekularnim strukturama koje su protein, rjeđe nukleinskim kiselinama, lipidima ili drugim konfiguracijama koje se nalaze unutar ili na površini ćelija i sl. s kojom stupa u interakciju, započinjući lanac biohemijskih i fizikalno-hemijskih procesa koji vode do određenog efekta.
Postoje dvije vrste membranskih receptora - ionski kanali i receptori povezani sa G-proteinom. Na primjer, natrijumski kanal karakterističan je za adetilholin i slične lijekove. Acetilholin uzajamno djeluje sa proteinom kanala, uzrokujući u njemu konformacijske promjene, koje doprinose otvaranju kanala i prodiranju natrijum jona u ćeliju. Taj proces je u osnovi nervnog uzbuđenja. Neke ljekovite tvari, u interakciji s bjelančevinom natrijum-kanala, sprečavaju njegovo otvaranje, blokirajući tako prijenos živčanih ekscitacija.
Takozvani G-protein pričvršćen je za unutarnji dio plazma membrane stanica, što osigurava sinkronizaciju procesa interakcije lijekova s \u200b\u200bistodobnom aktivacijom odgovarajućih intracelularnih ciljnih proteina. Kao što je prikazano na slici, molekul lijeka uzajamno djeluje sa receptorom (P) na vanjskoj površini membrane, što izaziva konformacijske promjene receptora proteina. Zbog toga G-protein mijenja svoju prostornu strukturu, migrira u ravnini membrane do enzima koji su u neaktivnom stanju unutar ćelije. Interakcija G-proteina s enzimima (T) određuje njihovu aktivaciju (LV / P / T). Norepinefrin, dopamin i drugi ligandi djeluju posebno na receptore povezane sa G-proteinom. Treba napomenuti da acetilkolin može komunicirati ne samo s proteinskim kanalima, već i s receptorima povezanim s G-proteinom.
Da bi došlo do interakcije između liganda i bioreceptora, potrebno je da one imaju komplementarnost, to jest da između njih mora postojati određeni afinitet, odnosno afinitet (dopisivanje veličine, prostorna konfiguracija, prisustvo suprotnih naboja itd.). Na primjer, negativni naboj receptora mora odgovarati pozitivnom naboju egzogenog liganda, a nepolarni radikali neke tvari mogu se vezati na hidrofobna mjesta receptora.
Među fizikalno-hemijskim svojstvima ljekovitih tvari koje utječu na njihovu interakciju s receptorima, treba izdvojiti veličinu molekula, ovisno o tome koja tvar može komunicirati s čitavim receptorom ili s njegovom komponentom. Kinetika njegovog prodora kroz biološke membrane također ovisi o veličini molekule lijeka. Tipično, kako se povećava veličina molekula, povećava se njena fleksibilnost i mogućnost stvaranja van der Waals veza s makromolekularnim partnerom. Osim toga, važna je stereohemija molekula lijeka. Farmakološka aktivnost ovisi o izomernom obliku ljekovite supstance. I treba imati na umu: što je tvrđa konformacija molekula receptora, to je veća razlika u djelovanju stereoizomera.
Interakcija ljekovite tvari - receptora nastaje zbog intermolekularnih veza. U početku tvar privlači receptor elektrostatskim silama, pa u prisustvu komplementarnosti formira veze s receptorom koristeći fizičke i fizikalno-hemijske interakcije (tipične za lijekove koji se izlučuju iz tijela u nepromijenjenom ili nepromijenjenom obliku) ili kemijske interakcije (svojstvene spojevima koji podvrgnuti hemijskim transformacijama u tijelu). Najslabije van der Waalove sile sudjeluju u određivanju specifičnosti interakcije ljekovite tvari s biohemijskim reaktivnim sustavima. Vodikove veze uključene su u procese prepoznavanja i fiksiranja neke tvari (liganda) u biostrukture. Ionske veze nastaju u slučajevima kada ljekovite tvari sadrže kationsku ili anionsku skupinu, a suprotne strukture su u bioreceptorima. Često se ionske veze formiraju u prvim fazama farmakološke reakcije između tvari i receptora. U takvim slučajevima, učinak lijeka je reverzibilan. Važno je formiranje koordinacijskih kovalentnih veza. S njihovim učešćem nastaju interakcije alkilacijskih sredstava s biosubratima, kao i lijekova i protuotrova s \u200b\u200bmetalima, pri nastanku stabilnih helatnih kompleksa, na primjer, untiol s arsenom ili tetacin-kalcij s olovom. Djelovanje takvih tvari je nepovratno.
Pored toga, postoji hidrofobna interakcija. Iako je energija njegovih veza mala, interakcija velikog broja dugih alifatičkih lanaca dovodi do pojave stabilnih sistema. Hidrofobne interakcije igraju ulogu u stabiliziranju biopolimernih konformacija i stvaranju bioloških membrana.
Ostaci aminokiselina u molekuli proteinskih receptora sadrže polarne i nepolarne grupe koje određuju stvaranje polarnih i nepolarnih veza između njih i ljekovitih supstanci. Polarne grupe (-OH, -NH, COO-, -N3H, \u003d O) omogućavaju formiranje uglavnom jonskih i vodoničnih veza. Nepolarne grupe (vodonik, metil, ciklički radikali itd.) Tvore hidrofobne veze sa lekovitim tvarima male molekulske mase.
Dakle, interakcija lijekova sa specifičnim receptorima može se postići različitim hemijskim vezama koje imaju nejednaku snagu. Dakle, približna jačina kurariformnih supstanci s holinergičkim receptorima za elektrostatičku (ionsku) interakciju je 5 kcal / mol, dipol-ion - 2-5 kcal / mol, dipol-dipol - 1-3 kcal / mol, vodikove veze - 2-5 kcal / mol, van der Waals veze - 0,5 kcal / mol, hidrofobne veze - 0,7 kcal po CH2 grupi. Smanjenje čvrstoće veze ovisno o udaljenosti između atoma za elektrostatsku interakciju je r -2, dipolni ion je r -3, dipol dipola je r -4, vodikova veza r -4, van der Waalsova veza r -7 . Ova vrsta veze može se prekinuti, što osigurava reverzibilnost djelovanja lijekova. Trajnije su kovalentne veze koje pružaju dug i često nepovratan učinak tvari, na primjer, alkilirajući antitumorske lijekove. Većina lijekova reverzibilno se veže na receptore. U ovom je slučaju u pravilu priroda spoja vrlo složena: u njemu mogu istovremeno sudjelovati ionske, dipol-dipolske, van der Waals, hidrofobne i druge vrste veza, što je u najvećoj mjeri određeno komplementarnošću tvari i receptora, a samim tim i stupnjem njihove konvergencije između od sebe.
Snaga vezivanja neke tvari za receptore označena je terminom "afinitet". Tvari koje djeluju na iste receptore mogu imati različit stupanj afiniteta za njih. U ovom slučaju, tvari s većim afinitetom mogu izbaciti tvari s nižim afinitetom iz spoja s receptorima. Za određivanje ravnotežnog stanja između "okupiranih" receptora (DR), slobodnih receptora i slobodne supstance (D) koristi se konstanta disocijacije (K D) koja se određuje sljedećom formulom:
K D \u003d [D] * [R] / [DR]
Negativni logaritam K D (pR D) pokazatelj je afiniteta. Za karakterizaciju afiniteta često se koristi pokazatelj pD 2, tj. Negativni logaritam EC 50, (koncentracija tvari u kojoj izaziva učinak od 50% maksimalnog učinka).
Raznolikost kemijskih interakcijskih veza i njihova nejednaka snaga, odnosno srodnost između liganda i bioreceptora, objašnjavaju se složenom strukturom lijekova koji sadrže radikale različite reaktivnosti i koji imaju višedimenzionalni volumetrijski oblik, kao i složenošću procesa interakcije koji se često dešavaju u nekoliko faza (faza): stvaranje složenih slojeva ljekovita supstanca je receptor; intramolekularno grupiranje; složena disocijacija.
Stoga samo tvari s izraženim afinitetom prema bioreceptoru mogu izazvati farmakološki učinak. Ozbiljnost efekta ovisi o koncentraciji lijeka i ukupnom broju receptora.
Ako tvari imaju dovoljnu unutarnju aktivnost, tada se nazivaju agonistima. Pod unutrašnjom aktivnošću podrazumijeva se sposobnost agonista da uzrokuju biološki učinak promjenom konformacije receptora, tj. Sposobnost liganda da aktivira receptor. Ovaj fenomen se smatra afinitetom agonističko-recepcijskog kompleksa prema pretvaraču; pretvaranje vanjskih signala u unutarnje naziva se transdukcijom. Intracelularni prijenos signala je u osnovi procesa poput kontrakcije mišićnih vlakana, stanične diobe, proliferacije, diferencijacije itd. Sada je utvrđeno da ćelija ima mnogo tvari (hormoni, bioaktivni peptidi, nukleotidi, steroidi, bioregulatori niske molekularne težine itd.) specifični receptori. Kao rezultat interakcije ovih tvari s ovim specifičnim receptorima, nastaju sekundarni glasnici (posrednici) koji pokreću kaskadu biohemijskih reakcija.
Postoji koncept " djelomični agonisti"- ljekovite tvari koje, kad se vezuju za receptore, ne daju maksimalan učinak. Taj nerazumljivi fenomen navodno je posljedica nepotpune (manje) ovisnosti afiniteta kompleksa lijeka i receptora za traneduktorom. Na primjer, djelomični agonist receptora opijata djeluje slično kao i puni agonist ovih morfija, iako je slabiji od potonjeg. Istovremeno, kada se koristi zajedno, nalorfin slabi ili uklanja učinke morfija; posebno se uklanja inhibicijski učinak morfija na disanje. Izoprenalin je pravi agonist, a prenalterol je djelomični agonist β-adrenergičkih receptora. Prema teoriji receptora, pravi agonist može izazvati maksimalan odgovor, čak i ako djeluje samo sa dijelom receptora.
Specifični receptori mogu imati ista ili različita mjesta vezivanja za agoniste i antagoniste. Moguća su različita mjesta vezivanja za različite agoniste. U slučaju kada agonist i antagonist imaju ista mesta vezivanja i blokirajući efekat antagonista na receptor u potpunosti se eliminira povećanjem koncentracije agonista (postiže se maksimalan učinak agonista), odnos između antagonista i agonista označava se kao konkurentski antagonizam. Ako su mjesta vezivanja za agonist i antagonist različita, tada se odnos između njih definira kao nekompetitivni antagonizam. Za karakterizaciju antagonista često se koristi pA2 (negativni logaritam molarne koncentracije antagonista, pri kojem se njegova koncentracija mora udvostručiti kako bi se dobio standardni efekat agonista).
U uslovima celog organizma, agonisti i antagonisti izazivaju promene u određenim fiziološkim funkcijama. U ovom slučaju djelovanje antagonista određuje se činjenicom da inhibiraju utjecaj specifičnih prirodnih liganda na specifične receptore (na primjer, atropin M-holinergički antagonist inhibira djelovanje njihovog agonista acetilkolina). Promjene koje su u direktnoj vezi s interakcijom tvari sa specifičnim receptorima označavaju se pojmom "primarna farmakološka reakcija koja može biti početak niza reakcija koje vode do stimulacije ili inhibicije određenih fizioloških funkcija".
Promjene u funkcijama organa ili sustava (na primjer, promjena snage i učestalosti srčanih kontrakcija, tonusa glatkih mišića unutarnjih organa, izlučivanje žlijezda, krvni tlak itd.) Uzrokovane lijekovima su označene kao farmakološki učinci ove tvari. Dakle, za srčane glikozide primarna farmakološka reakcija je inhibicija aktivnosti transportne Na +, K-ATPaze miokardnih vlakana, što se smatra mogućim specifičnim receptorom za srčane glikozide. U vezi s tim, poremećaj ulaska K + u mišićna vlakna i izlazak iz Na + vlakana povećava se i sadržaj Ca2 + u citoplazmi, što pospješuje interakciju aktina i miozina. Rezultat tih promjena je porast broja otkucaja srca što je glavni farmakološki učinak srčanih glikozida.
Produljeno izlaganje specifičnih receptora agonistima često je popraćeno smanjenjem njihove osjetljivosti. Potonji mogu biti povezani sa promjenom receptora, smanjenjem njihovog broja (gustoće) ili poremećajem procesa koji slijede nakon pobuđivanja receptora. U tom slučaju, farmakološki efekti agonista postaju manje izraženi.
Dakle, farmakološki učinci većine lijekova povezani su s njihovim učinkom na odgovarajuće specifične receptore.
Tvari visokog afiniteta prema bioreceptoru i niskom unutrašnjom aktivnošću nazivaju se antagonisti, odnosno blokatori, jer oni, bez izazivanja promjena u konformaciji bioreceptora, ometaju interakciju endogenih i / ili egzogenih agonističkih liganda s njim. Postoje takozvani "sekundarni ili glupi receptori sa kojima se vezuju ljekovite tvari, ali nemaju farmakološki učinak. Takvi "glupi" receptori najčešće su prisutni u proteinima i krvnoj plazmi (ali se mogu naći i u tkivima). Povezanost s "nemim" receptorima dovodi do smanjenja koncentracije slobodne ljekovite supstance, a time i do smanjenja terapeutskog efekta.
Brojne suvremene teorije kojima se objašnjava mehanizam interakcije ligand-receptor, stanje samih receptora, nedostatak proporcionalnosti između broja zauzetih receptora i konačne reakcije, promjene u efikasnosti prijenosa signala i postojanje rezervnih receptora i djelomičnih agonista itd. Činile su osnovu za ideje o mehanizmu djelovanja predstavnika raznih grupe lekova. Ove interakcije dijele se na interakciju receptora i na kemijsku interakciju.
Mehanizam interakcije lijekova s \u200b\u200bbioreceptorima mogu se prikazati kao sljedeća shema: svaki se ligand (ljekovita supstanca ili fiziološki supstrat) veže na točno određeno mjesto na određenom receptoru. Aktivirani receptori direktno ili indirektno regulišu protok iona (1) i / ili druge unutarćelijske procese (izlučivanje ili kontrakciju mišića) ili aktiviraju sistem proteina koji veže nukleotide gvanin (G-proteini), što, pak, pojačava aktiviranje drugog sistema enzim-posrednika. Nekoliko različitih drugih medijatora funkcionira u citoplazmi, aktivirajući različite ciljne proteine, na primjer, proteinske kinaze. Potonji djeluju na specifične podloge i posreduju farmakološki učinak.
Iz predstavljenog opisa jasno je da se djelovanje lijekova provodi sljedećim mehanizmima:
- fiziološke funkcije tkiva (na primjer kontraktilna, sekretorna) mogu se regulirati s nekoliko receptora, a samim tim i raznim ligandima;
- može biti nekoliko intermedijarnih koraka između interakcije ljekovite tvari s receptorom i odgovora tkiva ili organa, posebno aktivacije drugih receptora povezanih sustava liječnika;
- efikasnost mehanizama odgovornih za slijed podražaja-odgovor, kao i gustina receptora, mogu varirati od tkiva do tkiva.
Terapeutski učinak određenih lijekova nastaje uslijed njihove direktne (nevezano za specifične receptore) hemijske interakcije s endogenim spojevima ili drugih mehanizama interakcije (osmotski pritisak, adsorpcija). Dakle, za osmotske diuretike - manitol, urea - nema specifičnih receptora. Ove tvari povećavaju osmotski tlak u bubrežnim tubulima, uslijed čega dolazi do poremećaja reapsorpcije vode i diureze. Djelovanje adsorpcijskih tvari, diuretika koji formiraju kiselinu nije povezano sa specifičnim receptorima.
Antacidi (npr. Aluminij ili magnezijevi hidroksidi) reagiraju s klorovodičnom kiselinom, čime nastaju proizvodi slabih kiselinskih svojstava. Hemirajuće tvari koje se vežu za neke metale formiraju neaktivne hemijske komplekse.
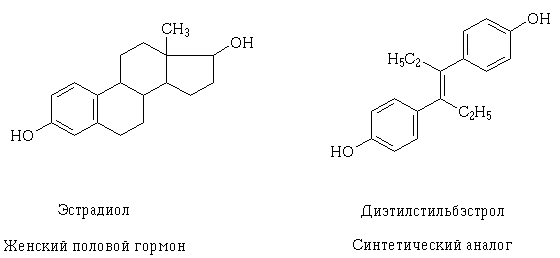
Kako se znanje o strukturi receptora i mehanizmu moguće farmakodinamičke interakcije lijekova na staničnoj razini produbljuje, moguće ih je namjerno stvoriti, kao i objasniti zašto lijekovi mogu imati takav učinak, a koji se na prvi pogled razlikuju po njihovoj strukturi. Primjer takve pojave je estradiol i transizomer dietilstilbestrola, sintetičkog analoga ženskog genitalija. Njihovi strukturni molekuli su različiti, ali sadrže iste hidroksi skupine po svojstvima i veličinama, slično smještene i orijentirane u prostoru, zbog čega molekule tih tvari mogu komunicirati s istim receptorom i imaju sličan farmakološki učinak.
Načini na koje ljekovite tvari izazivaju određene farmakološke učinke označeni su terminom "mehanizmi djelovanja". Ovaj se koncept koristi za objašnjenje učinaka lijekova na molekularnom, organskom i sistemskom nivou. Na primjer, mehanizam djelovanja antiholinesteraze na molekularnom nivou svodi se na blokadu acetilkolinesteraze interakcijom s njenim anionskim i esterazim centrima. Istovremeno se objašnjava mehanizam hipotenzivnog učinka antiholinesteraznih lijekova, bradikardija i vazodilatacija kao razlog ovog efekta, tj. Oni razmatraju mehanizam ovog djelovanja na razini organa.
Studije mehanizama djelovanja lijekova su u tijeku, a ideje o mehanizmu djelovanja lijeka s obzirom na to da se dobivaju novi podaci ne samo da mogu postati detaljnije, već i značajno se promijeniti.