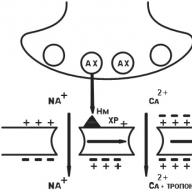
مکانیسم های عمل مواد دارویی - این روشهایی است که مواد باعث اثرات دارویی می شوند. مکانیسم اصلی فعالیت داروها شامل موارد زیر است:
جسمی
مکانیسم تعامل مستقیم شیمیایی.
غشاء (فیزیکی و شیمیایی).
آنزیمی (بیوشیمیایی).
گیرنده
مکانیسم فیزیکی عمل. عمل یک ماده دارویی با خواص فیزیکی آن همراه است. به عنوان مثال ، کربن فعال شده به طور ویژه فرآوری می شود و بنابراین فعالیت سطح بالایی دارد. این به او اجازه می دهد تا گازها ، آلکالوئیدها ، سموم و غیره را جذب کند.
تعامل شیمیایی مستقیم. این یک مکانیسم نسبتاً نادر از عملکرد داروها است ، ماهیت آن این است که داروها به طور مستقیم با مولکولها یا یونها در بدن ارتباط برقرار می کنند. چنین مکانیسم عمل ، به عنوان مثال ، توسط داروی یونیتول متعلق به گروه پادزهرها موجود است. در صورت مسمومیت با سم های تیول از جمله نمک های فلزات سنگین ، یونیتول با آنها یک واکنش شیمیایی مستقیم وارد می کند و در نتیجه باعث تشکیل مجتمع های غیر سمی می شود که در ادرار دفع می شوند. بنابراین ، آنتی اسیدها نیز عمل می کنند ، که با یک اسید هیدروکلریک وارد یک تعامل شیمیایی مستقیم می شوند و باعث کاهش اسیدیته آب معده می شوند.
غشاء (فیزیکوشیمیایی) مکانیسم این دارو با تأثیر داروها بر جریانهای یونی (Na + ، K + ، Cl - و سایر موارد) که پتانسیل الکتریکی ترانسمیبنی را تعیین می کنند ، همراه است. طبق این مکانیسم ، بیهوشی ، داروهای ضد آریتمی ، بی حسی موضعی و غیره استفاده می شود.
آنزیمی (بیوشیمیایی) مکانیسم این مکانیسم با توانایی برخی داروها در انجام اثر فعال کننده یا مهاری بر روی آنزیم ها تعیین می شود. زرادخانه مواد مخدر با چنین مکانیسم عمل بسیار گسترده است. به عنوان مثال ، داروهای آنتی کولین استراز ، مهارکننده های مونوآمین اکسیداز ، مسدود کننده پمپ پروتون و غیره.
مکانیسم گیرنده. در بدن انسان مواد بیولوژیکی بسیار فعال (واسطه ها) وجود دارد که با گیرنده ها در تعامل هستند و عملکردهای اندام ها یا بافت های مختلف بدن را تغییر می دهند.
گیرنده ها ساختارهای ماکرومولکولی با حساسیت انتخابی به برخی ترکیبات شیمیایی هستند. با تعامل داروها با گیرنده ها ، تغییرات بیوشیمیایی و فیزیولوژیکی در بدن اتفاق می افتد ، که با یک یا یک اثر بالینی دیگر همراه است.
واسطه ها و داروهایی که گیرنده ها را فعال کرده و باعث ایجاد اثر بیولوژیکی می شوند آگونیست ها. به مواد دارویی که به گیرنده ها متصل می شوند ، اما باعث فعال شدن و اثر بیولوژیکی آنها نمی شوند ، اثر آگونیست ها را کاهش داده یا از بین می برند ، خوانده می شوند. آنتاگونیست ها. تخصیص نیز آگونیست های آنتاگونیست - موادی که در زیرگروه های گیرنده های مشابه متفاوت عمل می کنند: برخی از زیرگروه های گیرنده را تحریک می کنند ، و دیگران را مسدود می کنند. به عنوان مثال ، nalbuphine ضد درد دارویی ، گیرنده های مواد مخدر کاپا را تحریک می کند (بنابراین حساسیت درد را کاهش می دهد) و گیرنده های موی افیونی را مسدود می کند (بنابراین ، از نظر وابستگی به مواد مخدر خطرناک تر است).
توانایی اتصال مواد به گیرنده ها با اصطلاح "میل" گفته می شود. در رابطه با گیرنده های مشابه ، میل به مواد مختلف می تواند متفاوت باشد.
انواع گیرنده های زیر متمایز می شوند:
گیرنده های غشایی پلاسما:
نوع کانال: گیرنده های کولینرژیکی از نوع N ، گیرنده های کولینرژیک نوع عضلانی ، گیرنده های GABA.
گیرنده های پروتئین G: گیرنده های α- و β- آدرنرژیک ، گیرنده های M3-colinoreceptors.
گیرنده های نوع یکپارچه: بدون گیرنده.
سیتوزولی
میتوکندری
فارماکودینامیک یک بخش است داروسازی عمومیبررسی ویژگیهای عملکرد داروها بر روی بدن. یعنی ، مطالعات فارماکودینامیک:
- مکانیسم عمل مواد مخدر؛
- پایان اثرات دارویی;
- وابستگی عمل به مواد مخدر به شرایط مختلف.
- تأثیر داروها بر تجویز مکرر.
- عمل ترکیبی از داروها؛
- ناسازگاری دارو؛
- عوارض جانبی داروها
مکانیسم های عمل داروها
مکانیسم های عملکرد داروها روش هایی هستند که باعث ایجاد مواد در اثر دارویی می شوند. مکانیسم اصلی فعالیت داروها شامل موارد زیر است:
- جسمی
- مکانیسم تعامل مستقیم شیمیایی.
- غشاء (فیزیکی و شیمیایی).
- آنزیمی (بیوشیمیایی).
- گیرنده
مکانیسم فیزیکی عمل. عمل یک ماده دارویی با خواص فیزیکی آن همراه است. به عنوان مثال ، کربن فعال شده به طور ویژه فرآوری می شود و بنابراین فعالیت سطح بالایی دارد. این به او اجازه می دهد تا گازها ، آلکالوئیدها ، سموم و غیره را جذب کند.
تعامل شیمیایی مستقیم. این یک مکانیسم نسبتاً نادر از عملکرد داروها است ، ماهیت آن این است که داروها به طور مستقیم با مولکولها یا یونها در بدن ارتباط برقرار می کنند. چنین مکانیسم عمل ، به عنوان مثال ، توسط داروی یونیتول متعلق به گروه پادزهرها موجود است. در صورت مسمومیت با سم های تیول از جمله نمک های فلزات سنگین ، یونیتول با آنها یک واکنش شیمیایی مستقیم وارد می کند و در نتیجه باعث تشکیل مجتمع های غیر سمی می شود که در ادرار دفع می شوند. بنابراین ، آنتی اسیدها نیز عمل می کنند ، که با یک اسید هیدروکلریک وارد یک تعامل شیمیایی مستقیم می شوند و باعث کاهش اسیدیته آب معده می شوند.
غشاء (فیزیکوشیمیایی) مکانیسم این دارو با تأثیر داروها بر جریانهای یونی (Na + ، K + ، Cl - و سایر موارد) که پتانسیل الکتریکی ترانسمیبنی را تعیین می کنند ، همراه است. طبق این مکانیسم ، بیهوشی ، داروهای ضد آریتمی ، بی حسی موضعی و غیره استفاده می شود.
آنزیمی (بیوشیمیایی) مکانیسم این مکانیسم با توانایی برخی داروها در انجام اثر فعال کننده یا مهاری بر روی آنزیم ها تعیین می شود. زرادخانه مواد مخدر با چنین مکانیسم عمل بسیار گسترده است. به عنوان مثال ، داروهای آنتی کولین استراز ، مهارکننده های مونوآمین اکسیداز ، مسدود کننده پمپ پروتون و غیره.
مکانیسم گیرنده. در بدن انسان مواد بیولوژیکی بسیار فعال (واسطه ها) وجود دارد که با گیرنده ها در تعامل هستند و عملکردهای اندام ها یا بافت های مختلف بدن را تغییر می دهند.
گیرنده ها ساختارهای ماکرومولکولی با حساسیت انتخابی به برخی ترکیبات شیمیایی هستند. با تعامل داروها با گیرنده ها ، تغییرات بیوشیمیایی و فیزیولوژیکی در بدن اتفاق می افتد ، که با یک یا یک اثر بالینی دیگر همراه است.
واسطه ها و داروهایی که گیرنده ها را فعال کرده و باعث ایجاد اثر بیولوژیکی می شوند آگونیست ها. به مواد دارویی که به گیرنده ها متصل می شوند ، اما باعث فعال شدن و اثر بیولوژیکی آنها نمی شوند ، اثر آگونیست ها را کاهش داده یا از بین می برند ، خوانده می شوند. آنتاگونیست ها. تخصیص نیز آگونیست های آنتاگونیست - موادی که در زیرگروه های گیرنده های مشابه متفاوت عمل می کنند: برخی از زیرگروه های گیرنده را تحریک می کنند ، و دیگران را مسدود می کنند. به عنوان مثال ، nalbuphine ضد درد دارویی ، گیرنده های مواد مخدر کاپا را تحریک می کند (بنابراین حساسیت درد را کاهش می دهد) و گیرنده های موی افیونی را مسدود می کند (بنابراین ، از نظر وابستگی به مواد مخدر خطرناک تر است).
توانایی اتصال مواد به گیرنده ها با اصطلاح "میل" گفته می شود. در رابطه با گیرنده های مشابه ، میل به مواد مختلف می تواند متفاوت باشد.
انواع گیرنده های زیر متمایز می شوند:
- گیرنده های غشایی پلاسما:
- نوع کانال: گیرنده های کولینرژیکی از نوع N ، گیرنده های کولینرژیک نوع عضلانی ، گیرنده های GABA.
- گیرنده های پروتئین G: گیرنده های α- و β- آدرنرژیک ، گیرنده های M3-colinoreceptors.
- گیرنده های نوع یکپارچه: بدون گیرنده.
- سیتوزولی
- میتوکندری
- هسته ای
گیرنده های غشایی پلاسما.
گیرنده های نوع کانال
گیرنده کولینرژیک N از نوع عصب (CNS ، گانگلیون خودمختار ، منطقه سینوکاروتیید ، بافت غده آدرنال کرومافین). پس از اتصال استیل کولین (AX) با گیرنده های H- کلینرژیک ، کانال های Na + باز می شوند و سدیم سدیم وارد سلول می شود و دارای بار مثبت است. غشای پست سیناپسی دپولاریزه است. یک پتانسیل عملی وجود دارد که در امتداد غشای نورون تغییر می کند و کانال های Na + وابسته به الکتریکی را باز می کند. یک ضربان عصبی در فیبر postganglionic بوجود می آید (شکل 6).
شکل 6. گیرنده کولینرژیک N n
Nm - گیرنده کولینرژیک نوع عضلانی (غشاهای سلول عضله اسکلتی). مراحل اولیه مشابه هستند ، اما کانال های Ca ++ وابسته به برق باز هستند. یون های Ca ++ وارد فیبر عضلانی می شوند ، Ca ++ از شبکه شبکه سارکوپلاسمی آزاد می شود. سطح Ca ++ بالا می رود ، که باعث انقباض عضلات می شود (شکل 7).

شکل 7. گیرنده N-m-cholinergic
گیرنده های گابا. این گیرنده های اسید γ-aminobutyric (GABA) هستند. GABA با گیرنده های GABA تعامل دارد ، در ساختار آنها کانال های کلریدی وجود دارد. در نتیجه تحریک گیرنده ، کانال ها باز می شوند و یون های کلر (Cl -) آزادانه وارد سلول می شوند. افزایش غلظت یون های کلر در داخل سلول منجر به پپلاریزاسیون غشاء و کاهش فعالیت نورون ها می شود. تحریک چنین سلولی دشوارتر است (شکل 8).

شکل 8. گیرنده گابا:
GABA-R - گابا گیرنده ، BD-R - گیرنده بنزودیازپین ، BR - گیرنده باربیتورات
گیرنده های مرتبط با پروتئین G
پروتئین های G ، یعنی پروتئین های اتصال GTP (گوانوزین تری فسفات) ، در غشای سلولی بومی سازی شده و از α- ، β- و γ-زیر واحد تشکیل شده اند. آنها (پروتئین های G) فعالیت جلوه های ویژه (پیام رسان های فوری ، واسطه های ثانویه) را تنظیم می کنند. این پیام رسان ها می توانند آنزیم باشند (آدنیلات سیکلاز ، فسفولیپاز). کانال های پتاسیم ، کلسیم ، سدیم؛ برخی پروتئین های حمل و نقل هر سلول می تواند پروتئین های G زیادی داشته باشد ، هر یک از آنها فعالیت پیام رسان های مختلف را تنظیم می کند ، ضمن اینکه عملکرد سلول را تغییر می دهد.
گیرنده كولینرژیك M 3 (غشای عضله صاف (MMCs) و سلولهای غده اگزوکرین). استیل کولین باعث تحریک M3-XR به پروتئین G می شود. فسفولیپاز-C (FLS) فعال می شود ، که باعث تجزیه کاتالیز PIDP (فسفاتیدیلینوزول دی فسفات) به ITP (اینوزیتول تری فسفات) و DAG (دیاسیل گلیسرول) می شود. ITF که وارد سیتوپلاسم MMC می شود ، Ca ++ را از غارها آزاد می کند .

شکل 9. گیرنده کولینرژیک M3
Ca ++ به کالمودولین متصل می شود ، میوزین کیناز (MK) را فعال می کند ، که باعث فسفوریلاسیون زنجیره های سبک میوزین می شود ، که منجر به انقباض سلول می شود (شکل 9). به طور مشابه ، تکانه ای در سیناپس های غدد ترشحی منتقل می شود.
نوراپی نفرین تحریک می کند α 1-آدرنرژیکبا شروع زنجیره ای از رویدادهای زیر:
نوراپی نفرین (HA) → α1-adrenoreceptor → فعال کردن زیرواحد پروتئین G s- فعال سازی PLL cle رخ FIDF → افزایش غلظت ITF → افزایش غلظت های Ca 2+ در سلول → Ca 2+ به کالمودولین → میوزین کیناز فعال می شود میوزین → میوزین با اکتین تداخل دارد → کاهش در MMC ایجاد می شود (شکل 10).

شکل 10. α 1-adrenoreceptor
ب 1 گیرنده(شکل 11). Norepinephrine b فعال سازی B1 -AP of فعال سازی α زیرواحد پروتئین G- فعال سازی AC → افزایش تولید اردوگاه از ATP → افزایش غلظت اردوگاه در کاردیومیوسیت ها → فعال سازی پروتئین کینازها → فسفوریلاسیون پروتئین های کلسیم entry افزایش ورود Ca 2+ از طریق کانال ها و افزایش غلظت کلسیم 2+ در سلول - افزایش قدرت انقباضات قلب.

شکل 11 گیرنده ب 1
ب 2 گیرنده(شکل 12). فعال کردن → b 2 -AP of فعال شدن α زیرواحد پروتئین G- فعال سازی AC formation افزایش تشکیل اردوگاه → پروتئین کیناز تحریک → کیناز که کاتالیز کردن فسفوریلاسیون میوزین کیناز است شکاف می یابد ، در حالی که فعالیت دوم از بین می رود → فسفوریلاسیون میوزین اتفاق نمی افتد → MMC.
تنظیم رهاسازی HA از انتهای اعصاب توسط انتقال دهنده عصبی توسط خود تحریک غشای پیش سازنده α2 -AP انجام می شود. انتشار HA کاهش می یابد.

شکل 12 گیرنده ب 2
گیرنده های نوع یکپارچه
این گیرنده ها پروتئین هایی هستند که به غشاء نفوذ می کنند. در این حالت ، قسمت بیرونی پروتئین نقش گیرنده را بازی می کند ، در حالی که قسمت داخلی نقش کاتالیزوری را ایفا می کند (شکل 13).

شکل 13 گیرنده نوع یکپارچه
گیرنده های سیتوزولی
تحت شرایط فیزیولوژیکی ، چنین گیرنده هایی برای اتصال هورمون های استروئیدی (هورمون های جنسی ، گلوکوکورتیکوئیدها) خدمت می کنند. این مواد وارد سلول شده و به گیرنده های سیتوزولی در آنجا متصل می شوند. این مجموعه به هسته نفوذ می کند و کار ژنوم را در آنجا تغییر می دهد. در نتیجه ، سنتز پروتئین در سلول تغییر می یابد (شکل 14).
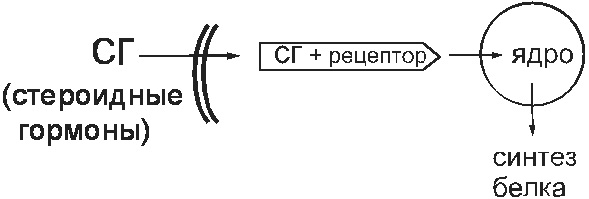
شکل 14 گیرنده سیتوزولی
گیرنده های میتوکندری
در میتوکندری نیز گیرنده هایی وجود دارد که مواد دارویی با آنها تداخل دارند ، مانند تریودوتیرونین هیدروکلراید ، که آنالوگ های هورمون طبیعی T 3 هستند. در نتیجه این تعامل ، سنتز ATP افزایش می یابد.
گیرنده های هسته ای
T3 به \u200b\u200bهسته نفوذ می کند و با گیرنده های این نوع تعامل دارد. در نتیجه ، کار ژنوم تغییر می کند و پروتئین های جدید سنتز می شوند.
اثرات دارویی نهایی (طبق گفته ورشینین)
علیرغم فراوانی داروها ، تغییرات ایجاد شده توسط آنها در بدن از همین نوع است (شکل 15). اثر هر دارویی بر روی اندام ها می تواند به پنج اثر اصلی دارویی کاهش یابد (طبق گفته N.V. Vershinin):
- تسکین دهنده - کاهش به حالت طبیعی افزایش عملکرد اندام (استفاده از داروهای آرام بخش).
- سرکوب - کمتر از حد معمول عملکرد بدن (استفاده از داروها برای بیهوشی) کاهش یابد.
- فلج - قطع عملکرد اندام کاهش یافته (افسردگی تنفسی در صورت مصرف بیش از حد مسکن های مخدر).
- تسکین دادن - تقویت عملکرد کاهش یافته به حالت عادی (استفاده از β 1-آدرنویمیمیکس).
- هیجان - افزایش عملکرد اندام بیش از حد طبیعی (استفاده از داروهای ادرارآور در صورت مسمومیت ، داروهای براق کننده).
شکل 15. اثرات دارویی نهایی

انواع عمل مواد مخدر
- نکته اصلی ثانویه است.
نکته اصلی یک عمل عملی است که زیربنای روش درمانی یا پیشگیری از یک دارو است. وثیقه - نامطلوب ، برای عمل بیمار داروها خطرناک است.
- برگشت پذیر ، برگشت ناپذیر.
هنگامی که در بدن هستید ، مواد دارویی با آن سلول هایی که دارای بستر بیولوژیکی هستند قادر به واکنش با این ماده هستند. این تعامل بستگی به ساختار شیمیایی دارو دارد. اتصال ماده مخدر به یک بستر مناسب است برگشت پذیر اگر آنها (بستر و مواد مخدر) برای مدتی به یکدیگر متصل شوند.
در چند مورد ، هدف درمانی نیاز دارد برگشت ناپذیر یک ساختار را از عملکرد آن خاموش کنید. این امر به عنوان مثال در مورد بسیاری از داروهای ضد میکروبی ، ضد توموری که قادر به ایجاد پیوندهای قوی (کووالانسی) با عناصر سلول های مارپیچ DNA ("اتصال متقابل") یا آنزیم های باکتریایی هستند ، در نتیجه سلول ها توانایی تولید مثل خود را از دست می دهند.
- مستقیم ، غیرمستقیم (غیرمستقیم).
مستقیم این عمل حاکی از آن است که اثر درمانی به دلیل تعامل مستقیم دارو با بیوسوبستر اندام بیمار بوده و مستقیماً به شیفتهای خاصی منتهی می شود. اگر عملکرد ارگان (سیستم) در نتیجه بار دوم تغییر کند تأثیر مستقیم دارو بر روی اندام دیگر ، سیستم دیگری ، این عمل غیر مستقیم (غیرمستقیم) نامیده می شود. گلیکوزیدهای قلبی باعث انقباض میوکارد (اثر مستقیم) و در نتیجه بهبود گردش خون در بدن می شوند که با بهبود دیورز (اثر غیرمستقیم) همراه است.
یک مورد خاص از یک اقدام غیرمستقیم است رفلکس عمل به عنوان مثال ، گشاد شدن عروق و بهبود بافت تروفیک در نتیجه تحریک انتهای اعصاب حسی پوست.
- انتخابی ، غیر انتخابی.
عمل انتخابی اثر دوزهای درمانی داروها بر روی گیرنده های خاص است. به عنوان مثال ، اثر سالبوتامول بر روی β2-آدرنرژیک ها. باید در نظر داشت که انتخاب داروها نسبی است ، با افزایش دوزها ، از بین می رود.
- محلی ، تحلیلگر.
محلی تأثیر دارو قبل از جذب آن به خون (به عنوان مثال پماد) انجام می شود.
بازدارنده عمل (سیستمیک) پس از جذب دارو به داخل خون توسعه می یابد. اکثر قریب به اتفاق داروها این تأثیر را دارند.
در اکثر موارد ، برای استفاده از یک ماده مخدر (لیگاند) که اثر خود را داشته باشد ، باید اجزای خاصی را در بدن داشته باشد - گیرنده های هدف ، ساختارهای مولکولی پروتئین ، کمتر اسیدهای نوکلئیک ، و غالباً اسیدهای نوکلئیک ، چربی یا سایر تنظیمات واقع در داخل یا سطح سلول ها ، که با آنها ارتباط برقرار می کند ، با شروع زنجیره ای از فرآیندهای بیوشیمیایی و فیزیکی و شیمیایی که منجر به اثر خاصی می شود
دو نوع گیرنده غشایی وجود دارد - کانال های یونی و گیرنده های مرتبط با پروتئین G. به عنوان مثال ، کانال سدیم مشخصه استیل کولین و داروهای مشابه است. استیل کولین با پروتئین کانال ارتباط برقرار می کند و باعث ایجاد تغییرات شکل در آن می شود ، که به باز شدن کانال و نفوذ یون های سدیم به سلول کمک می کند. این روند زمینه ساز هیجان عصبی است. برخی از مواد دارویی با تعامل با پروتئین کانال سدیم از باز شدن آن جلوگیری می کنند و از این طریق انتقال تحریک عصب را مسدود می کند.
پروتئین به اصطلاح G به قسمت داخلی غشای پلاسما سلولها متصل شده است ، که همزمان سازی فرآیند تعامل ماده مخدر با فعال سازی همزمان پروتئینهای هدف درون سلول را تضمین می کند. همانطور که در شکل نشان داده شده است ، مولکول دارو با گیرنده (P) در سطح بیرونی غشای تعامل برقرار می کند ، که باعث تغییرات ساختاری در پروتئین گیرنده می شود. به همین دلیل ، پروتئین G ساختار فضایی خود را تغییر می دهد ، در صفحه غشاء به آنزیم هایی که در حالت غیرفعال داخل سلول هستند مهاجرت می کند. تعامل پروتئین G با آنزیم ها (T) فعال سازی آنها (LV / P / T) را تعیین می کند. نوراپی نفرین ، دوپامین و سایر لیگاندها به طور خاص با گیرنده های مرتبط با پروتئین G در تعامل هستند. لازم به ذکر است که استیل کولین می تواند نه تنها با پروتئین کانال بلکه با گیرنده های مرتبط با پروتئین G ارتباط برقرار کند.
برای اینکه تعامل بین لیگاند و بیورسپتور اتفاق بیفتد ، لازم است که آنها یک مکمل هم داشته باشند ، یعنی بین آنها باید یک میل یا وابستگی خاص وجود داشته باشد (مکاتبات اندازه ، پیکربندی مکانی ، وجود بارهای متضاد و غیره). به عنوان مثال ، بار منفی گیرنده باید با بار مثبت یک لیگاند برون زا مطابقت داشته باشد ، و رادیکال های غیر قطبی یک ماده می توانند به سایت های آبگریز یک گیرنده متصل شوند.
از جمله خصوصیات فیزیکوشیمیایی مواد دارویی که بر تعامل آنها با گیرنده ها تأثیر می گذارد ، باید اندازه مولکول را از هم جدا کنیم ، بسته به این که این ماده با کل گیرنده یا با تشکیل دهنده آن در تعامل باشد. سینتیک نفوذ آن از طریق غشاهای بیولوژیکی نیز به اندازه مولکول دارو بستگی دارد. به طور معمول ، با افزایش اندازه یک مولکول ، انعطاف پذیری آن و احتمال تشکیل پیوندهای ون در والس با شریک ماکرومولکولی افزایش می یابد. علاوه بر این ، استریوشیمی یک مولکول دارو مهم است. فعالیت دارویی بستگی به فرم ایزومریک ماده دارویی دارد. و باید در نظر داشته باشید: هرچه ترکیب مولکول گیرنده سخت تر شود ، اختلاف عملکرد استریوایزرها بیشتر می شود.
اثر متقابل ماده دارویی - گیرنده به دلیل پیوندهای بین مولکولی است. در ابتدا ، یک ماده توسط نیروهای الکترواستاتیک به گیرنده جذب می شود و در صورت وجود مکمل ، با استفاده از فعل و انفعالات فیزیکی و فیزیکوشیمیایی پیوندهایی را با گیرنده ایجاد می کند (معمولاً برای داروهایی که از بدن به صورت غیرقابل تغییر یا تغییر یافته خارج می شوند) یا فعل و انفعالات شیمیایی (ذاتی ترکیبات که تحت تحولات شیمیایی در بدن). ضعیف ترین نیروهای ون در والس در تعیین ویژگی تعامل یک ماده دارویی با سیستم های واکنش بیوشیمیایی شرکت می کنند. پیوندهای هیدروژن در فرآیندهای تشخیص و تثبیت یک ماده (لیگاند) به ساختارهای زیستی نقش دارند. پیوندهای یونی در مواردی بوجود می آیند که مواد دارویی حاوی یک گروه کاتیونی یا آنیونی هستند و ساختارهای متضاد در بیورسکتورها قرار دارند. اغلب ، اوراق قرضه یونی در اولین مراحل واکنش دارویی بین مواد و گیرنده ها شکل می گیرد. در چنین مواردی ، اثر دارو برگشت پذیر است. تشکیل اوراق قرضه کووالانسی هماهنگی مهم است. با مشارکت آنها ، فعل و انفعالات عوامل آلکیل کننده کننده با بیوسوبستراتها ، و همچنین داروها و پادزهرها با فلزات ، در هنگام شکل گیری مجتمعهای کلات پایدار رخ می دهد ، به عنوان مثال ، یونیولیول با آرسنیک یا تتاسین-کلسیم با سرب. عمل چنین مواد غیر قابل برگشت است.
علاوه بر این ، تعامل آبگریز وجود دارد. اگرچه انرژی اوراق قرضه آن اندک است ، اما تعامل تعداد زیادی زنجیره بلند آلیفاتیک باعث ظهور سیستمهای پایدار می شود. برهم کنش های آبگریز در تثبیت ساختارهای بیوپلیمر و تشکیل غشاهای بیولوژیکی نقش دارد.
اسیدهای آمینه موجود در یک مولکول گیرنده پروتئین حاوی گروههای قطبی و غیر قطبی هستند که تشکیل پیوندهای قطبی و غیر قطبی بین آنها و مواد دارویی را تعیین می کنند. گروه های قطبی (-OH ، -NH ، COO- ، -N3H ، \u003d O) تشکیل پیوندهای عمدتا یونی و هیدروژن را فراهم می کنند. گروه های غیر قطبی (هیدروژن ، متیل ، رادیکال های چرخه ای و غیره) پیوندهای آبگریزی با مواد دارویی با وزن مولکولی کم دارند.
بنابراین ، تعامل داروها با گیرنده های خاص می تواند از طریق پیوندهای مختلف شیمیایی با استحکام نابرابر حاصل شود. بنابراین ، قدرت تقریبی مواد مانند curare با گیرنده های کولینرژیک برای تعامل الکترواستاتیک (یونی) 5 کیلو کالری در مول ، مولکول یونی - 2-5 کیلوکالری در مول ، مولکول دو قطبی - 1-3 کیلو کالری در مول ، پیوندهای هیدروژن - 2-5 کیلوکالری است / اوراق قرضه mol، van der Waals - 0.5 kcal / mol ، اوراق قرضه آبگریز - 0.7 کیلو کالری در هر گروه CH 2. کاهش استحکام باند بسته به فاصله بین اتم ها برای تعامل الکترواستاتیک r-2 ، یون قطبی R-3 ، قطر دو قطبی r -4 ، پیوند هیدروژن r -4 ، پیوند ون در والس r -7 است . این نوع اتصال می تواند شکسته شود ، که برگشت پذیری عمل داروها را تضمین می کند. ماندگاری بیشتری اوراق قرضه کووالانسی است که تأثیر طولانی و غالباً برگشت ناپذیری از مواد را فراهم می کند ، به عنوان مثال داروهای ضد تومور آلکیل سازی. بیشتر داروها به صورت برگشت پذیر به گیرنده ها متصل می شوند. در این حالت ، به عنوان یک قاعده ، ماهیت این ترکیب بسیار پیچیده است: یونی ، دو قطبی-دو قطبی ، وان در وال ، هیدروفوبیک و انواع دیگر اوراق قرضه می توانند همزمان در آن شرکت کنند که این امر تا حد زیادی با توجه به ماهیت مکمل ماده و گیرنده و در نتیجه درجه همگرایی آنها بین توسط خودم
استحکام اتصال ماده به گیرنده ها با اصطلاح "میل" مشخص می شود.. موادی که بر روی گیرنده های یکسان عمل می کنند ، ممکن است میزان وابستگی متفاوتی برای آنها داشته باشد. در این حالت ، مواد با میل بیشتر می توانند موادی را با میل کمتری از ترکیب با گیرنده ها جابجا کنند. برای تعیین حالت تعادل بین گیرنده های "اشغالی" (DR) ، گیرنده های آزاد و ماده آزاد (D) ، از ثابت تفکیک (K D) استفاده می شود که با فرمول زیر تعیین می شود:
K D \u003d [D] * [R] / [DR]
لگاریتم منفی K D (pR D) نشانگر وابستگی است. برای توصیف میل ، اغلب از شاخص pD 2 استفاده می شود ، یعنی لگاریتم منفی EC 50 ، (غلظت ماده ای که در آن باعث می شود اثر 50٪ از حداکثر تأثیر داشته باشد).
تنوع پیوندهای متقابل شیمیایی و استحکام نابرابر آنها ، یا وابستگی بین لیگاندها و بیورسکتورها با ساختار پیچیده داروهایی که حاوی رادیکالهایی با واکنش پذیری متفاوت و داشتن شکل حجمی چند بعدی هستند ، و همچنین پیچیدگی فرآیندهای تعامل ، که اغلب در چند مرحله (مرحله) رخ می دهند توضیح داده شده است: تشکیل پیچیده ماده مخدر گیرنده است. گروه بندی داخل مولکولی؛ تفکیک پیچیده
بنابراین ، فقط موادی که تمایل برجسته ای برای جذب کننده گیرنده دارند می توانند اثر دارویی ایجاد کنند. شدت اثر به غلظت دارو و تعداد کل گیرنده ها بستگی دارد.
اگر مواد دارای فعالیت داخلی کافی باشند ، به آنها آگونیست می گویند. با فعالیت داخلی توانایی آگونیست ها برای ایجاد یک اثر بیولوژیکی با تغییر ترکیب گیرنده ها ، یعنی توانایی یک لیگاند برای فعال کردن گیرنده درک می شود. این پدیده به عنوان وابستگی مجتمع گیرنده آگونیست به مبدل در نظر گرفته می شود ؛ تبدیل سیگنالهای خارجی به داخلی آن را ترانسدیشن می نامند. انتقال سیگنال داخل سلولی فرایندهایی مانند انقباض الیاف ماهیچه ها ، تقسیم سلولی ، تکثیر ، تمایز و غیره را در بر می گیرد. اکنون مشخص شده است که سلول دارای بسیاری از مواد (هورمون ها ، پپتیدهای فعال زیستی ، نوکلئوتیدها ، استروئیدها ، بیوژولاتورهای با وزن کم مولکولی و غیره) است. گیرنده های خاص. در نتیجه تعامل این مواد با این گیرنده های خاص ، پیام رسان های ثانویه (واسطه ها) تشکیل می شوند که باعث ایجاد آبشار واکنشهای بیوشیمیایی می شوند.
یک مفهوم وجود دارد " آگونیست های جزئی"- مواد دارویی که در صورت اتصال به گیرنده ها ، بیشترین تأثیر را ندارند. این پدیده غیرقابل درک ظاهراً ناشی از وابستگی ناقص (کمتر) وابستگی مجتمع گیرنده مواد مخدر برای ترانسکوتر است. به عنوان مثال ، یک نالورفین آگونیست گیرنده مواد افیونی جزئی مانند آگونیست کامل این گیرنده ها مورفین عمل می کند ، اگرچه ضعیف تر از دومی است. در همان زمان ، هنگامی که با هم استفاده می شود ، نالورفین اثرات مورفین را تضعیف یا از بین می برد. به طور خاص ، اثر مهاری مرفین بر تنفس از بین می رود. ایزوپرنالین یک آگونیست واقعی است ، و پردنیزول یک آگونیست جزئی برای گیرنده های β آدرنرژیک است. طبق تئوری گیرنده ، یک آگونیست واقعی می تواند یک واکنش حداکثر را القا کند ، حتی اگر تنها با بخشی از گیرنده ها در تعامل باشد.
گیرنده های خاص ممکن است دارای محل اتصال یکسان یا متفاوت برای آگونیست ها و آنتاگونیست ها باشند. سایت های مختلف اتصال برای آگونیست های مختلف امکان پذیر است. در صورتی که آگونیست و آنتاگونیست دارای مکانهای اتصال یکسان باشند و اثر مسدود کننده آنتاگونیست بر روی گیرنده با افزایش غلظت آگونیست کاملاً از بین برود (حداکثر اثر آگونیست حاصل می شود) ، رابطه آنتاگونیست و آگونیست به عنوان آنتاگونیسم رقابتی تعیین می شود. اگر مکان های اتصال دهنده برای آگونیست و آنتاگونیست متفاوت باشند ، آنگاه رابطه بین آنها به عنوان تضاد غیر رقابتی تعریف می شود. برای توصیف آنتاگونیست ها ، اغلب از pA2 استفاده می شود (لگاریتم منفی غلظت مولر آنتاگونیست ، که در آن باید غلظت آن برای به دست آوردن اثر استاندارد آگونیست دو برابر شود).
تحت شرایط یک ارگانیسم کامل ، آگونیست ها و آنتاگونیست ها باعث ایجاد برخی از عملکردهای فیزیولوژیکی می شوند. در این حالت ، عمل آنتاگونیست ها با این واقعیت مشخص می شود که آنها از نفوذ لیگاندهای طبیعی خاص بر روی گیرنده های خاص جلوگیری می کنند (به عنوان مثال ، آنتاگونیست آتروپین M- کولینرژیک عملکرد آگونیست استیل کولین آنها را مهار می کند). تغییراتی که به طور مستقیم با تعامل مواد با گیرنده های خاص مرتبط است با این اصطلاح "واکنش دارویی اولیه ، که ممکن است سرآغاز یک سلسله واکنش ها باشد که منجر به تحریک یا مهار برخی از کارکردهای فیزیولوژیکی می شود."
تغییرات در عملکرد اندامها یا سیستم ها (به عنوان مثال ، تغییر در قدرت و دفعات انقباضات قلب ، عضله صاف اندام اعضای داخلی ، ترشح غدد ، فشار خون و غیره) ناشی از یک ماده مخدر تعیین شده است. اثرات دارویی این ماده. بنابراین ، برای گلیکوزیدهای قلبی ، واکنش دارویی اولیه مهار فعالیت حمل و نقل Na + ، K-ATPase از الیاف میوکارد است که به عنوان یک گیرنده خاص ممکن برای گلیکوزیدهای قلبی در نظر گرفته می شود. از این نظر ، ورود K + به فیبرهای عضلانی و خروج از الیاف Na + مختل شده و محتوای Ca2 در سیتوپلاسم افزایش می یابد ، که باعث تعامل اکتین و میوزین می شود. نتیجه این تغییرات افزایش ضربان قلب است که اصلی ترین اثر دارویی گلیکوزیدهای قلبی است.
قرار گرفتن در معرض طولانی مدت گیرنده های خاص در برابر آگونیست ها اغلب با کاهش حساسیت آنها همراه است. دومی ممکن است با تغییر در گیرنده ها ، کاهش تعداد (تراکم) آنها یا اختلال در فرآیندهای دنباله تحریک گیرنده ها همراه باشد. در این حالت ، اثرات دارویی آگونیستها کمتر برجسته می شوند.
بنابراین ، اثرات دارویی اکثر داروها به تأثیر آنها بر روی گیرنده های خاص مربوطه مربوط می شود.
مواد با میل زیاد به بیورسکتور و فعالیت داخلی کم آنتاگونیست یا مسدود کننده نامیده می شوند ، زیرا آنها بدون ایجاد تغییر در ترکیب بیورسکتور ، تعامل لیگاندهای آگونیست درون زا و / یا برون زا با آن را مهار می کنند. گیرنده های ثانویه یا گنگ وجود دارد که مواد دارویی به آنها متصل می شوند ، اما هیچ اثر دارویی ندارند. چنین گیرنده های "گنگ" اغلب در پروتئین ها و پلاسمای خون وجود دارند (اما در بافت ها نیز وجود دارد). اتصال با گیرنده های "بی صدا" منجر به کاهش غلظت ماده دارویی آزاد و در نتیجه کاهش اثر درمانی می شود.
بسیاری از تئوری های مدرن که در مورد مکانیسم تعامل لیگاند - گیرنده ، وضعیت گیرنده ها ، عدم تناسب بین تعداد گیرنده های اشغالی و واکنش نهایی ، تغییر در بازده انتقال سیگنال و وجود گیرنده های ذخیره و آگونیست های جزئی و غیره توضیح داده شده است ، پایه و اساس ایده های خود را در مورد مکانیسم عملکرد نمایندگان انواع مختلف تشکیل می دهد. گروه های دارویی این فعل و انفعالات به تعامل گیرنده و تعامل شیمیایی تقسیم می شوند.
مکانیسم تعامل داروها با بیورسکتور می تواند به عنوان طرح زیر ترسیم شود: هر لیگاند (ماده مخدر یا بستر فیزیولوژیکی) به یک سایت خاص در یک گیرنده خاص متصل می شود. گیرنده های فعال شده به طور مستقیم یا غیرمستقیم شار های یون (1) و / یا سایر فرآیندهای داخل سلول (ترشح یا انقباض عضله) را تنظیم می کنند یا سیستم پروتئین های نوکلئوتیدی گوانین (پروتئین های G) را فعال می کنند ، که به نوبه خود ، تقویت سیستم دوم واسطه آنزیمی را تقویت می کند. چندین واسطه دوم مختلف در سیتوپلاسم عملکرد دارند و پروتئین های مختلف هدف را فعال می کنند ، به عنوان مثال پروتئین کینازها. دومی روی بسترهای خاص عمل می کند و اثر دارویی را واسطه می کند.
از توضیحات ارائه شده می توان دریافت که مواد مخدر توسط مکانیسم های زیر انجام می شود:
- عملکردهای فیزیولوژیکی بافت (به عنوان مثال انقباضی ، ترشحی) توسط چندین گیرنده و در نتیجه لیگاند های مختلف تنظیم می شود.
- می توانید چندین مرحله واسط بین تعامل یک ماده مخدر با گیرنده و پاسخ یک بافت یا عضو ، به ویژه فعال شدن سیستم های مرتبط با واسطه دوم گیرنده ها وجود داشته باشد.
- اثربخشی مکانیسم های مسئول دنباله پاسخ محرک ، و همچنین چگالی گیرنده ها ، از بافت به بافت دیگر متفاوت است.
اثر درمانی برخی داروها به دلیل تعامل مستقیم شیمیایی آنها (غیر مرتبط با گیرنده های خاص) با ترکیبات درون زا یا سایر مکانیسم های تعامل (فشار اسمزی ، جذب) است. بنابراین برای دیورتیک های اسمزی - مانیتول ، اوره - گیرنده خاصی وجود ندارد. این مواد باعث افزایش فشار اسمزی در لوله های کلیوی می شوند ، در نتیجه جذب مجدد آب مختل می شود و دیورز افزایش می یابد. عملکرد مواد جاذب ، ادرارآورهای تشکیل دهنده اسید با گیرنده های خاص همراه نیست.
آنتی اسیدها (به عنوان مثال آلومینیوم یا هیدروکسید منیزیم) با اسید هیدروکلریک واکنش می دهند تا محصولاتی با خاصیت اسیدی ضعیف تشکیل دهند. مواد چلاتی ، به بعضی از فلزات متصل می شوند ، مجتمع های شیمیایی غیرفعال را تشکیل می دهند.
از آنجا که دانش در مورد ساختار گیرنده ها و مکانیسم تعامل دارویی احتمالی داروها در سطح سلولی عمیق تر می شود ، ایجاد هدفمند آنها امکان پذیر می شود ، همچنین توضیحی در مورد اینکه چرا مواد دارویی که در نگاه اول در ساختار آنها متفاوت است ممکن است چنین تأثیر داشته باشد. نمونه ای از چنین پدیده ای استرادیول و ترانزومر دی اتیل استیل بیسترول ، آنالوگ مصنوعی دستگاه تناسلی زن است. مولکول های ساختاری آنها متفاوت است ، اما دارای همان گروه های هیدروکسی در خواص و اندازه هستند ، به طور مشابه در فضا قرار گرفته و جهت یابی می شوند ، به همین دلیل مولکول های این مواد می توانند با یک گیرنده یکسان تعامل داشته و از نظر دارویی مشابهی داشته باشند.
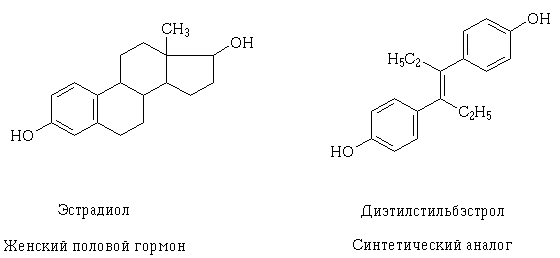
روش هایی که مواد دارویی باعث اثرات دارویی خاصی می شوند با اصطلاح "مکانیسم عمل" مشخص می شوند. این مفهوم برای توضیح اثرات داروها در سطح مولکولی ، اندام و سیستمیک استفاده می شود. به عنوان مثال ، مکانیسم عملکرد عوامل آنتی کولین استراز در سطح مولکولی با تعامل با مراکز آنیونی و استراز به محاصره استیل کولین استراز کاهش می یابد. در عین حال ، توضیح مکانیسم اثر فشار خون داروهای آنتی کولین استراز ، برادی کاردی و عروق زدایی به عنوان علت این اثر ذکر شده است ، یعنی آنها مکانیسم این اثر را در سطح اندام در نظر می گیرند.
مطالعات در مورد مکانیسم های عملکرد داروها در حال انجام است و ایده های مربوط به مکانیسم عملکرد یک ماده مخدر با به دست آوردن داده های جدید نه تنها می تواند دقیق تر شود بلکه تغییر قابل توجهی نیز می یابد.