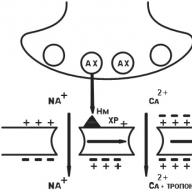
برخی داروها فعالیت آنزیمهای خاص (داخل سلولی یا خارج سلولی) را تقویت یا مهار می کنند. نقش اصلی در حصول اطمینان از عملکرد سلول ها توسط سیستم جهانی آدنیلات سیكلاز سلول ها ایفا می كند و تأثیر بسیاری از داروها با فعالیت آنزیم های آدنیلات سیكلاز یا فسفودی استراز تنظیم می شود كه غلظت غلظت آدنوزین مونوفسفات حلقوی داخل سلولی (cAMP) را تنظیم می كنند.
داروها می توانند آنزیم ها را تحریک یا مهار کنند ، با آنها در درجات مختلف ، برگشت پذیر یا برگشت ناپذیر ، در تعامل با آنها باشند ، که بر شدت و مدت اثر دارویی تأثیر می گذارد.
اثرات فیزیکی و شیمیایی داروها بر روی غشای سلولی
تأثیر فیزیکوشیمیایی روی غشای سلولی ، تغییر در پتانسیل الکتریکی ترانسمبرون به عنوان یک نتیجه از تأثیر در انتقال یونها از طریق غشای سلولی است. این برای فعالیت سلولهای سیستم عصبی و عضلانی بسیار مهم است: انجام تکانه های عصبی از طریق سیناپسها مختل می شود و فعالیت الکتریکی سلول ها سرکوب می شود.
بنابراین ، داروهای ضد آریتمی ، ضد تشنج ، عوامل بیهوشی عمومی و بی حسی موضعی عمل می کنند.
اثرات شیمیایی مستقیم (سمیت سلولی) داروها
داروها می توانند به طور مستقیم با مولکولها یا ساختارهای درون سلولی کوچک ارتباط برقرار کنند و منجر به اختلال در فعالیت سلول شود.
داروهای ضد باکتریایی ، داروهای ضد ویروسی و سیتوستاتیک اثر مشابهی دارند.
اثر داروها ممکن است با تغییر در عملکرد سلول همراه نباشد (به عنوان مثال ، خنثی کردن اسید هیدروکلریک با آنتی اسیدها یا اثر مسهل های روغنی).
انتخاب مواد مخدر
گزینش عملکرد داروها از طریق توزیع و تجمع مختلف داروها در اندام ها ، بافت ها ، سلول ها و انتخاب مکانیسم عمل آنها حاصل می شود.
گزینشی ، توانایی انجام اثر مطلوب خاص است و به دلیل تأثیرگذاری بر انواع مختلف یا زیرگروه های گیرنده ، باعث ایجاد اثرات نامطلوب دیگر نمی شود. به عنوان مثال ، داروهای مسدود کننده β- آدرنرژیک (metoprolol ، atenolol) ، آنتاگونیست های گیرنده سروتونین (ketanserin) بر روی یک زیرگروه خاص از گیرنده های مربوطه عمل می کنند ، اما انتخاب اینگونه داروها اغلب نسبی است و با افزایش دوز همان عوامل مسدود کننده بتا-آدرنرژیک ، تا حدی از بین می رود. روش دیگر برای اطمینان از انتخاب نسبی عملکرد دارو ، استفاده انتخابی از LF مربوطه در محل اثر مورد نظر (به عنوان مثال ، تجویز داخل رحمی نیتروگلیسیرین در بیماران مبتلا به بیماری عروق کرونر) است.
هیچ دارویی که به صورت انتخابی روی یک گیرنده ، اندام و یا یک فرآیند آسیب شناختی خاص عمل کند ، وجود ندارد. هرچه انتخاب دارو بیشتر باشد ، موثرتر است.
داروهایی با انتخاب کم عمل روی بسیاری از بافت ها ، اندام ها و سیستم ها اثر می گذارند و باعث ایجاد عوارض جانبی زیادی می شوند. هر دارویی طیف کمابیش وسیعی از فعالیت دارد و می تواند تعدادی از واکنش های مطلوب یا نامطلوب را ایجاد کند.
به عنوان مثال ، مورفین که دارای فعالیت ضد درد حاد است ، به گروه داروهای ضد درد مواد مخدر تعلق دارد. با این حال ، تنفس را کاهش می دهد ، رفلکس سرفه را سرکوب می کند ، دارای خاصیت آرام بخش است ، باعث استفراغ ، یبوست ، برونکواسپاسم ، ترشح هیستامین ، دارای خاصیت ضد ادراری و غیره است.
عوامل ضد پستان ، با عمل به سلولهای سریع تقسیم شده ، نه تنها به بافت تومور بلکه به مغز استخوان ، اپیتلیوم روده نیز آسیب می رسانند و باعث تحریک واکنشهای جانبی شدید می شوند.
هرچه میزان انتخاب داروها بیشتر باشد ، تحمل بهتر بیماران و تعداد عوارض جانبی ناشی از آن نیز کمتر خواهد بود.
به عنوان نمونه می توان از انسداد گیرنده های H2 نسل سوم ، مسدود کننده های کولینرژیک M1 و مهار کننده های H + ، K + -ATPase استفاده کرد.
انتخاب دارو به میزان مصرف آن بستگی دارد. هرچه این دارو بیشتر باشد ، داروی انتخابی کمتری دارد.
بنابراین ، مسدود کننده های انتخابی β 1-آدرنرژیک بطور عمده بر میوکارد تأثیر می گذارند ، اما با افزایش دوز ، آنها همچنین بر گیرنده های β 2-آدرنرژیک واقع در برونش ها ، رگ های خونی ، لوزالمعده و اندام های دیگر تأثیر می گذارند و منجر به ایجاد واکنش های نامطلوب می شوند (برونکواسپاسم ، انقباض عروق).
انتخاب عملکرد داروهای ضد ویروسی ، مانند آسیکلوویر نیز به دوز بستگی دارد: سرکوب DNA پلیمراز ویروسی در غلظت دارو 3000 برابر کمتر از آنهایی که روی DNA پلیمراز سلولهای انسانی تأثیر می گذارند ، بنابراین ، آسیکلوویر در دوزهای درمانی غیر سمی است.
5- عملكرد موضعي و انعطاف پذيري داروها. فعالیت مستقیم و انعکاس پذیر. محلی سازی و مکانیسم عمل. اهداف داروها. عمل برگشت پذیر و برگشت ناپذیر. اکشن انتخابی
5- عملكرد موضعي و انعطاف پذيري داروها. فعالیت مستقیم و انعکاس پذیر. محلی سازی و مکانیسم عمل. اهداف داروها. عمل برگشت پذیر و برگشت ناپذیر. اکشن انتخابی
عمل ماده ای که در محل کاربرد آن اتفاق می افتد موضعی نامیده می شود. به عنوان مثال ، عوامل پاکت نامه غشای مخاطی را می پوشانند و از تحریک انتهای اعصاب آوران جلوگیری می کنند. با بی حسی سطحی ، استفاده از بی حسی موضعی به غشای مخاط منجر به بلوک انتهای اعصاب حسی فقط در محل استفاده دارو می شود. با این حال ، یک اثر محلی واقعی بسیار نادر است ، زیرا مواد می توانند تا حدی جذب شوند و یا تحت فشار قرار گیرند اثر رفلکس.
عمل ماده ای که پس از جذب آن ، ورود به جریان خون عمومی و سپس به بافت ایجاد می شود ، انعطاف پذیر نامیده می شود. عمل انحطاط
1 از انگلیسی ترخیص- تمیز کردن
2 از لات. resorbeo- جذب می کنم.
اثر بستگی به مسیر مصرف دارد داروها و توانایی آنها برای عبور از موانع بیولوژیکی
با عمل موضعی و تحریک کننده ، داروها یا اثر مستقیمی دارند و یا یک رفلکس دارند. اولین مورد در محل تماس مستقیم ماده با بافت تحقق می یابد. با اثر رفلکس یک ماده ، اگزروئلها یا رهگیرها بر اثر تأثیر می گذارند و با تغییر در وضعیت مراکز عصبی مربوطه یا دستگاههای اجرایی ، این اثر را نشان می دهد. بنابراین ، استفاده از خردل در آسیب شناسی سیستم تنفسی به طور انعطاف پذیر باعث بهبود غنائم آنها می شود (روغن خردل اساسی باعث تحریک کننده های بیرون کشنده های پوستی می شود). لوبلین دارویی که به صورت داخل وریدی تجویز می شود ، تأثیر مهیبی در شیمی گیرنده گلومرول کاروتید دارد و با تحریک منعکس کننده مرکز تنفس ، باعث افزایش حجم و دفعات تنفس می شود.
وظیفه اصلی فارماکودینامیک این است که دریابیم که داروها در کجا و چگونه عمل می کنند و باعث اثرات خاصی می شوند. با تشکر از بهبود تکنیک های روش شناختی ، این مسائل نه تنها در سطح سیستمیک و اندام بلکه در سطح سلولی ، درون سلولی ، مولکولی و زیر مولکولی برطرف می شوند. بنابراین ، برای داروهای عصبی ، آن ساختارهای سیستم عصبی ایجاد شده اند که سازندهای سیناپسی دارای بیشترین حساسیت به این ترکیبات هستند. برای موادی که روی متابولیسم تأثیر می گذارند ، بومی سازی آنزیم ها در بافت ها ، سلول ها و سازندهای درون سلولی مختلف تعیین می شود ، فعالیت آنها بویژه قابل توجهی تغییر می کند. در همه موارد ، ما در مورد آن بسترهای بیولوژیکی ، "اهداف" که دارو با آنها تداخل دارد صحبت می کنیم.
گیرنده ها ، کانال های یونی ، آنزیم ها ، سیستم های حمل و نقل و ژن ها به عنوان "اهداف" برای داروها عمل می کنند.
گیرنده ها گروههای فعال ماکرومولکولهای بسترهایی هستند که یک ماده با آنها در ارتباط است. گیرنده هایی که تظاهرات عملکرد مواد را فراهم می کنند ، خوانده می شوند خاص
4 نوع گیرنده زیر مشخص می شوند (شکل.
I. گیرنده هایی که به طور مستقیم عملکرد کانال های یونی را کنترل می کنند. این نوع گیرنده به طور مستقیم با کانالهای یونی همراه است شامل گیرنده های n-کولینرژیک ، گیرنده های GABA A و گیرنده های گلوتامات.
دوم گیرنده ها از طریق فرستنده های G-پروتئین های ثانویه یا سیستم کانال های یونی پروتئین های یونی به یک مؤثر تبدیل می شوند. چنین گیرنده هایی برای بسیاری از هورمون ها و واسطه ها (گیرنده های کولینرژیک m ، گیرنده های آدرنرژیک) در دسترس هستند.
III. گیرنده هایی که به طور مستقیم عملکرد آنزیم کارآمد را کنترل می کنند. آنها به طور مستقیم با تیروزین کیناز در ارتباط هستند و فسفوریلاسیون پروتئین را تنظیم می کنند. براساس این اصل ، گیرنده های انسولین ، تعدادی از فاکتورهای رشد چیده شده اند.
چهارم گیرنده هایی که رونویسی DNA را کنترل می کنند. بر خلاف گیرنده های غشایی از نوع I-III ، این گیرنده های داخل سلول (پروتئین محلول سیتوزولی یا هسته ای) هستند. هورمونهای استروئیدی و تیروئید با چنین گیرنده هایی در تعامل هستند.
مطالعه زیرگروه های گیرنده (جدول II.1) و اثرات مرتبط با آن بسیار مثمر ثمر بوده است. از نخستین مطالعات از این نوع ، کار روی سنتز بسیاری از مسدود کننده های بتا بود که به طور گسترده در بیماری های مختلف سیستم قلبی عروقی مورد استفاده قرار می گیرند. سپس ، مسدود کننده های گیرنده هیستامین H2 ، در درمان زخم معده و زخم اثنی عشر مؤثر بودند. پس از آن ، سنتز شد
شکلاصول عمل آگونیست ها در فرآیندهای کنترل شده توسط گیرنده ها.
من - تأثیر مستقیمی بر نفوذپذیری کانال های یونی (گیرنده های کولینرژیک ، گیرنده های GABA A). دوم - تأثیر غیرمستقیم (از طریق پروتئین G) بر نفوذپذیری کانالهای یونی یا فعالیت آنزیم هایی که تنظیم کننده فرستنده های ثانویه (گیرنده های مایع کولینرژیک ، گیرنده های آدرنرژیک) را تنظیم می کنند. III - تأثیر مستقیمی بر فعالیت آنزیم مؤثر تیروزین کیناز (گیرنده های انسولین ، گیرنده های تعدادی از فاکتورهای رشد). چهارم - تأثیر بر رونویسی DNA (هورمونهای استروئیدی ، هورمونهای تیروئید).
اما بسیاری از داروهای دیگر که روی گروه های مختلف گیرنده های α-آدرنرژیک ، دوپامین ، گیرنده های مواد افیونی و غیره فعالیت می کنند ، این مطالعات نقش مهمی در ایجاد گروه های جدید داروهای دارای عملکرد انتخابی دارند که در پزشکی استفاده می شوند.
با توجه به تأثیر مواد بر روی گیرنده های پس سیناپسی ، باید به احتمال اتصال آلوستریک به مواد درون زا (مثلاً گلیسین) و اگزوژن (به عنوان مثال آنژیولیتیک های سری بنزودیازپین) توجه کنید ؛ به فصل 11.4 ، شکل 11.3) مبدا مراجعه کنید. تعامل Allosteric 1 با گیرنده باعث ایجاد "سیگنال" نمی شود. با این حال ، مدولاسیون اثر اصلی واسطه وجود دارد ، که هم می تواند افزایش یابد و هم کاهش یابد. ایجاد مواد از این نوع امکانات جدیدی را برای تنظیم عملکرد سیستم عصبی مرکزی باز می کند. یکی از ویژگیهای عصب دهنده های عملکرد آلوستریک این است که آنها مستقیماً در انتقال واسطه اصلی تأثیر نمی گذارند بلکه فقط آن را در جهت دلخواه اصلاح می کنند.
نقش مهمی در درک مکانیسم های تنظیم انتقال سیناپسی با کشف گیرنده های پیش سیناپسی (جدول II.2) ایفا کرده است. راه های اتوروگلایز هموتروپیک (عمل واسطه ترشح کننده بر روی گیرنده های پیش سیناپسی همان انتهای عصب) و تنظیم هتروتروپی (تنظیم پیش سیناپسی به دلیل واسطه دیگر) رهاسازی واسطه ها مورد بررسی قرار گرفت که باعث می شود دوباره ویژگی های عملکرد بسیاری از مواد مورد بررسی قرار گیرد. این اطلاعات همچنین به عنوان مبنای جستجوی هدفمند برای تعدادی از داروها (به عنوان مثال پرازوسین) قرار گرفت.
1 از یونانی همه چیز- متفاوت ، متفاوت ، استریوها- مکانی.
جدول II.1نمونه هایی از گیرنده ها و زیرگروه های آنها

وابستگی یک ماده به گیرنده ، که منجر به تشکیل مجتمع "گیرنده ماده" با آن می شود ، با اصطلاح "میل" 1 بیان می شود. توانایی یک ماده در تعامل با گیرنده برای تحریک آن و ایجاد یک اثر خاص ، فعالیت داخلی نامیده می شود.
1 از لات. affinis- مهربانی
موادی که هنگام تعامل با گیرنده های خاص ، باعث ایجاد تغییراتی در آنها می شوند که منجر به اثر بیولوژیکی می شوند ، آگونیست 1 نامیده می شوند (آنها همچنین فعالیت درونی دارند). اثر تحریک کننده آگونیست بر روی گیرنده ها می تواند منجر به فعال یا مهار عملکرد سلول شود. اگر تعامل آگونیست با گیرنده ها باعث حداکثر اثر شود ، به آن آگونیست کامل گفته می شود. در مقابل با دومی ، آگونیستهای جزئی که در تعامل با همان گیرنده ها هستند ، بیشترین تأثیر را ندارند. ماده هایی که به گیرنده ها متصل شده و آنها را تحریک نمی کنند ، آنتاگونیست 2 نامیده می شوند. آنها هیچ فعالیت درونی ندارند (برابر با 0). اثرات دارویی آنها ناشی از تضاد با لیگاند های درون زا (واسطه ها ، هورمون ها) و همچنین با مواد آگونیست اگزوژن است. اگر آنها همان گیرنده هایی را که آگونیست ها با آنها ارتباط برقرار می کنند ، اشغال می کنند ، پس ما در مورد آن صحبت می کنیم آنتاگونیست های رقابتیاگر - سایر قسمتهای ماکرومولکول که مربوط به گیرنده خاصی نیستند ، اما با آن بهم وصل هستند ، سپس - آنتاگونیست های غیر رقابتی.هنگامی که یک ماده به عنوان آگونیست در یک زیرگروه گیرنده ها و به عنوان آنتاگونیست بر روی ماده دیگر عمل می کند ، یک آگونیست آنتاگونیست تعیین می شود. به عنوان مثال ، پنتازوسین ضد درد یک آنتاگونیست μ و آگونیست گیرنده های مواد مخدر δ و κ مخدر است.
تعامل "گیرنده ماده" به دلیل اوراق قرضه بین مولکولی انجام می شود. یکی از ماندگارترین اوراق قرضه کووالانسی است. برای تعداد کمی از داروها (α-مسدود کننده فنوکسی بنزامین ، برخی از داروهای ضد انفجار) شناخته شده است. کمتر پایدار است پیوند یونی گسترده به دلیل تعامل الکترواستاتیک مواد با گیرنده ها. حالت دوم برای مسدود کننده های گانگلیونی ، عوامل کوراری فرم ، استیل کولین معمولی است. نقش مهمی توسط نیروهای Van van Waals که پایه و اساس برهم کنش های آبگریزی و همچنین پیوندهای هیدروژن هستند تشکیل می شود (جدول II.3).
جدول II.3.انواع تعامل مواد با گیرنده ها

1 این به تعامل مولکولهای غیر قطبی در یک محیط آبی اشاره دارد. * 0.7 کیلو کالری (3 کیلو گرم) در هر گروه CH 2.
بسته به قدرت پیوند "گیرنده ماده" ، یک عمل برگشت پذیر (مشخصه بیشتر مواد) و برگشت ناپذیر (معمولاً در مورد پیوند کووالانسی) از هم متمایز می شوند.
1 از یونانی آگونیست ها- رقیب (آگون- مبارزه)
2 از یونانی آنتاگونیسم- مبارزه ، رقابت (ضد- در برابر چشمه- مبارزه)
اگر یک ماده فقط با گیرنده های منحصر به فرد عملکردی از یک بومی سازی خاص در تعامل باشد و بر گیرنده های دیگر تأثیر نگذارد ، عمل چنین ماده ای انتخابی تلقی می شود. بنابراین ، برخی از عوامل شبیه به شکل بصورت کاملا انتخابی گیرنده های کولینرژیک صفحه انتهایی را مسدود می کنند و باعث آرامش عضلات اسکلتی می شوند. در دوزهایی که اثر میوپارالتیک دارند ، تأثیر کمی روی سایر گیرنده ها دارند.
مبنای انتخابی بودن عمل ، میل (میل) ماده به گیرنده است. این به دلیل وجود برخی از گروههای کاربردی خاص ، و نیز سازماندهی کلی ساختار ماده ای است که برای تعامل با این گیرنده ، مناسب ترین است ، یعنی مکمل آنها غالباً اصطلاح "عمل انتخابی" با دلیل خوب با اصطلاح "عمل ترجیحی" جایگزین می شود ، زیرا انتخاب مطلق عمل مواد عملاً وجود ندارد.
هنگام ارزیابی اثر متقابل مواد با گیرنده های غشایی که یک سیگنال را از سطح بیرونی غشا به داخل منتقل می کنند ، همچنین باید آن پیوندهای واسطه ای را که اتصال گیرنده به مؤثر است ، در نظر گرفت. مهمترین مؤلفه های این سیستم پروتئینهای G 1 ، گروهی از آنزیم ها (آدنیلات سیكلاز ، گوانلات سیكلاز ، فسفولیپاز C) و فرستنده های ثانویه (cAMP ، cGMP ، IF 3 ، DAG ، Ca 2+) هستند. افزایش در شکل گیری فرستنده ثانویه منجر به فعال شدن پروتئین کینازها می شود که فسفوریلاسیون داخل سلولی پروتئین های مهم نظارتی و ایجاد اثرات مختلف را فراهم می کنند.
اکثر پیوندهای موجود در این آبشار پیچیده می تواند نقطه ای از کاربرد مواد دارویی باشد. با این حال ، چنین نمونه هایی هنوز هم کاملاً محدود هستند. بنابراین ، در رابطه با پروتئین های G ، فقط سموم شناخته شده هستند که به آنها پیوند می خورند. با گرمs پروتئین پروتئین سم وبروریو وبا با G و تعاملمن -protein - سم چوبهای سیاه پوست.
مواد جداگانه ای وجود دارد که به طور مستقیم بر آنزیم های دخیل در تنظیم بیوسنتز فرستنده ثانویه تأثیر می گذارد. بنابراین ، diterpen با منشأ گیاه فورسکولین ، که در مطالعات تجربی مورد استفاده قرار می گیرد ، باعث تحریک آدنیلات سیکلاز (اثر مستقیم) می شود. فسفودی استراز مهار متیل اکسانتین ها را مهار می کند. در هر دو مورد ، غلظت cAMP در داخل سلول افزایش می یابد.
یكی از مهمترین اهداف برای عملكرد مواد کانال های یونی است. پیشرفت در این زمینه تا حد زیادی با توسعه روش هایی برای ضبط عملکرد کانال های یونی منفرد همراه است. این نه تنها تحقیقات اساسی در مورد سینتیک فرآیندهای یونی را تحریک می کند ، بلکه به ایجاد داروهای جدید که جریان های یونی را تنظیم می کنند نیز کمک کرده است (جدول II.4).
در اواسط قرن بیستم ، مشخص شد که بی حسی موضعی کانال های Na + وابسته به پتانسیل را مسدود می کند. مسدود کننده کانال های Na + شامل بسیاری از داروهای ضد آریتمی است. علاوه بر این ، نشان داده شد که تعدادی از داروهای ضد صرع (دی فنین ، کاربامازپین) نیز کانالهای وابسته به پتانسیل سدیم را مسدود می کنند و فعالیت ضد تشنجی آنها ظاهراً با این موضوع همراه است.
1 انواع پروتئین های G و عملکرد آنها: G S - ترکیب گیرنده های تحریکی با آدنیلات سیکلاز. G i - ترکیب گیرنده های بازدارنده با آدنیلات سیکلاز؛ G o - ترکیب سلولهای گیرنده با کانالهای یونی (کاهش Ca2 فعلی). جق- ترکیبات گیرنده هایی که فسفولیپاز C را فعال می کنند. پروتئین های G از 3 زیر واحد - α ، β و γ تشکیل شده است.
جدول II.4.به معنی مؤثر در کانال های یونی است

در 30-40 سال گذشته ، توجه زیادی به مسدود کننده های کانال Ca 2+ شده است ، که ورود یون های Ca 2+ به سلول را از طریق کانال های Ca2 وابسته به ولتاژ مختل می کند. افزایش علاقه به این گروه از مواد تا حد زیادی به این دلیل است که یون های Ca 2+ در بسیاری از فرآیندهای فیزیولوژیکی شرکت می کنند: انقباض عضلات ، فعالیت ترشحی سلول ها ، انتقال عصبی عضلانی ، عملکرد پلاکت و غیره.
بسیاری از داروهای این گروه در معالجه بیماریهای شایع مانند آنژین صدری ، آریتمی قلبی و فشار خون شریانی بسیار مؤثر بوده اند. داروهای گسترده ای مانند وراپامیل ، دیلتیازم ، فنیگیدین و بسیاری دیگر شناخته شده است.
فعال کننده های کانال های Ca2 ، به عنوان مثال ، مشتقات دی هیدروپیریدین نیز توجه را به خود جلب می کنند. از چنین موادی می توان به عنوان کاردیوتونیک ، عوامل تشدید کننده عروق ، موادی که باعث تحریک ترشح هورمون ها و واسطه ها و همچنین محرک های سیستم عصبی مرکزی می شوند ، استفاده کرد.
مورد توجه ویژه جستجوی مسدود کننده ها و فعال کننده های کانال های Ca 2+ با تأثیر غالب بر قلب ، رگ های خونی مناطق مختلف (مغز ، قلب و ...) ، سیستم عصبی مرکزی است. مقدمات خاصی برای این امر وجود دارد ، از آنجا که کانال های Ca 2 ناهمگن هستند.
در سال های اخیر ، موادی که عملکرد کانال های K + را تنظیم می کنند ، مورد توجه بسیاری قرار گرفته اند. نشان داده شده است که کانال های پتاسیم از نظر ویژگی های عملکردی بسیار متنوع هستند. از یک سو ، این به طور قابل توجهی مطالعات دارویی را پیچیده می کند ، و از سوی دیگر ، پیش نیازهای واقعی برای جستجوی مواد فعال انتخابی را ایجاد می کند. هر دو فعال کننده و مسدود کننده کانال پتاسیم شناخته شده است.
فعال کننده های کانال های پتاسیم در باز و آزاد سازی یون های K از سلول نقش دارند. اگر این اتفاق در عضلات صاف رخ دهد ، بیش از حد قطر غشاء ایجاد می شود و تن ماهیچه ها کاهش می یابد. با تشکر از این مکانیسم از ماینوکسیدیل و دیازوکسید به عنوان داروهای ضد فشار خون و همچنین داروی آنتی نینال نیکوراندیل استفاده می شود.
مسدود کننده های کانال پتاسیم به عنوان داروهای ضد آریتمی (آمیودارون ، اورنید ، سوتولول) مورد توجه هستند.
مسدود کننده کانال های پتاسیم وابسته به ATP در لوزالمعده ترشح انسولین را افزایش می دهد. براساس این اصل ، داروهای ضد دیابتی از گروه سولفونیل اوره (کلروپروپامید ، بوتامید و غیره) عمل می کنند.
اثر تحریک آمینوپیریدین ها در سیستم عصبی مرکزی و انتقال عصبی عضلانی نیز با اثر انسداد آنها در مجاری پتاسیم همراه است.
بنابراین ، قرار گرفتن در معرض کانال های یونی اثرات داروهای مختلف را تحت تأثیر قرار می دهد.
یک "هدف" مهم برای عملکرد مواد آنزیم ها هستند. احتمال قرار گرفتن در معرض آنزیم هایی که تشکیل دهنده فرستنده های ثانویه را تنظیم می کنند (به عنوان مثال ، اردوگاه) قبلاً ذکر شده است. مشخص شده است که مکانیسم عملکرد داروهای ضد التهابی غیر استروئیدی به دلیل مهار سیکلواکسیژناز و کاهش بیوسنتز پروستاگلاندین است. مهار کننده های آنزیم تبدیل کننده آنژیوتانسین (کاپتوپریل و دیگران) به عنوان داروهای ضد فشار خون استفاده می شوند. داروهای آنتی کولین استراز که استیل کولین استراز را مسدود کرده و استیل کولین را تثبیت می کند ، به خوبی شناخته شده است.
ماده ضد انفجار متوترکسات (یک آنتاگونیست اسید فولیک) دی هیدروفولات ردوکتاز را مسدود می کند و از تشکیل تتراهیدروفولات جلوگیری می کند ، که برای سنتز نوکلئوتید پورین ، تیمیدیلات لازم است. داروی ضد میکروبی acyclovir ، با تبدیل شدن به آسیکلوویر تری فسفات ، DNA پلیمراز ویروسی را مهار می کند.
یکی دیگر از اهداف "هدف" برای اقدام به داروها سیستمهای حمل و نقل برای مولکولهای قطبی ، یونها و مولکولهای آبگریزی کوچک است. این شامل پروتئین های به اصطلاح حمل و نقل است که مواد را در غشای سلولی حمل می کنند. آنها سایتهای شناسایی مواد درون زا دارند. این سایت ها می توانند با داروها در تعامل باشند. بنابراین ، داروهای ضد افسردگی سه حلقه ای ، جذب عصبی نوراپی نفرین را مسدود می کنند. رزرپین رسوب نوراپی نفرین را در وزیکولها مسدود می کند. از جمله دستاوردهای قابل توجه ایجاد مهارکننده های پمپ پروتون در مخاط معده (امپرازول و غیره) است که به نظر می رسد در زخمهای معده و اثنی عشر و همچنین در معده هایپراسید بسیار مؤثر است.
اخیراً ، در رابطه با رمزگشایی ژنوم انسانی ، مطالعات گسترده ای در رابطه با استفاده به عنوان هدف انجام شده است ژنهاشکی نیست که ژن درمانییکی از مهمترین زمینه های داروسازی مدرن و آینده است. ایده چنین درمانی تنظیم عملکرد ژنهایی است که نقش اتیوپاتوژنتیک آنها به اثبات رسیده است. اصول اساسی ژن درمانی افزایش ، کاهش یا خاموش کردن بیان ژن و همچنین جایگزینی یک ژن جهش یافته است.
راه حل این مشکلات به لطف توانایی کلون کردن زنجیره ها با یک توالی نوکلئوتیدی مشخص ، واقعی شد. معرفی چنین زنجیره های اصلاح شده با هدف عادی سازی سنتز پروتئین هایی که این آسیب شناسی را تعیین می کنند ، و بر این اساس ، در بازگرداندن عملکرد سلول های مختل شده انجام می شود.
یک مشکل اصلی در موفقیت آمیز ژن درمانی تحویل اسیدهای نوکلئیک به سلولهای هدف است. اسیدهای نوکلئیک باید از فضاهای خارج سلولی وارد پلاسما شوند و سپس با عبور از غشاهای سلولی ، به هسته نفوذ کنند و در کروموزومها وارد شوند. پیشنهاد می شود از برخی ویروس ها (به عنوان مثال ، ویروس ویروس ، آدنوویروس) به عنوان حمل کننده یا بردار استفاده شود. علاوه بر این ، با کمک مهندسی ژنتیک ، ویروس های بردار توانایی تکثیر خود را از دست می دهند ، یعنی. هیچ ویروسی از آنها تشکیل نمی شود. سیستم های حمل و نقل دیگر پیشنهاد شده اند - مجتمع های DNA با لیپوزوم ها ، پروتئین ها ، DNA پلاسمید و سایر ریزگردها و میکروسفرها.
به طور طبیعی ، ژن گنجانیده شده باید برای مدت زمان كافی عمل كند ، یعنی. بیان ژن باید پایدار باشد.
ژن درمانی بالقوه مربوط به بسیاری از بیماریهای ارثی است. اینها شامل حالات نقص ایمنی ، برخی از انواع آسیب شناسی کبد (از جمله هموفیلی) ، هموگلوبینوپاتی ، بیماری های ریه (به عنوان مثال فیبروز کیستیک) ، بافت ماهیچه ای (دیستروفی عضلانی دوشن) و غیره است.
تحقیقات در یک جبهه وسیع در حال انجام است تا روش های احتمالی استفاده از ژن درمانی برای درمان بیماری های تومور روشن شود. این امکانات برای جلوگیری از بیان پروتئینهای انکوژن است. در فعال سازی ژنهایی که قادر به مهار رشد تومور هستند. در تحریک تشکیل آنزیم های ویژه در تومورهایی که باعث می شوند مواد منفجره را به ترکیبات سمی تبدیل کنند فقط به سلولهای تومور افزایش مقاومت سلولهای مغز استخوان به اثر مهاری عوامل ضد بلاستوما. تقویت ایمنی در برابر سلولهای سرطانی و غیره
در مواردی که مسدود کردن بیان ژنهای خاص ضروری می شود ، از فناوری ویژه ای به اصطلاح الیگونونوکلئوتیدها به اصطلاح antisense (ضد حساس) استفاده می شود. دومی زنجیره های نسبتاً کوتاهی از نوکلئوتیدها (از 15-25 پایه) هستند که مکمل منطقه اسید نوکلئیک که ژن هدف در آن قرار دارد ، مکمل هستند. در نتیجه تعامل با الیگونوکلئوتید ضد حساس ، بیان این ژن سرکوب می شود. این اصل عمل در درمان بیماری های ویروسی ، توموری و سایر بیماری ها مورد توجه است. اولین داروی گروه نوکلئوتیدهای ضد حساس ، Vitraven (fomivirsen) ، بصورت موضعی برای رتینیت ناشی از عفونت سیتومگالوویروس استفاده می شود. به نظر می رسد این نوع دارو برای درمان لوسمی میلوئیدی و سایر بیماری های خونی است. آنها تحت آزمایشات بالینی قرار دارند.
در حال حاضر ، مشکل استفاده از ژن ها به عنوان اهداف برای اثرات دارویی عمدتاً در مرحله تحقیقات اساسی است. فقط چند ماده امیدوارکننده از این نوع ، آزمایشات بالینی اولیه و بالینی را انجام می دهند. با این حال ، شکی نیست که در این قرن بسیاری از ابزارهای مؤثر برای ژن درمانی نه تنها ارثی ، بلکه بیماریهای اکتسابی نیز ظاهر می شوند. این داروها اساساً جدید برای درمان تومورها ، بیماریهای ویروسی ، حالات نقص سیستم ایمنی ، خونریزی و اختلالات انعقاد خون ، آترواسکلروز و غیره خواهند بود.
ارسال کار خوب خود به پایگاه دانش آسان است. از فرم زیر استفاده کنید
دانشجویان ، دانشجویان فارغ التحصیل ، دانشمندان جوانی که از پایگاه دانش در مطالعات و کار خود استفاده می کنند از شما بسیار سپاسگزار خواهند بود.
ارسال شده در http://www.allbest.ru/
GOU VPO "آکادمی پزشکی دولتی نیژنی نووگورود وزارت بهداشت ، درمان و توسعه اجتماعی فدراسیون روسیه"
گروه داروسازی عمومی و کلینیکی
عمل مواد مخدر
1. اثرات موضعی و تحریک کننده داروها
عمل ماده ای که در محل کاربرد آن اتفاق می افتد موضعی نامیده می شود. به عنوان مثال ، عوامل پاکت نامه غشای مخاطی را می پوشانند و از تحریک انتهای اعصاب آوران جلوگیری می کنند. با بی حسی سطحی ، استفاده از بی حسی موضعی به غشای مخاط منجر به بلوک انتهای اعصاب حسی فقط در محل استفاده دارو می شود. با این حال ، یک اثر محلی واقعی بسیار نادر است ، از آنجا که مواد می توانند تا حدی جذب شوند یا اثر بازتابی داشته باشند.
عمل ماده ای که پس از جذب آن ، ورود به جریان خون عمومی و سپس به بافت ایجاد می شود ، انعطاف پذیر نامیده می شود. اثر جاذب بستگی به مسیر مصرف داروها و توانایی نفوذ آنها در موانع بیولوژیکی دارد.
2. عمل مستقیم و رفلکس
با عمل موضعی و تحریک کننده ، داروها یا اثر مستقیمی دارند و یا یک رفلکس دارند. اولین مورد در محل تماس مستقیم ماده با بافت تحقق می یابد. با تأثیر رفلکس ، مواد بر روی ادرار یا مهارکننده ها اثر می گذارند و اثر با تغییر وضعیت مراکز عصبی مربوطه یا ارگان های اجرایی آشکار می شود. بنابراین ، استفاده از خردل در آسیب شناسی سیستم تنفسی به طور انعطاف پذیر باعث بهبود غنائم آنها می شود (روغن خردل اساسی باعث تحریک کننده های بیرون کشنده های پوستی می شود). لوبلین دارویی که به صورت داخل وریدی تجویز می شود ، تأثیر مهیبی در شیمی گیرنده گلومرول کاروتید دارد و با تحریک منعکس کننده مرکز تنفس ، باعث افزایش حجم و دفعات تنفس می شود.
فارماکودینامیک دارویی انتخابی برگشت پذیر
3. بومی سازی و مکانیسم عمل
وظیفه اصلی فارماکودینامیک این است که دریابیم که داروها در کجا و چگونه عمل می کنند و باعث اثرات خاصی می شوند. با تشکر از بهبود تکنیک های روش شناختی ، این مسائل نه تنها در سطح سیستمیک و اندام بلکه در سطح سلولی ، درون سلولی ، مولکولی و زیر مولکولی برطرف می شوند. بنابراین ، برای داروهای عصبی ، آن ساختارهای سیستم عصبی ایجاد شده اند که سازندهای سیناپسی دارای بیشترین حساسیت به این ترکیبات هستند. برای موادی که روی متابولیسم تأثیر می گذارند ، بومی سازی آنزیم ها در بافت ها ، سلول ها و سازندهای درون سلولی مختلف تعیین می شود ، فعالیت آنها بویژه قابل توجهی تغییر می کند. در همه موارد ، ما در مورد آن بسترهای بیولوژیکی ، "اهداف" که دارو با آنها تداخل دارد صحبت می کنیم.
4. "اهداف" برای مواد مخدر
گیرنده ها ، کانال های یونی ، آنزیم ها ، سیستم های حمل و نقل و ژن ها به عنوان "اهداف" برای داروها عمل می کنند.
گیرنده ها گروههای فعال ماکرومولکولهای بسترهایی هستند که یک ماده با آنها در ارتباط است. گیرنده هایی که تظاهرات عملکرد مواد را فراهم می کنند ، خوانده می شوند خاص
4 نوع گیرنده زیر مشخص می شوند (شکل.
I. گیرنده هایی که به طور مستقیم عملکرد کانال های یونی را کنترل می کنند. این نوع گیرنده به طور مستقیم با کانال های یونی همراه است شامل گیرنده های n-کولینرژیک ، گیرنده های GABAA ، گیرنده های گلوتامات.
دوم گیرنده ها از طریق فرستنده های G-پروتئین های ثانویه یا سیستم کانال های یونی پروتئین های یونی به یک مؤثر تبدیل می شوند. چنین گیرنده هایی برای بسیاری از هورمون ها و واسطه ها (گیرنده های کولینرژیک m ، گیرنده های آدرنرژیک) در دسترس هستند.
III. گیرنده هایی که به طور مستقیم عملکرد آنزیم کارآمد را کنترل می کنند. آنها به طور مستقیم با تیروزین کیناز در ارتباط هستند و فسفوریلاسیون پروتئین را تنظیم می کنند. براساس این اصل ، گیرنده های انسولین ، تعدادی از فاکتورهای رشد چیده شده اند.
چهارم گیرنده هایی که رونویسی DNA را کنترل می کنند. بر خلاف گیرنده های غشایی از نوع I-III ، این گیرنده های داخل سلول (پروتئین محلول سیتوزولی یا هسته ای) هستند. هورمونهای استروئیدی و تیروئید با چنین گیرنده هایی در تعامل هستند.
با توجه به تأثیر مواد بر روی گیرنده های بعد از سیناپسی ، باید به احتمال اتصال آلوستریک به مواد درون زا (مثلاً گلیسین) و اگزوژن (به عنوان مثال سری آنزولیزیک بنزودیازپین) منشاء داد. تعامل Allosteric با گیرنده باعث ایجاد "سیگنال" نمی شود. با این حال ، مدولاسیون اثر اصلی واسطه وجود دارد ، که هم می تواند افزایش یابد و هم کاهش یابد. ایجاد مواد از این نوع امکانات جدیدی را برای تنظیم عملکرد سیستم عصبی مرکزی باز می کند. یکی از ویژگیهای عصب دهنده های عملکرد آلوستریک این است که آنها مستقیماً در انتقال واسطه اصلی تأثیر نمی گذارند بلکه فقط آن را در جهت دلخواه اصلاح می کنند.
نقش مهمی در درک مکانیسم های تنظیم انتقال سیناپسی با کشف گیرنده های پیش سیناپسی ایفا کرده است. راه های اتوروگلایز هموتروپیک (عمل واسطه ترشح کننده بر روی گیرنده های پیش سیناپسی همان انتهای عصب) و تنظیم هتروتروپی (تنظیم پیش سیناپسی به دلیل واسطه دیگر) رهاسازی واسطه ها مورد بررسی قرار گرفت که این امر باعث می شود تا دوباره ویژگی های عملکرد بسیاری از مواد بررسی شود. این اطلاعات همچنین به عنوان مبنای جستجوی هدفمند برای تعدادی از داروها (به عنوان مثال پرازوسین) قرار گرفت.
وابستگی ماده به گیرنده ، و منجر به تشکیل مجتمع "گیرنده ماده" با آن ، با اصطلاح "میل" مشخص می شود. توانایی یک ماده در تعامل با گیرنده برای تحریک آن و ایجاد یک اثر خاص ، فعالیت داخلی نامیده می شود.
5- عمل برگشت پذیر و برگشت ناپذیر. عمل انتخابی
بسته به قدرت پیوند "گیرنده ماده" ، یک عمل برگشت پذیر (مشخصه بیشتر مواد) و برگشت ناپذیر (معمولاً در مورد پیوند کووالانسی) از هم متمایز می شوند.
اگر یک ماده فقط با گیرنده های منحصر به فرد عملکردی از یک بومی سازی خاص در تعامل باشد و بر گیرنده های دیگر تأثیر نگذارد ، عمل چنین ماده ای انتخابی تلقی می شود. بنابراین ، برخی از عوامل شبیه به شکل بصورت کاملا انتخابی گیرنده های کولینرژیک صفحه انتهایی را مسدود می کنند و باعث آرامش عضلات اسکلتی می شوند. در دوزهایی که اثر میوپارالتیک دارند ، تأثیر کمی روی سایر گیرنده ها دارند.
مبنای انتخابی بودن عمل ، میل (میل) ماده به گیرنده است. این به دلیل وجود برخی از گروههای کاربردی خاص ، و نیز سازماندهی کلی ساختار ماده ای است که برای تعامل با این گیرنده ، مناسب ترین است ، یعنی مکمل آنها غالباً اصطلاح "عمل انتخابی" با دلیل خوب با اصطلاح "عمل ترجیحی" جایگزین می شود ، زیرا انتخاب مطلق عمل مواد عملاً وجود ندارد.
ارسال شده در Allbest.ru
اسناد مشابه
اثر ترکیبی داروها. ویتامین های K ، E ، B2 ، B6 ، C ، P: نقش بیولوژیکی ، نشانه ها. به معنای تنظیم عملکرد انقباضی رحم: طبقه بندی و مکانیسم عمل. عوامل ضد عفونی کننده و ضد ویروسی.
آزمون ، اضافه شده 1396/11/01
انواع اهداف مولکولی برای عمل به مواد مخدر. تأثیر ایزومریسم نوری بر فعالیتهای بیولوژیکی داروهای ضد التهابی غیر استروئیدی. ایزومتریک هندسی. تأثیر ایزومریسم هندسی بر عملکرد دارویی آنها.
مقاله اضافه شده 11/20/2013
کدگذاری دیجیتال داروها. تأثیر عوامل مختلف بر خواص مصرف کننده و کیفیت مواد مخدر ، راههای حمایت از کالاها در مراحل چرخه زندگی. اقدام دارویی ، نشانه ها داروها بر اساس chaga.
مقاله ترم ، اضافه شده 12/28/2011
تعریف و تاریخچه ظهور داروهای نوتروپیک ، طبقه بندی آنها با توجه به مکانیسم عمل و ساختار شیمیایی. مکانیسم عمل و اثرات اصلی داروهای نوتروپیک. اثربخشی استفاده از این داروها در عمل پزشکی.
چکیده ، اضافه شده 12/12/2012
ویژگی کلی میکوز. طبقه بندی داروهای ضد قارچ. کنترل کیفیت داروهای ضد قارچ. مشتقات ایمیدازول و تریازول ، آنتی بیوتیک های پلی آمین ، آلیلامین ها. مکانیسم عملکرد عوامل ضد قارچی.
مقاله ترم ، اضافه شده 14/4/2014
فارماکودینامیک به عنوان یکی از شاخه های اساسی فارماکولوژی. تفاوت بین اثرات اصلی و جانبی داروها. نقش اوراق قرضه یونی در مکانیسم عملکرد داروها. تعیین شاخص درمانی. تأثیر عوامل خارجی بر واکنش دارو.
چکیده ، اضافه شده 07/28/2010
طبقه بندی گروه دارویی فارماکوکینتیک ، مکانیسم عمل و فارماکودینامیک ، عوارض جانبیفرمهای آزاد و دوزها ، ویژگیهای دارویی: داروی استیل اسیدسیلیک (آسپیرین) ، سیپروفلوکساسین ، فرموترول.
کار آزمایشی ، اضافه شده در 12/22/2015
اهداف اصلی داروسازی: ایجاد داروها؛ مطالعه مکانیسم های عملکرد داروها؛ مطالعه فارماکودینامیک و فارماکوکینتیک داروها در آزمایش و عمل بالینی. داروسازی داروهای سیناپوتروپیک.
ارائه اضافه شده 04/08/2013
تاریخچه کشف آنتی بیوتیک ها. شرح دارویی عوامل ضد باکتریایی از اقدامات انتخابی و غیر انتخابی به عنوان اشکال داروها. اصول شیمی درمانی منطقی و خواص عوامل شیمی درمانی ضد میکروبی.
ارائه ، اضافه شده در 2014/04/28
دارو درمانی - قرار گرفتن در معرض مواد دارویی - بر اساس استفاده از ترکیب داروها ، ترکیب عملکرد علائم آنها. تعامل داروها: فیزیکی ، شیمیایی ، فارماکوکینتیک ، فارماکودینامیک.